1-プロパノール:特性、反応、製造および用途
1-プロパノールとは?
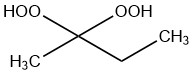
n-プロピルアルコールまたはプロパン-1-オールとも呼ばれる1-プロパノールは、化学式 CH3CH2CH2OH で表される第一級アルコールです。特有のアルコール臭を持つ無色透明の液体で、水、エタノール、エーテルと任意の割合で混和します。
1-プロパノールはイソプロピルアルコールの構造異性体ですが、産業界では溶剤や消毒剤として広く利用されている後者の方がより大きな重要性を持っています。
天然にはフーゼル油中に存在し、発酵の副産物として、あるいは植物性物質の変質・分解過程で微量に生成されます。
目次
- 1-プロパノールとは?
- 1. 1-プロパノールの物理的特性
- 2. 1-プロパノールの化学反応
- 3. 1-プロパノールの工業的生産
- 4. 1-プロパノールの用途
- 5. 1-プロパノールの毒性学
- 参考文献 (References)
1. 1-プロパノールの物理的特性
1-プロパノールは透明な無色の液体で、典型的なアルコール臭を有します。水と完全に混和するほか、エーテル、エステル、酸、ケトン、その他のアルコールを含む多くの有機溶媒に容易に溶解します。
n-プロパノールの物理的特性を表1にまとめます。
表1:1-プロパノールの物理的特性
| 特性 | 値 |
|---|---|
| CAS登録番号 | 71-23-8 |
| 化学式 | C3H8O |
| モル質量 (g/mol) | 60.09 |
| 凝固点 (°C) | −126.2 |
| 沸点 (°C) | 97.20 |
| 蒸気圧 (kPa) | 20 °Cにて: 1.987 40 °Cにて: 6.986 60 °Cにて: 20.292 80 °Cにて: 50.756 |
| アントワン式 (2–120 °C, tは°C) | log P(kPa) = 6.97257 − 1499.21 / (204.64 − t) |
| 蒸気密度 (空気 = 1) | 2.07 |
| 密度 (20 °C, g/cm3) | 0.80375 |
| フランシス式 (−21 to 180 °C, tは°C) | 密度 = 0.8813 + (5.448 × 10-4 t) − 21.536 / (313.09 − t) |
| 屈折率 (nD20) | 1.38556 |
| 粘度 (20 °C, mPa·s) | 2.256 |
| 表面張力 (20 °C, mN/m) | 23.75 |
| 臨界温度 (°C) | 263.65 |
| 臨界圧力 (kPa) | 5169.60 |
| 臨界密度 (g/cm3) | 0.275 |
| 熱容量 (液体, 25 °C, J/(mol·K)) | 141 |
| 蒸発熱 (kJ/mol) | 25 °Cにて: 47.53 97.20 °Cにて: 41.78 |
| 燃焼熱 (液体, 25 °C, kJ/mol) | 2033 |
| 生成熱 (蒸気, 25 °C, kJ/mol) | −254.7 |
| 引火点 (タグ開放式, °C) | 28.9 |
| 自然発火温度 (°C) | 371.1 |
| 爆発限界 (空気中, vol %) | 下限: 2.2 上限: 14.0 |
| 電気伝導率 (25 °C, S) | 2 × 10-8 |
2. 1-プロパノールの化学反応
1-プロパノールの化学的性質は、低分子量の第一級アルコールとして典型的です。ヒドロキシ基に特徴的な様々な反応、すなわち酸化、エステル化、アミノ化、脱水、およびエーテル化反応が起こります。生体系において、1-プロパノールは容易に分解され、最も生分解性の高いアルコールの一つと見なされています。
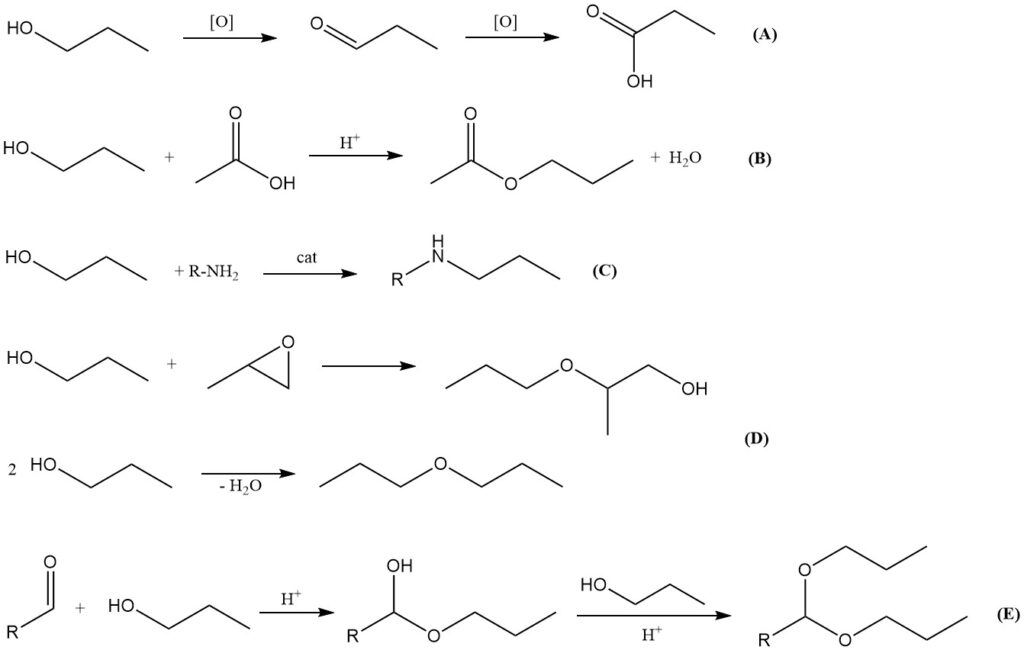
酸化反応 (A)
1-プロパノールの酸化は、まず対応するアルデヒドであるプロパナールへと進行し、さらなる酸化によってプロピオン酸を生じます。銅クロマイト、酸化クロム(VI)、またはピリジニウム塩などの金属触媒の存在下で、空気を用いることにより部分酸化を行うことが可能です。
エステル化反応 (B)
他のアルコールと同様に、1-プロパノールは有機酸および無機酸と反応してエステルを形成します。強酸触媒(例:硫酸、p-トルエンスルホン酸、メタンスルホン酸、またはイオン交換樹脂)の存在下で酢酸と反応させると、塗料、インク、香料産業で重要な溶剤として利用される酢酸n-プロピルが得られます。
また、酢酸メチルまたは酢酸エチルとのエステル交換反応によっても、酢酸n-プロピルを製造することができます。
アミノ化反応 (C)
1-プロパノールは、ニッケル、コバルト、モリブデンなどの遷移金属触媒の存在下、高温高圧条件でアンモニアまたはアミンと還元的アミノ化反応を起こします。この反応によりプロピルアミン誘導体が生成されますが、これらは対応するイソプロピルアミン誘導体と比較すると工業的な重要性は低くなります。
エーテル化および脱水反応 (D)
1-プロパノールをアルキレンオキシド(例:エチレンオキシド、プロピレンオキシド)と反応させると、溶剤として広く使用されるグリコールエーテルが得られます。固体酸触媒を用いて1-プロパノールを脱水すると、ジ-n-プロピルエーテルを生成できます。プロペンへの脱水も可能ですが、実用的な工業的意義はありません。
アセタール形成 (E)
他の第一級アルコールと同様に、1-プロパノールはアルデヒドと反応してヘミアセタールを形成し、脱水条件下の酸触媒存在下でさらにアセタールへと変換されます。1-プロパノール由来のアセタールは、医薬品合成における中間体として利用されます。
3. 1-プロパノールの工業的生産
工業的には、1-プロパノールは主にエチレンのヒドロホルミル化(オキソ法)によってプロパナール(プロピオンアルデヒド)を生成し、続いてそれを触媒水素化してアルコールにすることによって製造されます。
かつてはテキサス州ビショップにおいてセラニーズ社がプロパンの気相酸化プロセスを運用していましたが、このルートは1973年に廃止されました。それ以来、欧米ではオキソ(OXO)法が主要な製法となっています。
南アフリカでは、サソール(Sasol)社がフィッシャー・トロプシュ合成を通じて1-プロパノールを生産しています。プロピレンの反マルコフニコフ水和による1-プロパノール製造の試みも研究されていますが、商業的応用には至っていません。
3.1. ヒドロホルミル化および水素化による1-プロパノールの製造
ヒドロホルミル化(オキソ法)による1-プロパノールの商業生産は、2段階の工程で行われます。まず、エチレンを合成ガスを用いたヒドロホルミル化によりプロパナールに変換し(1)、次いでプロパナールを触媒水素化して1-プロパノールを得ます(2)。
(1) C2H4 + CO + H2 → CH3CH2CHO
(2) CH3CH2CHO + H2 → CH3CH2CH2OH
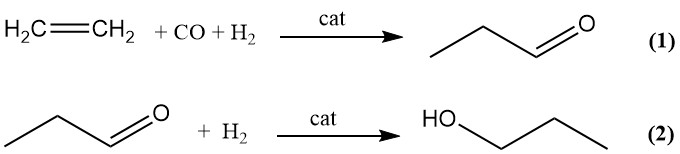
ヒドロホルミル化工程における微量な副生成物には、プロパン、1-プロパノール、およびアルドール縮合によって形成される高沸点副生成物(ヘビーエンド)が含まれます。コバルト、鉄、ニッケル、ロジウム、イリジウムの遷移金属カルボニル錯体はオキソ反応を触媒することができますが、商業的に利用されているのはコバルトとロジウムのみです。
米国では、Texas Eastman、Union Carbide、およびHoechst Celaneseにおいてオキソ技術を用いた1-プロパノールの製造が行われています。Texas Eastman社は当初、コバルトベースの HCo(CO)4 触媒を使用していましたが、1989年にホスフィン修飾ロジウム系を採用しました。欧州では、Hoechst AGおよびBASF AGによって生産が行われています。
ロジウム–トリフェニルホスフィン触媒は、反応速度の向上、安定性の改善、操作圧力の低減、および副生成物の減少により、コバルト触媒に代わって広く普及しました。ロジウムカルボニルは、元々コバルト触媒用に設計されたプラントにも適応可能です。
ロジウムはより高い圧力を必要とするものの、その活性は非常に高く、高沸点留分の生成も抑えられます。ドイツのHoechst AG(Ruhrchemie工場)では、ロジウムカルボニルを用いてプロパナールを合成し、これを水素化して1-プロパノールを製造しています。ロジウムカルボニルは、コバルト類似体よりも100〜1,000倍高い反応性を持つと報告されています。
ロジウム触媒によるエチレンのヒドロホルミル化は、90〜120 °C、2.17〜3.55 MPa、H2:CO比 1:1〜3:1、ロジウム濃度 1〜10 mM、トリフェニルホスフィン濃度 0.1〜0.4 M の条件で実施されます。これらの条件下で、プロパナールの収率は98〜99%に達し、エタンおよびヘビーエンドへの転換は0.5〜1.0%に抑えられます。
ハロゲンを含むロジウム源は、ハロゲン化錯体が低いヒドロホルミル化性能を示すため、触媒活性を抑制します。最も活性の高い触媒前駆体はヒドリドカルボニルトリス(トリフェニルホスフィン)ロジウム、HRhCO[P(C6H5)3]3 であり、これはトリフェニルホスフィンリガンドの解離によって活性種を生成します。
過剰なトリフェニルホスフィンは、リンからロジウムへのフェニル基移動による触媒の失活を抑制します。この移動が起こると、不活性なロジウム–ホスフィドクラスターが形成される原因となります。
プロパナールから1-プロパノールへの水素化は確立されたプロセスです。ラネーニッケルや担持ニッケルなどのニッケル系触媒、および銅–酸化クロム触媒が一般的に使用されます。水素化方法には、気相法と液相法の両方が採用されています。
液相操作は 2.17〜4.24 MPa、100〜170 °C で行われます。気相水素化は通常 790 kPa 以下で操作されます。反応器の形式としては、固定床、スラリー床、またはトリクルベッド(滴下床)方式が用いられます。1-プロパノールの収率は95%以上を達成しています。
副生成物には、アセタール、エーテル、エステル、およびジオールが含まれます。COおよびトリフェニルホスフィンは共に触媒毒として作用するため、水素化の前に原料から除去する必要があります。
工業的な操作では、オキソ反応器の流出物から過剰な合成ガスを用いてプロパノールの蒸気をストリッピングし、続いて凝縮および水素化前のCO除去が行われます。得られた粗1-プロパノールは、2塔式の蒸留システムで精製されます。
コバルトカルボニルまたはロジウムカルボニル触媒を使用する場合、反応器圧力が高いためプロパナールの液体引き抜きが必要となり、触媒の回収および取り扱いのための追加設備が必要となります。
3.2. サソール(Sasol)のフィッシャー・トロプシュ法による1-プロパノールの生産
サソール社は、フィッシャー・トロプシュ(FT)合成の副次生成物として1-プロパノールを生産しています。このプロセスでは、Lurgi固定床反応器で石炭をガス化し、合成ガス(COおよびH2)を生成します。ガス流は凝縮性成分から分離・精製された後、Sasol Syntholユニットに導入されます。
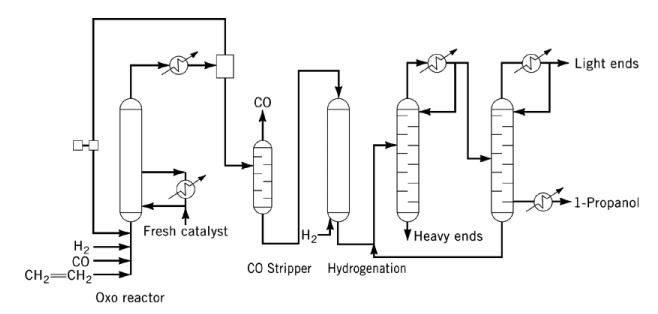
流動床反応器内でガスは微細な鉄系触媒と接触し、極めて強い発熱を伴うフィッシャー・トロプシュ反応によって、炭化水素と含酸素化合物の混合物が生成されます。
反応器からの凝縮液は、炭化水素分画と水相に分離されます。水相ストリームにはアルコールとケトンの混合物が含まれています。アルコールの大部分は高オクタン価ガソリンにブレンドされますが、特定のアルコール分画は純製品の回収のために蒸留工程に送られます。
これらの工程から、1-プロパノールとエタノールが多段分離システムで単離され、その年間の総生産能力は約25,000〜30,000トンに達します。
4. 1-プロパノールの用途
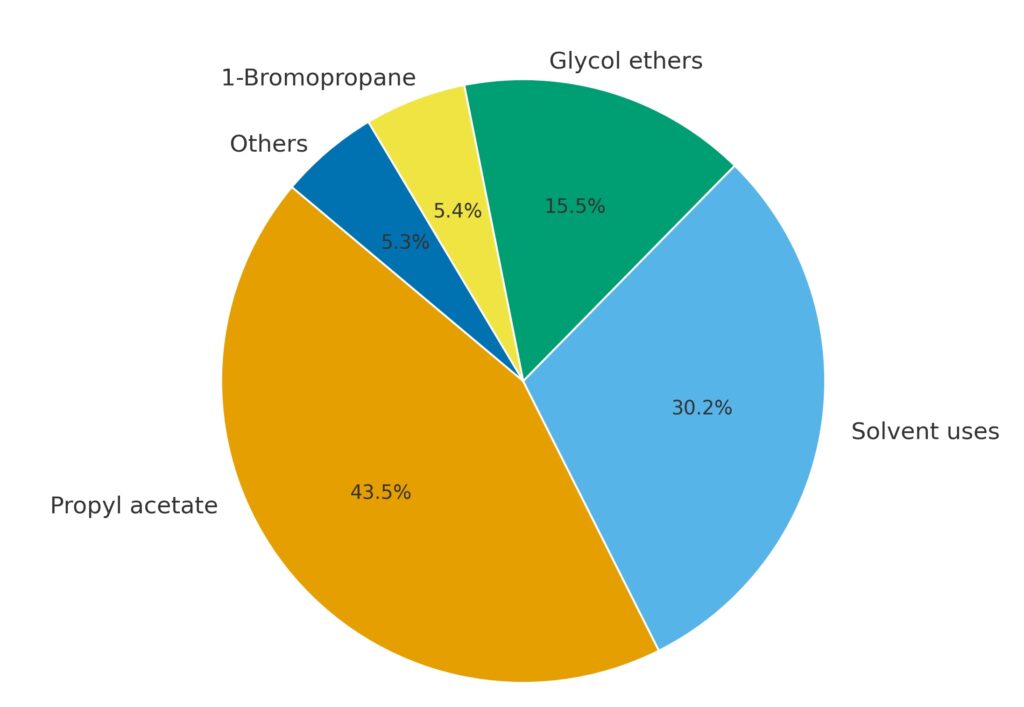
1-プロパノールは主に溶剤および化学中間体として使用されます。最も重要な誘導体は酢酸n-プロピルであり、これが世界全体の消費量の大部分を占めています。
1-プロパノールは、フレキソ印刷およびグラビア印刷用インクの溶剤として広く利用されており、特にポリオレフィンやポリアミドフィルムへの印刷に適しています。エタノールや2-プロパノールと比較して、印刷品質や乾燥挙動の面で優位性があります。また、塗料、コーティング剤、化粧品、農薬、殺虫剤の溶剤としても使用されています。
欧州では、細菌、真菌、ウイルスに対する高い殺菌(バイオサイド)活性を持つことから、手指および表面消毒剤の成分としての重要性がますます高まっています。
1-プロパノールの大部分は酢酸n-プロピルへと転換され、インク、ラッカー、セルロース誘導体、ワックス、殺虫剤製剤の溶剤として使用されます。プロピオン酸n-プロピルなどの他のエステル類はコーティング剤に使用されており、臭気特性が改善されていることから、酢酸n-ブチルの代替品と見なされています。
1-プロパノールは、エチレングリコールモノプロピルエーテル、ジエチレングリコールモノプロピルエーテル、プロピレングリコールモノプロピルエーテル、ジプロピレングリコールモノプロピルエーテルなどのグリコールエーテル類を製造するための原料です。これらの溶剤は、高い溶解性と水への親和性を兼ね備えており、コーティング剤や洗浄剤に使用されます。
欧州では、1-プロパノールのかなりの割合がプロピルアミン類に転換されます。これらは除草剤や医薬品製造の中間体となります。
また、1-プロパノールは、塩化メチレンやオゾン層破壊物質の代替溶剤として使用される1-ブロモプロパンの前駆体でもあります。その他の用途としては、香料成分、農薬製剤の補助溶剤、飼料添加物などが挙げられます。
5. 1-プロパノールの毒性学
1-プロパノールは、引火点が38 °C未満の引火性液体に分類されます。米国労働安全衛生局(OSHA)の 29 CFR 1910.1200 に基づき、有害物質として規制されています。
毒性研究によれば、1-プロパノールの動物に対する毒性はわずかです(表2)。エームス試験およびマウスリンパ腫前向き変異試験において陰性の結果を示しており、変異原性はないと考えられます。
表2:1-プロパノールの毒性データ
| 投与方法 / パラメータ | 値 |
|---|---|
| 経口投与、ラット、LD50 | 1.9 g/kg |
| 経皮、ウサギ、LD50 | 5.4 g/kg |
| 吸入、ラット、LC50 | 24,000 ppm |
| ACGIH TLV, TWA | 200 ppm |
| 有害性評価 (NFPA: 健康, 火災, 反応性) | 1, 3, 0 |
| 有害性評価 (HMIS: 健康, 火災, 反応性) | 2, 3, 0 |
注:LD50 = 半数致死量。LC50 = 半数致死濃度。TLV = 許容濃度。TWA = 時間加重平均値。
米国国家毒性プログラム(NTP)および国際がん研究機関(IARC)は、1-プロパノールを発がん性物質として分類していません。急性曝露は眼の刺激や化学火傷を引き起こす可能性があり、皮膚への繰り返し接触は皮膚炎につながる恐れがあります。過剰な濃度の蒸気を吸入すると眼や気道を刺激し、極めて高い濃度では麻酔作用を引き起こす可能性があります。
米国において、1-プロパノールは包括的環境対処・補償・責任法(CERCLA)にリストされており、報告義務のある漏洩量は1日あたり 100 lb(45.4 kg)です。また、40 CFR 60.489 に基づく大気排出基準にも含まれており、製造設備からの揮発性有機化合物(VOC)排出の抑制が求められています。米国のいくつかの州では、情報公開法(Right-to-know rules)に基づいてリストアップされています。
食品および農薬規制において、1-プロパノールは 21 CFR 172.515 に基づき着香料および助剤として許可されており、農薬製剤の溶剤または補助溶剤として使用される場合は、残留許容基準の適用から除外されています。
参考文献 (References)
1. Unruh, J.D. and Pearson, D. (2000). n-Propyl Alcohol. In Kirk-Othmer Encyclopedia of Chemical Technology, (Ed.). https://doi.org/10.1002/0471238961.1618151621141821.a01
2. Klabunde, J., Bischoff, C. and Papa, A.J. (2025). Propanols. In Ullmann’s Encyclopedia of Industrial Chemistry. https://doi.org/10.1002/14356007.a22_173.pub3