エチレンジアミン四酢酸 (EDTA): 性質、製造および用途
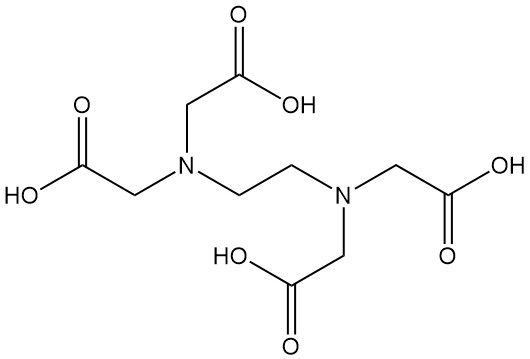
エチレンジアミン四酢酸とは何か?
エチレンジアミン四酢酸(通称EDTA)は、化学式 C10H16N2O8 で表されるアミノポリカルボン酸です。水に不溶な白色固体であり、さまざまな産業で最も一般的に使用されるキレート剤の一つです。
エチレンジアミン四酢酸 (EDTA)、ニトリロ三酢酸 (NTA)、およびそれらの塩は、1930年代にI.G. Farbenindustrieの研究室のFerdinand Munzによって初めて合成されました。以来、工業用キレート剤として極めて重要な地位を築いています。
EDTAのようなアミノポリカルボン酸は、アミノ酸と同様に強酸や強塩基と塩を形成することができます。さらに、二価および三価の陽イオンと強力な水溶性錯体を形成する能力を持っています。これらの錯体は金属イオンの反応性を著しく変化させるため、多種多様な工業プロセスにおいて価値のある化合物となっています。
EDTAの主な工業的用途は、カルシウム、バリウム、鉄、その他の陽イオンを含むスケールや不溶性沈殿物の生成防止、あるいはその除去です。
目次
- エチレンジアミン四酢酸とは何か?
- 1. エチレンジアミン四酢酸 (EDTA) の物理的性質
- 2. エチレンジアミン四酢酸の化学的性質
- 3. エチレンジアミン四酢酸 (EDTA) の製造
- 4. エチレンジアミン四酢酸 (EDTA) の用途
- 5. EDTAの毒性
- 参考文献
1. エチレンジアミン四酢酸 (EDTA) の物理的性質
エチレンジアミン四酢酸は、水にわずかに溶ける無色の結晶性固体です。EDTAの主要な物理的性質を下表に示します。
表1: EDTAの物理的性質
| 項目 | 値 |
|---|---|
| CAS番号 | [60-00-4] |
| 化学式 | C10H16N2O8 |
| 分子量 | 292.24 g/mol |
| 融点 | 245 °C (分解) |
| 相対密度 | 0.86 g/cm3 |
| 水への溶解度 (20 °C) | 0.1 g/L |
| pKa1 | 2 |
| pKa2 | 2.7 |
| pKa3 | 6.16 |
| pKa4 | 10.26 |
| 引火点 | > 100 °C |
2. エチレンジアミン四酢酸の化学的性質
EDTAは、二価および三価の金属陽イオンと水溶性錯体を形成します。これらの錯体はキレート(ギリシャ語の「chele(蟹のハサミ)」に由来)と呼ばれる環状構造を特徴としており、金属イオンは解離したリガンドである EDTA4- によって強固に結合されます。
この錯体の強さは安定度定数によって数値化され、金属イオン (M) とキレート剤 (EDTA4-) の平衡濃度を反映します。
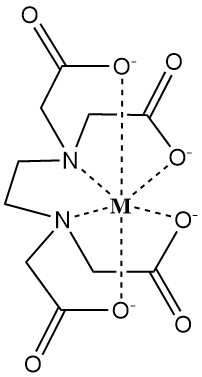
キレート強度に影響を与える要因には、pH、競合アニオン、および沈殿アニオンがあります。
高いpHは、完全に解離したキレートアニオン(例:EDTA4-)の濃度を高め、結合能力を向上させるため、キレート化に有利に働きます。しかし、高いpHでは水酸化物イオン (OH–) の影響を受ける可能性があり、金属が不溶性の水酸化物を形成する場合(例:pH 5.5以上での Fe3+ の沈殿)、金属キレートが破壊されることがあります。
炭酸塩、リン酸塩、シュウ酸塩などのアニオンはキレート剤と競合し、金属-キレート剤錯体の実効強度を低下させる可能性があります。
一般的に、EDTAのようなキレート剤は金属イオンと 1:1 の錯体を形成します。ただし、キレート剤の濃度を 1:1 以上に高めることで、安定性をさらに向上させることができます。
金属陽イオンをアニオン性金属錯体に変換すると、他の物質との相互作用が変化します。例えば、負に帯電した [Fe(III)(EDTA)]– 錯体は、吸着されやすい Fe3+ 陽イオンと比較して、土壌中をより容易に移動できます。
キレート化は、錯体形成によって遊離金属イオン (M) の濃度を低下させ、実効的な酸化電位を実質的に上昇させます。この原理は、さまざまな重要な工業プロセスの基礎となっています。
3. エチレンジアミン四酢酸 (EDTA) の製造
かつてエチレンジアミン四酢酸 (EDTA) は、エチレンジアミン、クロロ酢酸、および水酸化ナトリウムの反応によって商業的に製造されていました。しかし、このプロセスでは製品が塩化ナトリウムで汚染され、精製が困難であるため、現在は廃止されています。
特定の原料の触媒酸化などの他の方法も検討されましたが、商業的に採用されるには至りませんでした。
今日では、親ポリアミンのシアノメチル化を伴う2つの主要なプロセスが、EDTAおよび関連キレート剤の製造を支配しています。
3.1. エチレンジアミンのアルカリシアノメチル化
エチレンジアミンのアルカリシアノメチル化は、エチレンジアミン四酢酸を合成するために最も広く使用されているプロセスです。
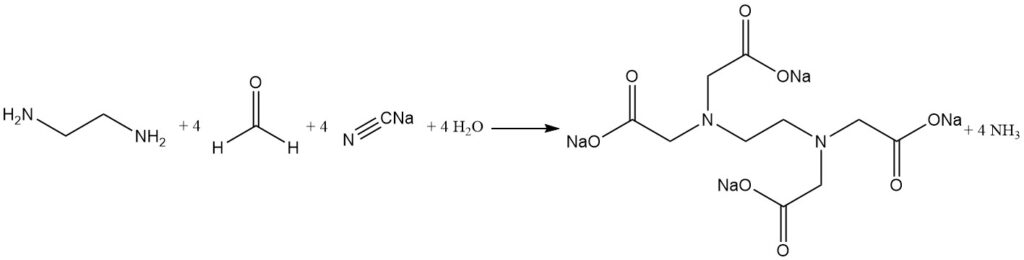
シアン化ナトリウムとホルムアルデヒドをエチレンジアミンと反応させることで、高収率(90%以上)でEDTAが製造されます。副産物としてアンモニアが生成されますが、反応中に連続的に除去されます。ただし、微量のアンモニアが反応し、ニトリロ三酢酸やグリシンなどの不要な副産物の塩が形成されることがあります。
原料間の反応からグリコール酸塩が形成されることもありますが、これらの不純物がほとんどのキレート剤用途に与える影響は軽微です。
3.2. 2段階シンガー合成 (Singer synthesis)
2段階シンガー合成では、シアノメチル化工程と加水分解反応を分離します。ここでは、シアン化水素とホルムアルデヒドをエチレンジアミンと反応させ、中間生成物である (エチレンジニトリロ)四アセトニトリルを高収率(96%以上)で形成します。
この不溶性の中間体を単離・洗浄した後、水酸化ナトリウムで加水分解することで、副産物としてアンモニアを伴う純粋なEDTA四ナトリウムを得ることができます。反応を2段階に分けることで、不純物の生成を最小限に抑え、高度に精製されたキレート剤を製造することが可能になります。
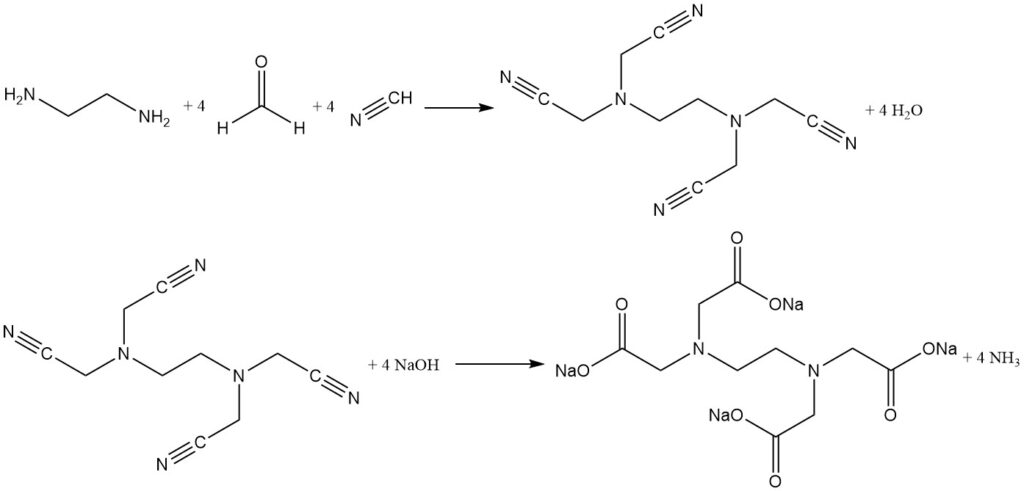
この2段階のアプローチは、アンモニアを用いた純粋なニトリロ三酢酸の効率的な製造にも使用されています。
4. エチレンジアミン四酢酸 (EDTA) の用途
金属イオンを結合して不活性化するという独自の能力を持つEDTA型キレート剤は、さまざまな産業で応用されています。
- 繊維・染料工業: 繊維、化学薬品、水に含まれる微量金属不純物を錯体化することで、染料の不要な変色を防ぎます。
- パルプ・製紙工業: 過酸化水素やジチオン酸塩で漂白された紙パルプの白色度を向上させます。蒸解および漂白段階で安定剤および金属イオン制御剤として機能します。
- ボイラーの洗浄とスケール防止: ボイラーからのスケール堆積物の洗浄に使用され、カルシウムやマグネシウムイオンを錯体化することでスケールの形成を防ぎます。ただし、過剰なキレート剤による腐食を避けるために適切な用量管理が重要です。
- 金属表面処理: 付着した酸化被膜を溶解することで金属表面の洗浄を助け、徹底的なすすぎを可能にします。めっき液には、滑らかで均一な金属被覆を得るためにEDTAが添加されます。
- 洗剤・クリーナー: 洗濯洗剤、硬質表面用クリーナー、浴室用洗剤に添加され、洗浄力を高めます。
- 殺菌・化粧品: 特定の細菌(特にグラム陰性菌)の外細胞壁を破壊し、殺菌剤の効果を高めます。また、化粧品、シャンプー、眼科製品の防腐助剤としても機能します。
- 食品工業: マヨネーズやドレッシングなどの脂肪乳濁液において、腐敗を促進する金属イオンを錯体化することで酸化による酸敗を防ぎます。また、ジャガイモなどの食品における鉄による変色を防ぎます。
- 農業(肥料): 鉄、亜鉛、マンガン、銅などの微量元素がキレート形態で肥料に添加されます。これにより、リン酸塩などの土壌成分との相互作用による沈殿を防ぎ、植物による吸収効率を高めます。
- 化学分析: 当量点での遊離金属イオン濃度の急激な変化を利用した滴定法(キレート滴定)で広く使用されます。また、分光光度法におけるマスキング剤としても利用されます。
5. EDTAの毒性
EDTAとその塩は、食品添加物、医薬品、化粧品など、さまざまな用途で長年にわたる安全な使用実績があります。初期の毒性試験では、比較的低い毒性が示されています。ラットを用いた研究では、Na2EDTA(二ナトリウム塩)の半数致死量 (LD50) は体重1kgあたり2.0〜2.2gと報告されています。
Na2EDTAを飼料中に0.5%から5.0%含ませた研究では、最高投与量での下痢と摂食量の減少を除き、顕著な悪影響は見られませんでした。また、EDTA三ナトリウムは皮膚感作物質ではないと考えられています。
EDTAは遺伝物質と相互作用する可能性がありますが、ヒトに対する遺伝毒性(遺伝的損傷を引き起こす性質)の関連性は極めて低いと考えられます。Na3EDTA(三ナトリウム塩)を用いた研究では、化合物に関連する発がん性は示されていません。
参考文献
Ethylenediaminetetraacetic Acid and Related Chelating Agents; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a10_095.pub2