타르타르산: 성질, 반응, 생산 및 용도
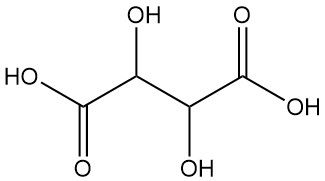
주석산으로도 잘 알려진 타르타르산(Tartaric acid)은 IUPAC 명명법으로 2,3-디히드록시부탄디산(2,3-dihydroxybutanedioic acid)이라 불리며, 많은 과일에서 천연적으로 발견되는 백색 결정성 유기산입니다. 화학식은 C4H6O6입니다. 이 분자는 두 개의 비대칭 탄소 중심과 두 개의 카르복실산 그룹, 그리고 동일 분자 내에 디알코올 구조를 가지고 있어 총 네 가지의 입체 이성질체가 존재합니다.
거울상 이성질체:
L(+)-타르타르산과 D(-)-타르타르산은 편광의 평면을 회전시키는 광학 활성 이성질체입니다. 이 거울상 이성질체들은 서로 반대 방향의 광학 회전도를 갖는 것을 제외하고는 동일한 물리적, 화학적 성질을 공유합니다.
부분 입체 이성질체:
DL-타르타르산(라세미 혼합물)은 L(+)형과 D(-)형이 등몰량으로 결합된 합성 혼합물입니다. 이는 내부 보상 작용으로 인해 광학적으로 불활성입니다.
메조(Meso)-타르타르산은 광학 활성형이나 라세미형과는 다른 뚜렷한 물리적 성질을 가진 또 다른 광학 불활성 부분 입체 이성질체입니다. 라세미형과 메조형 모두 광학 활성을 나타내지 않는 산입니다.
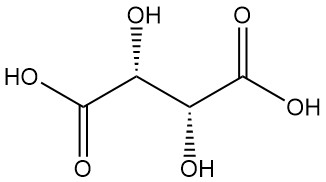
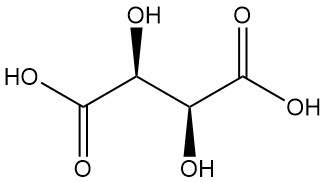
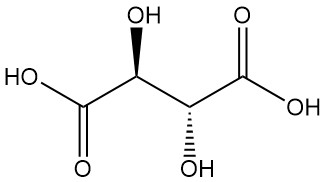
타르타르산은 고대부터 그 칼륨염(주석)으로 알려져 왔으며, 18세기에 쉴레(Scheele)에 의해 처음으로 분리되었습니다. 베르셀리우스(Berzelius)는 1830년에 그 구조를 결정했습니다. 파스퇴르(Pasteur)의 타르타르산염에 관한 획기적인 연구(1848–1860)는 유기 화학에 혁명을 일으켰습니다.
그는 타르타르산 나트륨 암모늄 결정을 분리하고 각각의 광학 회전도를 입증함으로써 라세미형과 광학 활성형 사이의 관계를 설명했습니다.
L(+)-타르타르산은 가장 지배적인 천연 형태이자 상업적으로 생산되는 변체입니다. 이는 다양한 식물, 특히 포도에서 산 또는 염의 형태로 발견되며, 와인 발효 과정 중에 주석산 수소 칼륨(주석)으로 축적됩니다. 이 불용성 침전물이 상업적인 L(+)-타르타르산 생산의 주요 원료가 됩니다.
목차
- 1. 타르타르산의 물리적 성질
- 2. 타르타르산의 화학 반응
- 3. 타르타르산의 천연 자원
- 4. 타르타르산의 생산
- 5. L(+)-타르타르산의 유도체
- 6. 타르타르산의 용도
- 7. 타르타르산의 독성
- 참고 문헌
1. 타르타르산의 물리적 성질
천연 L(+)-타르타르산의 물리적 성질은 표 1에 제시되어 있으며, 이는 D(-)-타르타르산의 성질과 동일합니다. 타르타르산은 냄새가 없는 고체로 강한 산미를 지니며 공기 중에서 안정합니다.
타르타르산 용액의 광학 회전도는 농도에 따라 달라지며, 다음과 같은 방정식으로 표현됩니다:
[α] = 15.050 – 0.1535 c
여기서 c는 20~50% wt/vol 범위의 타르타르산 농도입니다.
표 2는 다양한 온도에서의 용해도를 나타내며, 표 3은 온도에 따른 타르타르산 용액의 상대 밀도를 보여줍니다.
표 1: 물리적 성질
| 성질 | 값 |
|---|---|
| 분자량 | 150.09 g/mol |
| 결정 형태 | 무수 단사정계 침상 (5 °C 이상) |
| 밀도 | 1.7598 g/cm3 |
| 녹는점 | 169–170 °C |
| 외관 | 무색 결정 |
| 분해 | 220 °C 이상 (카라멜화된 설탕 냄새) |
| 용해도 (물) | 매우 높음 |
| 용해도 (알코올, 18 °C) | 100g당 20.4g |
| 용해도 (디에틸 에테르, 18 °C) | 100g당 0.3g |
| 광학 회전도 (20% wt/vol) | +11.98° (D형은 -11.98°) |
| 연소 엔탈피 | 1149.9 kJ/mol |
| 비열 용량 (0-100 °C) | 1237 kJ kg-1 K-1 |
| 산 해리 상수 (25 °C) | K1 = 1.17 × 10-3 K2 = 5.0 × 10-5 |
| 용액의 끓는점 | 25% 용액: 102.2 °C 50% 용액: 106.7 °C |
| 굴절률 (녹는점 170 °C) | 1.464 |
표 2: 온도에 따른 물 용해도 (g/100 g H2O)
| 온도 (°C) | 0 | 5 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| 용해도 | 115 | 120 | 125 | 139 | 156 | 176 | 195 | 218 | 244 | 273 | 307 | 343 |
표 3: 온도에 따른 밀도
| 온도 (°C) | 밀도 |
|---|---|
| 1 | 1.0045 |
| 10 | 1.0469 |
| 20 | 1.0969 |
| 30 | 1.1505 |
| 40 | 1.2078 |
| 50 | 1.2696 |
2. 타르타르산의 화학 반응
L(+)-타르타르산은 170-180 °C 사이에서 녹으며 수분 손실 없이 메타타르타르산으로 이성화(구조 재배열)됩니다. 추가로 가열하면 무정형 무수물이 생성됩니다. 이 무수물들은 물과 함께 끓이면 다시 타르타르산으로 돌아갑니다.
220 °C 이상에서는 타르타르산이 분해되고 부풀어 오르며 발화하여 탄소질 잔류물을 남깁니다.
타르타르산은 산화제에 매우 민감합니다. 과산화수소와 황산제일철(펜톤 시약)에 의한 타르타르산의 산화는 디옥소석신산(dioxosuccinic acid)을 생성합니다.
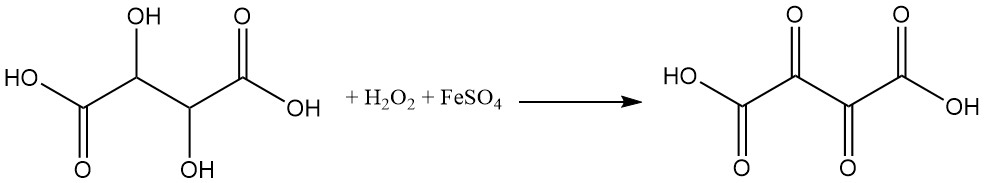
요오드화수소산으로 환원하면 석신산(succinic acid)이 생성됩니다.
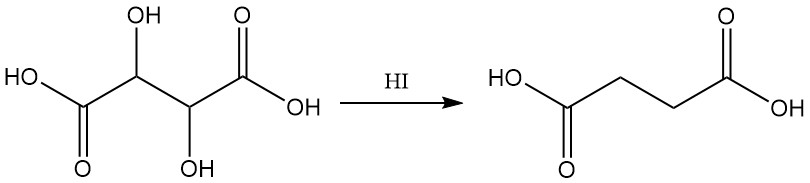
용액 내의 타르타르산염은 암모니아성 질산은과 반응하여 금속 은을 생성합니다(은거울 반응).
타르타르산은 염기에 의한 중금속 염의 침전을 억제하는 착화제(complexing agent)로 사용됩니다.
알칼리(KOH 또는 NaOH)와 함께 L(+)-타르타르산 용액을 장시간 끓이면 라세미형 및 메조-타르타르산이 형성됩니다.
3. 타르타르산의 천연 자원
L(+)-타르타르산은 상업적으로 대규모 생산되는 유일한 이성질체입니다. 유일한 원료는 와인 제조 과정에서 발생하는 천연 잔류물에서 나옵니다. 이러한 잔류물에는 주로 주석산 수소 칼륨(주석, cream of tartar) 형태의 타르타르산이 포함되어 있으며, 적은 양의 타르타르산 칼슘도 포함되어 있습니다.
타르타르산의 자원은 다음과 같습니다:
- 주석 (Tartar): 에탄올 농도가 높아짐에 따라 와인 통 벽에 달라붙는 붉은색 침전물입니다. 높은 농도(80–90%)의 주석산 수소 칼륨을 함유하고 있습니다.
- 침전물 (Lees): 와인 통 바닥에 가라앉는 침전물로, 낮은 농도(19–38%)의 주석산 수소 칼륨을 함유합니다.
- 건조 침전물: 더 높은(55-70%) 주석산 수소 칼륨 함량을 갖도록 가공된 침전물입니다.
- 증류 부산물: 증류소는 와인 침전물이나 포도 박(포도를 짠 후 남은 고형물)에서 이 물질을 얻습니다. 증류로 알코올을 제거한 후, 침전물이나 포도 박을 수산화칼륨으로 처리하여 타르타르산 칼슘을 침전시킵니다.
4. 타르타르산의 생산
여러 타르타르산 이성질체가 존재하지만, 상업적으로 대규모 생산되는 것은 L(+)-타르타르산이 유일합니다. 매우 적은 양의 라세미산도 특정 용도를 위해 합성됩니다.
4.1. L(+)-타르타르산의 생산
L(+)-타르타르산의 주요 생산국은 스페인, 프랑스, 이탈리아입니다. 예를 들어 1784년에 설립된 Société Legré-Mante는 가장 오래된 생산 업체 중 하나입니다.
L(+)-타르타르산 생산의 모든 방법은 황산을 이용한 타르타르산 칼슘의 분해에 의존합니다. 역사적으로 시작 물질(타르타르산 칼슘)을 얻기 위해 쉐러-케스트너(Scheurer-Kestner) 산성 공정과 쉴레-로비츠(Scheele-Lowitz) 중성 공정(Desfosses 변형 포함)이라는 두 가지 경쟁적인 방법이 사용되었습니다. 현재는 더 경제적인 중성 공정이 지배적인 방법입니다.
먼저 건조된 시작 물질(주석 또는 침전물)을 분쇄한 후 로스터에서 160 °C로 2시간 동안 로스팅합니다. 이 단계는 이후 단계에서 여과를 어렵게 만들 수 있는 유기 불순물을 제거합니다.
가열된 로스팅 생성물은 반응기로 옮겨져 물로 희석되고 수산화칼슘을 사용하여 pH 5까지 중화됩니다. 반응 온도는 70 °C로 유지됩니다.
반응 효율을 높이고 손실을 최소화하기 위해, 화학 양론적 요구량에 비해 10% 과량의 염화칼슘 또는 황산칼슘을 첨가합니다. 다음과 같은 화학 반응이 일어납니다:
2 KHC4H4O6 + Ca(OH)2 + CaCl2 → 2 CaC4H4O6 + 2 KCl + 2 H2O
형성된 타르타르산 칼슘은 회전식 여과기를 사용한 여과를 통해 남은 액체(모액)로부터 분리된 후 세척됩니다. 시작 물질이 증류소에서 온 경우 이 초기 단계는 생략될 수 있습니다.
두 번째 단계에서는 얻어진 타르타르산 칼슘을 황산을 사용하여 수용액 상태에서 분해합니다. 이 반응을 통해 타르타르산 용액과 불용성 황산칼슘이 생성됩니다:
CaC4H4O6 + H2SO4 → H2C4H4O6 + CaSO4
반응을 최적화하기 위해 타르타르산 양에 비해 약 5% 과량의 황산을 사용합니다. 생성된 혼합물은 여과 및 세척되어 불순물이 제거됩니다.
약 200 g/L 농도의 붉은색 타르타르산 용액은 진공 증발기에서 70 °C로 농축되어 650 g/L 농도에 도달합니다. 결정이 형성되기 시작할 때까지(약 1300 g/L) 70 °C 진공 하에서 추가 농축이 진행됩니다.
이 액체-결정 혼합물은 결정화기로 옮겨져 천천히 냉각되며, 이를 통해 결정 수율을 최대화합니다. 냉각 후 혼합물은 원심 분리기에서 건조되어 모액으로부터 결정을 분리합니다.
여전히 타르타르산을 포함하고 있는 모액은 증발, 과립화 및 건조 과정을 반복하여 과립형 타르타르산의 수율을 최대화합니다. 얻어진 과립은 냉각되어 650 g/L 타르타르산 용액을 형성합니다.
이 용액은 활성탄을 이용한 탈색과 과잉 철분 및 황산을 제거하기 위한 화학적 정제 과정을 70 °C에서 거칩니다. 그 후 여과되어 결정화가 시작될 때까지 진공 하에서 농축됩니다.
혼합물은 다시 결정화기로 옮겨지거나 냉각되어 결정 수율을 최대화합니다. 이후 원심 분리에 의해 분리됩니다. 잔류 타르타르산이 포함된 모액은 재처리되기 전에 증발, 과립화 및 건조 과정을 더 거칩니다.
정제된 과립은 140 °C의 오븐에서 건조된 후 2000 μm에서 100 μm 미만(분말)까지 다양한 입자 크기로 체질됩니다.
위에 기술된 공정이 주요 방법이지만, 다른 생산 공정도 탐구되어 왔습니다. 여기에는 발효 기반의 L(+)-타르타르산 생산과 라세미 DL-타르타르산의 화학적 합성이 포함됩니다.
4.2. 발효에 의한 L(+)-타르타르산 생산
전통적인 L(+)-타르타르산 생산 방법은 화학 반응에 의존하지만, 발효 기반 대안에 대한 연구가 진행 중입니다. 이 목적으로 두 가지 주요 박테리아 균주가 연구되었습니다:
- 아세토박터 서브옥시다스 (Acetobacter suboxydans): 이 박테리아 종은 포도당을 L(+)-타르타르산으로 전환하는 능력에 대해 연구되었습니다.
- 노카르디아 타르타리칸스 (Nocardia tartaricans): 이 박테리아는 시스-에폭시석신산과 그 나트륨 유도체를 원하는 생성물로 전환하는 데 유망한 것으로 보입니다.
4.3. 라세미 DL-타르타르산의 화학적 합성
L(+)-타르타르산이 상업 시장을 지배하고 있지만, 라세미 DL-타르타르산을 위한 소규모 생산 공정이 존재합니다.
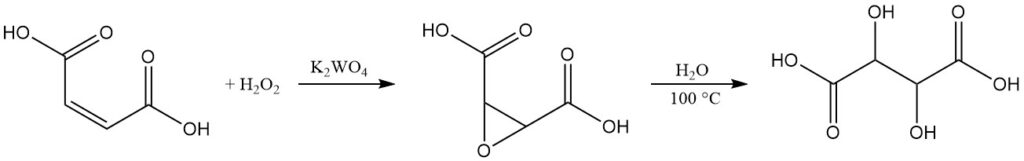
이 방법은 말레산 또는 그 염에서 시작합니다. 수용액에서 말레산은 텅스텐산 칼륨을 촉매로 하여 35% 과사화수소를 사용하여 산화됩니다. 이 반응은 중간 생성물인 에폭시-석신산을 생성합니다.
반응 혼합물을 끓임으로써 에폭시-석신산이 가수분해되어 라세미 타르타르산을 형성합니다. 냉각 후, 최종 생성물은 원심 분리, 세척 및 건조를 통해 분리됩니다.
이 공정의 여러 변형이 과학 문헌에 기록되고 탐구되었습니다. 이러한 연구 활동은 이 방법과 관련하여 제출된 수많은 특허 출원에 반영되어 있습니다. 현재 라세미 DL-타르타르산의 상업적 생산은 제한적이며, 남아프리카에서 단 하나의 소규모 생산 단위만이 운영되고 있습니다.
5. L(+)-타르타르산의 유도체
타르타르산은 수많은 염과 에스테르를 쉽게 형성하며, 그 중 일부는 중요한 상업적 용도로 사용됩니다. 이 섹션에서는 가장 잘 알려진 화합물들에 대해 논의합니다.
5.1. 타르타르산 나트륨 칼륨
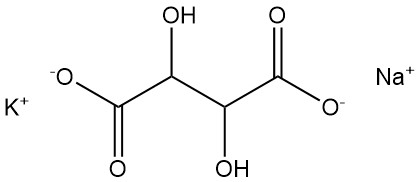
세네트염(Seignette’s salt) 또는 로셸염(Rochelle salt)으로도 알려진 타르타르산 나트륨 칼륨은 1672년 피에르 세네트(Pierre Seignette)에 의해 발견되었습니다.
물리적 성질:
- 화학식: KNaC4H4O6 · 4 H2O
- CAS 번호: [6381-59-5]
- 몰질량: 282.23 g/mol
- 밀도: 1.79 g/cm³
- 녹는점: 70–80 °C (220 °C에서 분해)
- 용해도: 0 °C 물 100mL당 26g, 26 °C 물 100mL당 66g
타르타르산 나트륨 칼륨 생산의 시작 물질은 최소 68%의 타르타르산 함량을 가진 주석입니다. 이 용액을 물로 희석하고, 뜨거운 수산화나트륨으로 중화하며, 활성탄으로 탈색한 후 여과합니다. 여과액은 증발에 의해 농축된 후 냉각 결정화되어 고체 염을 생성하며, 이를 포장 전에 분리, 세척, 건조 및 체질합니다. 상업적 입자 크기는 2000 μm에서 250 μm 미만(분말)까지 다양합니다.
5.2. 주석산 수소 칼륨
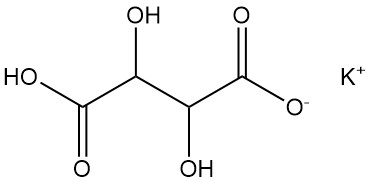
주석산 수소 칼륨(Potassium bitartrate)은 흔히 크림 오브 타르타르(cream of tartar)로 알려져 있습니다.
물리적 성질:
- 화학식: KHC4H4O6
- CAS 번호: [868-14-4]
- 밀도: 1.96 g/cm³
- 용해도: 20 °C 물 100mL당 0.57g, 100 °C 물 100mL당 6.1g
이는 주로 로셸염 생산 후 남은 모액에서 얻어집니다. 주석산 수소 칼륨은 탈색, 정제, 여과 과정을 거치며 염산이나 황산으로 산성화되어 침전됩니다. 이후 원심 분리, 건조, 분쇄 과정을 거쳐 미세 분말로 포장됩니다.
5.3. 안티모닐타르타르산 칼륨
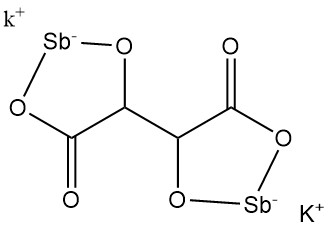
토제(Tartar emetic)로 불리는 안티모닐타르타르산 칼륨은 1631년 아드리안 드 민시히트(Adrien de Mynsicht)에 의해 발견되었습니다.
물리적 성질:
- 화학식: KSbC4H2O6 · 1.5 H2O
- CAS 번호: [28300-74-5]
- 몰질량: 333.93 g/mol
- 밀도: 2.61 g/cm³
- 용해도: 25 °C 물 100mL당 8.7g, 100 °C 물 100mL당 35.7g
안티모닐타르타르산 칼륨은 물 속에서 산화안티몬과 주석산 수소 칼륨의 반응에 의해 생성되며, 잔류 용액의 농축 및 결정화 과정이 뒤따릅니다. 여과 후 결정은 건조되고 분쇄됩니다.
5.4. 메타타르타르산
메타타르타르산은 타르타르산을 170-180 °C로 가열하여 생산합니다. 이 전환은 타르타르산 분자 내의 내부 에스테르화를 포함하여 다소 중합된 생성물을 생성합니다. 메타타르타르산은 타르타르산 염의 침전을 억제하는 탁월한 성질을 가지고 있습니다.
6. 타르타르산의 용도
L(+)-타르타르산과 그 유도체는 식품, 제약, 포도 재배 등 다양한 산업 분야에서 사용됩니다.
L(+)-타르타르산(E 334)의 용도는 다음과 같습니다:
- 와인 머스트(musts), 사탕, 젤리, 잼, 과일 넥타, 아이스크림, 젤라틴 및 페이스트의 산성화제로 사용되어 풍미를 향상시킵니다.
- 과일, 채소 또는 생선의 보존 시 상승적 항산화제로 사용되어 pH, 색상, 맛 및 영양가를 안정화합니다.
- 지방 및 오일의 항산화제로 사용됩니다.
- 탄산 음료의 제조에 사용됩니다.
- 활성 제약 성분의 부형제 또는 운반체로 사용되어 염기성을 교정하는 데 도움을 줍니다.
- 안정성과 높은 용해도로 인해 발포성 정제 및 분말의 산성화제로 사용됩니다.
- 시멘트 산업, 특히 회반죽 및 석고의 지연제로 사용됩니다.
- 금속의 연마 및 세척에 사용됩니다.
주석산 수소 칼륨(E 336)은 와인에서 타르타르산 염의 침전을 가속화하는 데 사용되며, 화학 효모의 생산 및 일부 약물 제제의 완하제로 사용됩니다.
세네트염(E 337)은 전착 공정에서 증착 및 수율을 개선하기 위해 사용되며, 전자 공학 및 압전기 분야, 거울의 은도금 시 환원제, 그리고 펠링 용액(Fehling’s solution)의 구성 성분으로 사용됩니다. 또한 담배 종이 생산의 연소 조절제, 일부 의약품의 완하제, 섬유 및 가죽 산업의 매염제로도 사용됩니다.
안티모닐타르타르산 칼륨은 소량으로 기침 시럽의 거담제로 사용되며 일부 열대 질병 치료에 도움을 줍니다.
메타타르타르산은 테이블 와인의 타르타르산염 결정화를 억제하는 데 사용됩니다.
지방산 모노글리세리드 및 디글리세리드의 타르타르산 에스테르는 제빵 산업에서 유화제로 사용됩니다.
7. 타르타르산의 독성
구연산(시트르산)과 달리 타르타르산은 인체의 크렙스 회로(에너지 생산 경로)에 직접 관여하지 않습니다.
천연 형태인 L(+)-타르타르산은 과일과 와인에서 발견됩니다. 경구 섭취 후 약 20%는 소변을 통해 배출되는 반면, 상당 부분은 장내 미생물에 의해 박테리아 분해를 거칩니다. 대변에서는 흔적이 발견되지 않습니다.
흡수된 타르타르산은 혈류에서 빠르게 제거되어 신장을 통해 배설되거나 다양한 조직에서 대사됩니다.
쥐를 대상으로 한 L(+)-타르타르산 나트륨의 장기 연구에서는 독성이나 발암성의 징후가 발견되지 않았습니다. 또한 체중 kg당 3g의 일일 용량에서 신장 기능이나 병리학에 부정적인 영향이 관찰되지 않았습니다.
라세미(DL)-타르타르산은 연구가 덜 되었으나, 천연 L(+) 이성질체와는 다르게 행동한다는 연구 결과가 있습니다.
DL-타르타르산은 혈류에서 더 느린 속도로 제거되며 신장에 더 오랜 기간 축적되어 잠재적으로 이러한 장기의 무게 증가를 유발할 수 있습니다. 이러한 신독성 효과로 인해 DL형은 식품이나 의약품 사용이 승인되지 않았습니다.
참고 문헌
타르타르산; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a26_163
타르타르산; Van Nostrand’s Encyclopedia of Chemistry. – https://onlinelibrary.wiley.com/doi/full/10.1002/0471740039.vec2453
과일의 유기산. https://onlinelibrary.wiley.com/doi/abs/10.1002/9781119431077.ch8
타르타르산. https://www.sciencedirect.com/science/article/abs/pii/B9780128190968000197