질산암모늄: 성질, 생산 및 용도
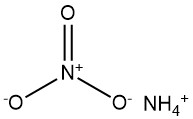
질산암모늄(NH4NO3)은 암모늄 이온(NH4+)과 질산 이온(NO3–)으로 구성된 화학 화합물입니다. 이는 무색의 결정성 물질로 농업, 산업 및 폭약 등 다양한 분야에서 널리 사용됩니다.
질산암모늄은 매우 중요한 화학 화합물입니다. 주요 생산 방식은 질산과 암모니아의 반응을 통해 이루어지며, 주로 고품질 비료의 원료로 사용됩니다. 직접 시비용 비료로서 이 화합물은 전 세계 질소 비료 소비량의 약 24%를 차지하고 있습니다.
질산암모늄은 다양한 혼합 비료 및 복합 비료 배합의 필수 성분이며, 전 세계 인구의 영양 요구를 충족시키는 데 중요한 역할을 합니다.
농업적 용도 외에도 질산암모늄은 강력한 산화제로 사용되며, 수많은 폭약 조성물에서 핵심적인 부분으로 활용됩니다.
목차
1. 질산암모늄의 물리적 및 화학적 성질
분자량이 80.05 g/mol인 질산암모늄은 무색의 염 형태로 나타납니다. 20 °C에서의 밀도는 1.725 g/cm³이며, 0 °C에서 31 °C 사이의 온도 범위에서 1.70 J/g·K의 비열 용량을 가집니다.
녹는점은 169.6-170 °C입니다. 암모니아와 질산으로부터 질산암모늄을 합성하는 과정은 다음과 같은 반응식에서 알 수 있듯이 강력한 발열 반응의 특성을 보입니다.
NH3 + HNO3 → NH4NO3 ΔH = -146 kJ/mol
32.3 °C에서 발생하는 상전이는 질산암모늄 함유 비료의 저장에 중대한 영향을 미칩니다. 이 전이 온도에 반복적으로 노출되면 밀도 차이로 인해 비료 알갱이가 변질되고 결국 부서지는 결과를 초래할 수 있습니다.
질산암모늄은 물에 매우 잘 녹으며 흡습성을 나타냅니다. 따라서 운송 및 저장 중에 수분 흡수를 방지하기 위한 주의 조치가 필수적입니다.
질산암모늄이 물에 녹을 때는 열을 흡수하므로, 염화나트륨 및 얼음과 함께 사용하는 한냉제(freezing mixtures)로 유용하게 쓰입니다.
질산암모늄은 다양한 비수용성 용매에도 용해됩니다. 액체 NH3는 이 염을 녹이는 용매 역할을 하며 NH3를 쉽게 흡수하여 ‘다이버 액체(Divers liquid)’로 알려진 용액을 생성합니다.
중량 기준으로 50~70% 농도의 질산암모늄 수용액은 NH3를 격렬하게 흡수하며 기체에서 NH3를 제거하는 세정제로 사용됩니다. 이 용액들은 과인산염의 암모니아화 공정에도 활용됩니다.
메탄올에서 질산암모늄은 30 °C에서 약 20%, 60 °C에서 약 40% 농도의 용액을 형성합니다. 에탄올에서의 용해도는 20 °C에서 약 4%이며, 아세톤에서는 용해도가 더 낮습니다. 에테르에는 녹지 않습니다.
강력한 산화제인 질산암모늄은 표준 온도 및 압력 조건에서 안정적입니다. 그러나 170 °C 이상으로 가열하면 기체로 분해됩니다. 이 분해 반응은 소량의 염소나 유리산(free acid)에 의해 가속화됩니다.
2. 질산암모늄의 생산
질산암모늄은 암모니아와 질산의 반응으로 생산됩니다. 또한 질소-인(NP) 및 질소-인-칼륨(NPK) 비료의 제조 과정에서도 생성됩니다.
이러한 형성은 인광석을 질산으로 분해할 때 발생하며, 그 결과 생성된 염이 비료의 성분이 됩니다.
유럽 지역에서는 질산칼슘, NH3, CO2의 반응을 통해 NH4NO3를 생산하기도 합니다.
2.1. 암모니아와 질산으로부터의 생산
질산암모늄은 기체 암모니아와 질산 사이의 반응으로 형성되며, NH4NO3 1몰당 100~115 J의 열 방출이 특징입니다. 다양한 생산 공정에서 이 발열 에너지는 수분을 부분적 또는 완전히 증발시키는 데 활용됩니다.
압력 조건과 사용되는 질산의 농도에 따라 95 – 97%의 질산암모늄 용액을 얻는 것이 가능합니다.
중화 과정에서는 국부적인 과열, 질소 손실 및 질산암모늄의 분해를 방지하기 위해 반응기 내에서 반응물을 신속하고 철저하게 혼합하는 것이 매우 중요합니다.
전통적인 설비들은 Uhde 공정이나 SBA(Société Belge de l’Azote) 공정과 같은 방식을 사용하는데, 이들은 반응 온도가 낮고 부식에 대한 민감도가 낮은 것이 특징입니다.
반응열을 최적으로 이용하는 것은 가압 중화 방식을 통해 달성됩니다.
UCB 공정(그림 1)은 가압 반응기 내부에 열교환기를 갖추고 있어 반응열의 일부를 증기 생산에 사용합니다. 예열된 암모니아와 52 – 63% 농도의 HNO3가 약 0.45 MPa(4.5 bar)의 압력과 170 – 180 °C의 온도로 작동하는 반응기 하부로 주입됩니다.
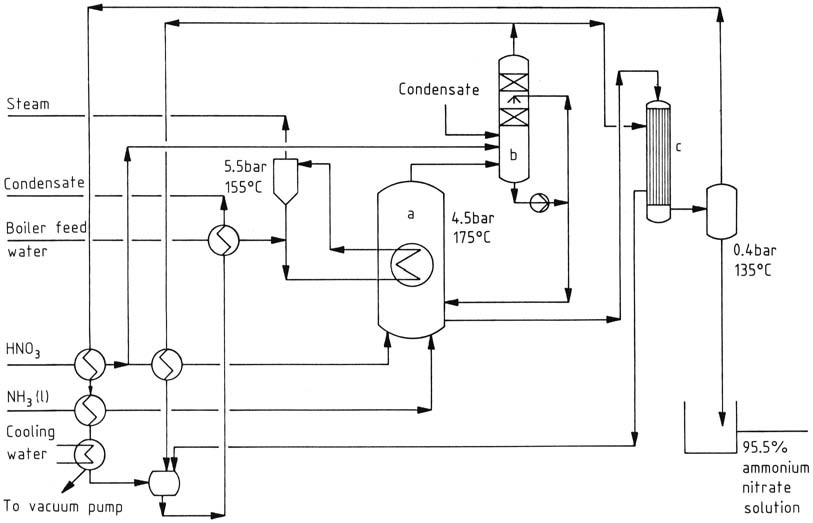
그 결과 생성된 75 – 80% NH4NO3 용액은 강하막식 증발기(falling film evaporator)에 의해 95%까지 농축됩니다. 여기서 반응열은 질산 내의 수분을 증발시켜 공정 증기를 생성하는 데 기여합니다.
이 공정 증기는 보일러 급수와 질산을 예열하고 강하막식 증발기를 가동하는 데 사용됩니다. 또한 반응열의 일부는 순수 증기를 생성하여 다른 용도로 스팀 풀(steam pool)에 공급될 수 있습니다.
pH 범위를 3 – 5로 유지함으로써 공정 증기로의 질소 손실을 완화하며, 과도한 공정 증기 축적을 방지하기 위해 운전 조건을 정밀하게 조정합니다.
또 다른 가압 공정은 Stamicarbon 공정(그림 2)으로, 분리기로 연결된 루프 반응기를 사용합니다. 반응 용액의 순환은 시스템 내에서 생성된 열을 통해 유지됩니다.
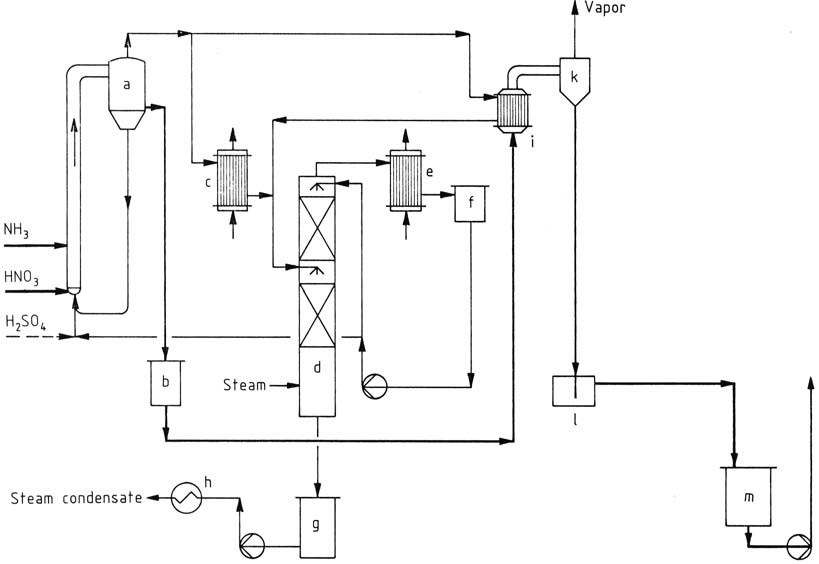
a) 중화기; b) 중간 탱크; c) 잉여 증기 응축기; d) 암모니아 스크러버; e) 응축기; f) 희석 암모니아 용액 탱크; g) 응축수 탱크; h) 냉각기; i) 증발기; k) 분리기; l) 밀봉 용기; m) 95% 질산암모늄 용액 저장 탱크
루프의 하단에는 예열된 질산(60 wt %), 암모니아 및 소량의 황산이 도입됩니다. 0.4 MPa(4 bar)와 178 °C에서 작동하는 이 반응기는 78% 농도의 질산암모늄 용액을 생성합니다.
분리기 상단에서 제거된 증기는 진공 증발기에서 NH4NO3 용액을 95%까지 농축하는 데 사용됩니다. 또한 과잉 증기는 응축되고, 회수된 암모니아는 반응기로 재순환됩니다.
98 – 99.5%까지의 추가 농축은 신선한 증기를 사용하는 후속 증발기에서 수행되며, 질산암모늄 용액의 온도는 중화 및 증발 과정 내내 180 °C 미만으로 세심하게 유지됩니다.
NSM/Norsk Hydro 가압 공정(그림 3)은 예열된 암모니아와 질산을 사용하는 것이 특징입니다. 0.4~0.5 MPa(약 4.5 bar)의 압력과 170~180 °C의 온도에서 작동하며, 70 – 80% 농도의 용액을 얻습니다.
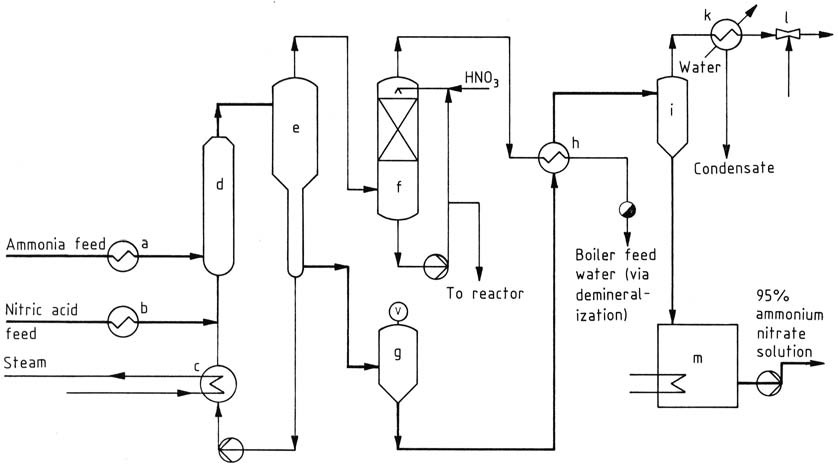
a) 암모니아 증발기/과열기; b) 질산 예열기; c) 보일러; d) 반응기; e) 반응기 분리기; f) 스크러버; g) 플래시탱크; h) 증발기; i) 분리기; k) 응축기; l) 이젝터; m) 탱크
열 사이폰 효과와 결합된 강제 순환 방식이 반응기를 통해 용액을 구동합니다. 반응열의 일부는 외부 보일러 내에서 순수 증기를 생성하는 데 기여하고, 일부는 반응기 내의 물을 기화시켜 질산암모늄 용액을 95%로 농축하는 데 필요한 공정 증기를 생성합니다.
암모니아 손실 최소화는 순환하는 질산암모늄 용액에 첨가된 질산으로 공정 증기를 세척함으로써 달성됩니다. 99.5%까지의 최종 농축 단계는 특수 진공 증발기 내에서 증기를 통해 이루어집니다.
미국에서 사용되는 Stengel 공정은 무수 질산암모늄의 직접 생산을 가능하게 합니다. 예열된 암모니아와 약 58%의 질산이 0.35 MPa(3.5 bar)와 240 °C에서 작동하는 충전식 수직 관형 반응기에 주입됩니다.
원심 분리기 내에서 진공으로 팽창한 후, NH4NO3와 증기의 혼합물은 뜨거운 공기로 스트리핑 과정을 거쳐 99.8% 농도의 NH4NO3 융액(melt)으로 배출됩니다.
이 융액은 이후 냉각된 스틸 벨트 위에서 고체화되며, 분쇄 또는 과립화 공정을 통해 추가 가공됩니다. 증기 제거는 이 공정의 상단에서 발생합니다.
이 모든 공정에서 원하는 pH 범위를 세심하게 유지하는 것이 중요합니다. 반응 온도가 170 °C 미만인 경우, 질소 손실을 최소화하기 위해 pH를 2.4에서 4 사이로 유지합니다.
온도가 더 높고 분해 가능성이 증가하는 가압 중화 장치에서는 4.6에서 5.4의 약간 높은 pH 범위가 필요합니다.
2.2. 질산칼슘 사수화물의 전환
Odda 공정에서는 인광석을 질산으로 침출하여 니트로인산 비료를 생산하는데, 이 과정에서 질산칼슘 사수화물(Ca(NO3)2 · 4 H2O)이 부산물로 상당량 형성됩니다.
니트로인산염의 생산은 증가하고 있는 반면, 질산칼슘에 대한 수요는 감소하고 있습니다. 수년 전 도입된 방법에는 질산칼슘 사수화물을 암모니아 및 이산화탄소로 처리하여 다음과 같은 화학 반응을 통해 질산암모늄과 탄산칼슘을 형성하는 공정이 포함됩니다.
Ca(NO3)2 · 4 H2O + 2 NH3 + CO2 → 2 NH4NO3 + CaCO3 + 3 H2O ΔH = -126 kJ/mol
이 반응 동안 방출되는 열은 관련된 모든 수분을 완전히 증발시키기에 충분할 만큼 큽니다. 그러나 고온에서 발생하는 불리한 평형 조건으로 인해 이 절차에 직접 접근하는 것은 불가능합니다.
BASF 공정은 Ca(NO3)2와 (NH4)2CO3가 관여하는 반응에서 제열 과정을 분리합니다. 이 방법에서는 NH3와 CO2를 순환하는 NH4NO3 용액 내에 용해시키고, 발생한 열을 효율적으로 관리합니다.
동시에 질산칼슘 사수화물은 별도의 NH4NO3 용액에 용해됩니다. 그 후 이 두 용액을 결합하여 약 50 °C에서 반응시키면 열 발생이 최소화됩니다.
침전된 방해석(calcite) 알갱이의 크기는 반응물이 도입되는 방식에 따라 조절할 수 있습니다. 반응 후 약 65%의 농도를 가진 NH4NO3 용액은 벨트 필터를 사용하여 CaCO3로부터 분리되며, 이후 증발에 의해 농축됩니다.
잔류 CaCO3에는 여전히 미량의 암모늄 화합물과 인산염이 포함되어 있을 수 있어, 석회 질산암모늄(CAN) 생산에 사용하기에 특히 적합합니다. 전환 전에 질산칼슘을 미리 준비함으로써 비교적 순수한 CaCO3 생성이 가능해집니다.
질산칼슘을 직접 전환하면서 동시에 반응 중에 방출되는 열을 처리하는 독특한 접근 방식으로, Hoechst는 특수 수직 반응기를 개발했습니다.
이 반응기 설계에서는 기체 CO2가 하단 섹션에서 도입되며, 암모니아는 세 개의 별도 구역 내에서 주입되고 각 구역은 수순환에 의해 능동적으로 냉각됩니다.
3. 질산암모늄의 용도
질산암모늄(AN)은 주로 비료로 사용되며, 순수 형태, 희석 형태 또는 복합 비료의 성분으로 쓰입니다. 미국, 동유럽 및 프랑스와 같은 지역에서 중요한 요소(urea)와 함께 액체 비료 형태로도 발견됩니다.
미국, 영국 및 프랑스의 농업 부문에서는 질소 함량이 33.5% 이상인 질산암모늄이 널리 사용됩니다. 미국은 또한 32.5% N을 함유한 비료를 활용합니다.
독일 연방 공화국에서는 질산암모늄을 석회, 돌로마이트, 황산암모늄 또는 가리와 혼합하여 사용하며, 특히 석회 질산암모늄(CAN)에 중점을 둡니다.
3.1. 석회 질산암모늄 (Calcium Ammonium Nitrate)
질산암모늄 용액(약 95 – 97%)은 분쇄된 석회석에서 유래하거나 질산칼슘의 전환을 통해 얻은 미세 탄산칼슘과 결합하여 알갱이로 변환될 수 있습니다.
후속 단계에는 건조, 냉각, 선별 및 고결 방지 처리가 포함됩니다. 질산암모늄과 석회석 사이의 반응으로 인해 발생하는 흡습성 질산칼슘의 형성은 (NH4)2SO4, MgSO4, FeSO4와 같은 첨가제를 넣어 방지합니다.
독일에서 석회 질산암모늄의 질소 함량은 초기 20.5% N에서 현재 27.5% N 수준으로 점진적으로 증가했으며, 이는 유럽 경제 공동체 규정의 상한선인 28% N을 준수하고 있습니다.
3.2. 황질산암모늄 (Ammonium Sulfate Nitrate)
이 혼합 황산-질산 비료는 약 95% 질산암모늄 용액에 황산암모늄을 첨가하거나, HNO3-H2SO4 혼합물을 암모니아로 중화하여 만듭니다.
약간 흡습성을 띠는 과립 제품은 복염인 2 NH4NO3 · (NH4)2SO4와 소량의 황산암모늄 혼합물이며, 질산암모늄 함량이 45% 미만인 경우 26% N의 질소 함량을 가집니다.
시간이 지남에 따라 이 혼합물은 추가 반응으로 인해 굳어지는 경향이 있습니다. 이러한 경화 현상은 Mg, Fe 또는 Al의 염을 도입하여 방지할 수 있습니다.
3.3. 칼륨 질산암모늄 (Potassium Ammonium Nitrate)
칼륨 질산암모늄은 황질산암모늄과 유사한 방식으로 합성되며, 칼륨염(염화물 또는 황산물)을 첨가하여 20–0–20 (N–P2O5–K2O)과 같은 비료를 생산합니다.
3.4. 니트로마그네시아 (Nitromagnesia)
니트로마그네시아는 질산암모늄, 황산암모늄, 그리고 돌로마이트, 탄산마그네슘 또는 황산마그네슘과 같은 마그네슘 화합물에서 유래한 비료입니다. 전형적인 배합 중 하나는 약 20% N, 8% MgO 및 보통 0.2% Cu를 함유할 수 있습니다.
3.5. 기타 응용 분야
질산암모늄은 폭발 온도가 비교적 낮기 때문에 광업에서 사용되는 안전 폭약의 핵심 성분입니다. NaCl과 결합하면 폭발 온도를 낮추어 가연성 가스(fire damp)의 점화 위험을 완화합니다.
어떤 경우에는 NaNO3 + NH4Cl → NH4NO3 + NaCl과 같은 상보적 염 쌍을 기반으로 안전 폭약이 조제되기도 합니다.
채광(암석 폭약)과 같이 더 큰 폭발력이 필요한 용도에는 약 6%의 디젤유를 포함하는 다공성 프릴(prilled) 질산암모늄이 사용됩니다.
소량의 질산암모늄은 아산화질소(일산화이질소) 생산에 관여합니다. 이 용도의 염은 유기 물질, 철, 염화물 및 황산염이 없어야 하며 99.5% NH4NO3의 고순도여야 합니다.
4. 안전성
질산암모늄은 일반적인 상황에서는 안정적이지만, 고온에서는 다음과 같은 뚜렷한 분해 반응을 일으킵니다.
1. 169 °C 이상에서의 흡열 해리 및 pH 감소:
NH4NO3 → HNO3 + NH3 ΔH = +175 kJ/mol
2. 200 °C에서 주의 깊게 가열할 때 발생하는 N2O의 발열 제거:
NH4NO3 → N2O + 2 H2O ΔH = -37 kJ/mol
3. 230 °C 이상에서의 N2 및 NO2 발열 제거:
4 NH4NO3 → 3 N2 + 2 NO2 + 8 H2O ΔH = -102 kJ/mol
4. 폭발(detonation)로 이어지는 질소 및 산소의 발열 제거:
NH4NO3 → N2 + 1/2 O2 + 2 H2O ΔH = -118.5 kJ/mol
순수한 질산암모늄, 농축된 뜨거운 용액, 특정 혼합물 및 비안정화된 비료 형태는 모두 충격파에 의해 폭발할 수 있는 폭약이 될 수 있습니다. 방출되는 열은 헥소겐(hexogen)과 같은 화합물에 비해 상대적으로 적지만, 상당한 양을 저장하는 것은 심각한 위험을 초래합니다. 수소 이온, 염화물 및 중금속과 같은 요인들이 분해를 촉매할 수 있습니다.
오염되거나 압착된 질산암모늄을 가열하는 것은 특히 위험합니다. 1947년 브레스트와 텍사스 시티 참사(왁스로 코팅된 비료용 질산암모늄이 화재로 폭발한 사건) 이후, 현재 규정은 가연성 물질을 0.2% 또는 0.4%로 제한하고 있습니다.
독일의 작업 물질법(Working Materials Act)은 질산암모늄의 저장, 적재 및 운송에 관한 규약을 개설하고 있습니다. 예를 들어, 폭발 가능성이 있는 질산암모늄의 저장은 특수 설비를 갖춘 시설 내의 소량으로 제한됩니다.
다른 유럽 국가들에서도 유사한 규칙이 적용되는 반면, 미국, 프랑스, 노르웨이 및 영국은 특정 조건 하에서 비교적 대량 저장을 허용합니다.
독일에서는 비료용 질산암모늄(석회 질산암모늄)에 석회석 가루나 돌로마이트 같은 불활성 물질을 첨가합니다. 최대 80%의 질산암모늄, 최대 0.4%의 가연성 성분, 그리고 최소 18%의 마그네슘 또는 탄산칼슘을 함유한 이러한 비료들은 비폭발성으로 간주됩니다.
안전 수칙은 다음과 같습니다.
- 저장 중 질산암모늄을 포함한 고체화된 제품에 충격을 가하지 마십시오.
- 질산암모늄 제품은 산화 가능성이 있거나 가연성 물질로부터 멀리 떨어진 곳에 보관하십시오.
- 질산암모늄을 가열할 때는 소량을 사용하고 촉매 접촉을 피하십시오.
참고 문헌
Ammonium Compounds; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a02_243