염화칼슘: 성질, 생산 및 용도

염화칼슘(CaCl2)은 흡습성이 강한 염으로, 물에 대한 용해도가 높고 수화물을 형성하는 능력이 있는 무색, 무취의 결정성 고체입니다.
염화칼슘은 다른 염류와 함께 바닷물과 광천수 속에 소량 존재합니다.
그 발견은 15세기로 거슬러 올라가지만, 18세기 후반에 이르러서야 비로소 상당한 주목을 받거나 연구되기 시작했습니다.
1800년대 중반 솔베이(Solvay) 암모니아-소다 공정이 개발되기 전까지는 상업적으로 생산되지 않았기 때문에, 초기 연구는 주로 실험실에서 조제된 샘플을 사용하여 수행되었습니다.
목차
1. 염화칼슘의 성질
염화칼슘은 넓은 온도 범위에 걸쳐 물에 대해 높은 용해도를 보이며, 175 °C 이상의 온도에서는 약 75%의 최대 용해도가 관찰됩니다.
가용성 무기 칼슘의 공급원으로서, 염화칼슘은 탄산염, 불화물, 황산염과 반응하여 불용성 또는 난용성 염을 형성합니다.
또한 염화칼슘은 암모니아와 CaCl2·8 NH3와 같은 수용성 화합물을 형성하며, 알코올과는 CaCl2·C2H5OH와 같은 화합물을 형성합니다.
나아가, 텅스텐산나트륨(Na2WO4)과 반응하여 합성 회중석(scheelite)으로 흔히 알려진 텅스텐산칼슘(CaWO4)을 생성합니다.
2. 염화칼슘의 생산
염화칼슘은 다양한 공정을 통해 상업적으로 생산되는 화합물입니다.
천연 염수의 정제와 합성 소다회 생산 과정에서 회수되는 염화칼슘은 여전히 가장 일반적인 생산 방법이며, 전체 생산량의 90% 이상을 차지합니다.
이러한 공정 중 하나는 천연 염수를 정제하는 것입니다. 캘리포니아와 미시간의 수원에서 얻은 천연 염수에는 칼슘, 마그네슘, 나트륨의 염화물 혼합물이 포함되어 있습니다.
이 염수에서 염화칼슘을 얻으려면 먼저 석회를 사용하여 수산화마그네슘, Mg(OH)2을 침전시켜 마그네슘을 제거해야 합니다. 남은 용액은 여과 및 농축 과정을 거치며, 이 과정에서 염화나트륨은 염화칼슘 용액에 대한 낮은 용해도 때문에 침전되어 분리됩니다.
염화칼슘을 생산하는 또 다른 방법은 염산과 탄산칼슘의 반응을 이용하는 것입니다. 이 반응을 통해 염화칼슘, 이산화탄소, 물이 생성됩니다.
염화칼슘 생산의 세 번째 방법은 솔베이(합성) 소다회 생산 공정에서 수산화칼슘과 염화암모늄을 반응시키는 것입니다.
이 공정에서 암모니아는 염화나트륨과 탄산칼슘의 반응을 돕는 촉매 역할을 합니다. 반응 자체는 복잡하지만 최종 결과물로 염화칼슘이 생성됩니다:
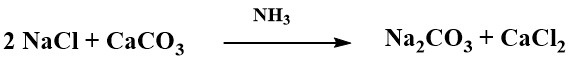
천연 염수 정제 및 솔베이 공정으로 얻은 염화칼슘 용액은 농도가 낮습니다.
증발을 통한 농축 후, 용액의 일부는 30-45% 염화칼슘 제품으로 판매됩니다. 또 다른 일부는 고형분 약 75%까지 추가 농축되며, 이는 이수화물(CaCl2·2 H2O) 상태에 해당합니다.
이 물질은 건조 및 플레이크(flake)화 과정을 거쳐 상업용 염화칼슘 이수화물(77 – 82% CaCl2) 및 무수(94 – 97% CaCl2) 제품으로 생산됩니다.
또는 플레이크 제조 장치 대신 응집 공정을 사용하여 무수 펠릿(pellet) 형태로 제조할 수도 있습니다.
3. 염화칼슘의 용도
염화칼슘의 다재다능함은 수분 흡수 및 유지 능력, 높은 용해도, 높은 용해열, 용액의 어는점 내림과 같은 독특한 물리적 성질의 조합과 관련이 있습니다.
염화칼슘은 제설 및 먼지 억제 능력으로 가장 널리 알려져 있습니다.
염화칼슘의 가장 큰 시장(전체 생산량의 30%)은 도로, 인도 및 주차장의 제설용입니다.
염화칼슘은 -51 °C (-60 °F)만큼 낮은 온도에서도 얼음을 녹일 수 있습니다. 수분에 노출될 때 열을 방출하기 때문에 얼음이 빠르게 녹으며, 보통 살포 후 15 – 30분 이내에 효과가 나타납니다.
염화칼슘은 암염(염화나트륨)의 효과를 강화하고 지속시키기 위해 암염과 병용되기도 합니다.
먼지 제어(Dust Control)는 염화칼슘 생산량의 약 25%를 차지합니다. 흡습성 및 조해성 덕분에 이 용도에 매우 적합합니다.
염화칼슘은 공기 중의 수분을 흡수하여 용액을 형성하고, 이 용액이 먼지 입자를 코팅하고 서로 결합시켜 먼지 발생을 크게 줄입니다.
염화칼슘 용액은 증기압이 낮아 증발이 느리기 때문에 도로 표면을 다지는 데 유용합니다.
염화칼슘은 시멘트 및 콘크리트 산업에서도 사용됩니다. 1 – 2%의 염화칼슘을 첨가하면 콘크리트의 경화 시간이 단축되어 조기 강도 발현이 가능해집니다.
염화칼슘을 콘크리트 타설 시 부동액으로 간주해서는 안 되지만, 21 °C (70 °F) 미만의 온도에서 타설되는 콘크리트 배합에 염화칼슘을 첨가하면 낮은 온도로 인한 경화 지연 효과를 상당 부분 상쇄할 수 있습니다.
염화칼슘 용액은 어는점이 낮아 식품 가공에서 열전달 매체로 널리 사용됩니다. 염화칼슘 브린(brine)은 냉각된 공기나 염화나트륨 브린에 비해 열전달 속도를 크게 높여줍니다. 브린과 다양한 식품 성형틀 사이의 접촉 시간이 단축되어 생산율이 높아집니다.
염화칼슘은 식품 산업에서 과일과 채소의 단단함을 높이고 가공 중 부패를 방지하기 위해서도 사용됩니다.
석유 및 석유 화학 산업에서 염화칼슘은 탄화수소의 건조제로 사용됩니다. 또한 유정 시추 시 시추 유체(drilling fluids), 패커 유체(packer fluids), 완결 유체(completion fluids) 및 수리 유체(workover fluids)에도 사용됩니다.
염화칼슘의 다른 용도로는 접착제의 보습제 및 겔화 온도 저하제, 동물 사료의 칼슘 공급원, 폐수 처리에서의 불화물 침출, 오일 에멀전 분해 및 플록(floc)의 밀도 강화 등이 있습니다.
참고 문헌
Calcium Chloride; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a04_547