ジクロロ酢酸:性質、製法、および応用
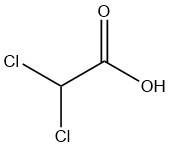
ジクロロ酢酸とは何か?
ジクロロ酢酸は、化学式 CHCl2COOH で表される酢酸の誘導体です。非常に腐食性の高い液体であり、粘膜を刺激する酸性蒸気を放出します。
ジクロロ酢酸は水と完全に混和し、アルコール、ケトン、炭化水素、塩素化炭化水素などのさまざまな有機溶媒に容易に溶解します。
目次
1. ジクロロ酢酸の物理的性質
2,2-ジクロロエタン酸としても知られるジクロロ酢酸の物理的性質は以下の通りです:
| 項目 | 値 / 条件 |
|---|---|
| モル質量 | 128.95 g/mol |
| 沸点 | 192 ℃ (101.3 kPa) |
| 凝固点 | 13.5 ℃ |
| 密度 | 1.564 |
| 蒸気圧 | 0.19 kPa (20 ℃) |
| 解離定数 | 5×10-2 mol/L (18 ℃) |
2. ジクロロ酢酸の化学反応
ジクロロ酢酸は、置換反応を受けやすい2つの塩素原子を持っています。
芳香族化合物と反応させるとジアリール酢酸を形成し、フェノールの存在下ではジフェノキシ酢酸が生成されます。
モノクロロ酢酸と比較すると、ジクロロ酢酸は加水分解を受けにくい性質を示します。しかし、モノクロロ酢酸の中に不純物としてジクロロ酢酸が存在すると、カルボキシメチルセルロース(CMC)やデンプンの製造過程で架橋を引き起こす可能性があります。この架橋効果は、最終製品の用途に応じて、望ましい場合もあれば望ましくない場合もあります。
3. ジクロロ酢酸の製造方法
ジクロロ酢酸を製造するための最も経済的に実行可能なアプローチは、ジクロロアセチルクロリドの加水分解です。
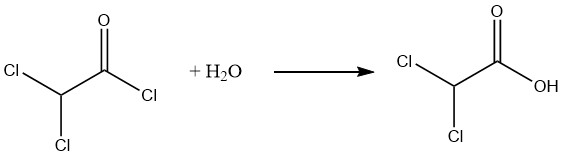
さらに、88~99%の硫酸を用いてペンタクロロエタンを加水分解するか、あるいは1,1-ジクロロアセトンを硝酸と空気で酸化することにより、純度98%のジクロロ酢酸を90%の収率で得ることができます。
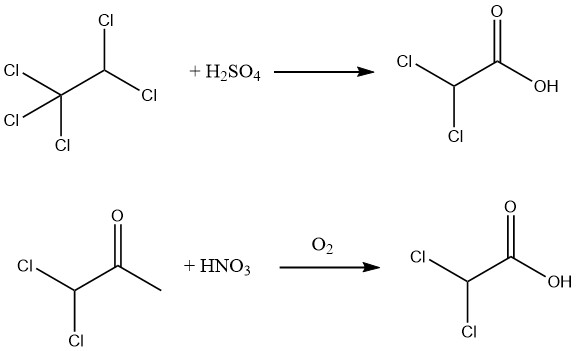
粗ジクロロ酢酸のエステル化によって容易に得られるメチルエステルを加水分解することで、極めて純度の高いジクロロ酢酸を製造することが可能です。
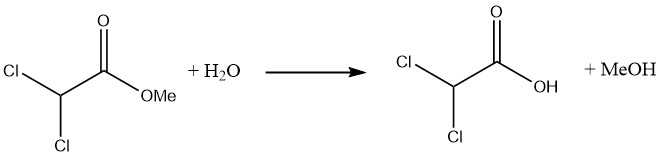
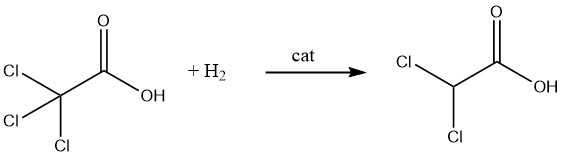
また、パラジウム触媒上でトリクロロ酢酸またはトリクロロ酢酸エチルを水素を用いて接触脱塩素化することにより、ジクロロ酢酸およびジクロロ酢酸エチルを得る方法もあります。
他のクロロ酢酸類から純粋なジクロロ酢酸を分留などの物理的手段で分離することは、特にジクロロ酢酸とトリクロロ酢酸の沸点差がわずかであるため、非常に困難であることが証明されています。
しかし、効率的な蒸留塔を用いれば、エステル混合物を満足に分留することができます。さらに、3種類のクロロ酢酸から誘導される塩の混合物を水、アルコール、または水-アルコール溶液で洗浄することにより、ジクロロ酢酸塩を優先的に溶解させ、これを酸性化することで純粋なジクロロ酢酸を得ることも可能です。
実験室レベルでは、抱水クロラールをシアン化カリウムまたはシアン化ナトリウムと反応させることでジクロロ酢酸を合成できます:
Cl3CCH(OH)2 + KCN → HCN + KCl + Cl2CHCOOH
4. ジクロロ酢酸の用途
ジクロロ酢酸は、繊維製造、特にポリエチレンテレフタレート(PET)製造時の分析測定における試験試薬として利用されています。また、ホルマリンの代替品として医薬用の消毒剤としても機能します。
さらに、ジクロロ酢酸はオリゴヌクレオチドの固相合成において、脱ブロッキング剤(脱保護剤)として重要な役割を果たします。この機能を果たすためには、クロラール(トリクロロアセトアルデヒド)を実質的に含まない高純度のジクロロ酢酸が必要となります。
有機合成において、ジクロロ酢酸(特にそのエステルの形態)は反応性の高い出発原料として機能します。グリオキシル酸、ジアルコキシ酸、ジアロキシ酸、およびスルホンアミドの製造に利用されており、極めて重要な中間体化合物となっています。
参考文献
Chloroacetic Acids; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a06_537.pub3