アクリル酸:性質、反応、製造および用途
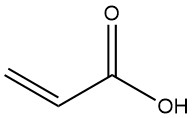
アクリル酸は、2-プロペン酸としても知られ、化学式 CH2=CHCOOH で表される最も単純な不飽和カルボン酸です。無色透明の液体で、可燃性、揮発性があり、わずかな毒性を持っています。
重合を防止するため、市販の製剤には通常、ヒドロキノンまたはそのモノメチルエーテルが添加されています。
かつて、アクリル酸の工業的製造にはアクリロニトリルの加水分解や改良レッペ法など様々な手法が用いられてきました。しかし、接触酸化技術、特にアクロレインを経由したプロペンからアクリル酸への転換技術の著しい進歩により、現在ではこれらの旧来の手法はほぼ完全に置き換わっています。
目次
1. アクリル酸の物理的性質
アクリル酸は、101.3 kPaにおいて沸点 141.0 °C、融点 13.5 °C を持つ透明無色の液体であり、固化すると針状結晶を形成します。
水、アルコール、エステル、およびその他様々な有機溶媒と高い混和性を示し、これらの物質に容易に溶解します。
その他の重要な物理的性質を以下に示します:
表1:アクリル酸の物理的性質
| 項目 | 値 |
|---|---|
| モル質量 (Mr) | 72.06 g/mol |
| 屈折率 | 1.421 |
| 密度 | 1.05 g/cm³ |
| 粘度 (25°C) | 1.15 mPa·s |
| 臨界温度 | 380 °C |
| 臨界圧力 | 5.06 MPa |
| 解離定数 (25°C) | 5.46 x 10-5 |
| pKa | 4.25 |
2. アクリル酸の化学反応
アクリル酸は、不飽和化合物と脂肪族カルボン酸の両方に特有の反応を示します。その高い反応性は、共役位にある2つの不飽和中心の存在に起因します。
カルボニル基によって分極したβ炭素原子は求電子剤として機能し、ビニル基への様々な求核剤や活性水素化合物の付加を可能にします。
さらに、炭素-炭素二重結合は、ラジカル開始付加反応、ジエンとのディールス・アルダー反応、および重合反応に関与します。
カルボキシル基に関しては、エステル化など、脂肪族酸に典型的な置換反応を受けます。
ビニル基とカルボキシル基が共同で反応する場合、特に二官能性試薬を用いると、多環式物質や複素環式物質を形成するための便利な経路となることがよくあります。
アクリル酸は容易に重合し、熱、光、過酸化物によって促進されますが、ヒドロキノンやヒドロキノンモノメチルエーテルなどの安定剤によって抑制されます。
特筆すべきは、これらのフェノール系重合禁止剤は酸素の存在下でのみ効果を発揮する点です。アクリル酸の重合プロセスは非常に強力な発熱反応であり、極めて激しく進行することがあります。
2.1. 付加反応
アクリル酸は、オレフィンによく見られる水素、ハロゲン化水素、シアン化水素などの物質と容易に付加反応を起こします:
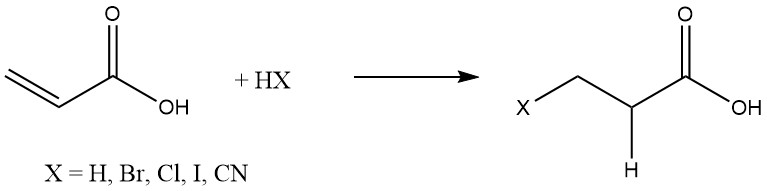
有機物質のマイケル付加は、三次アミン、四級アンモニウム塩、アルカリアルコキシドなどの塩基性触媒の存在下で進行します。
アンモニアやアミンは十分に塩基性が強いため、触媒なしで反応できます。アンモニア水溶液と炭酸アンモニウムを用いることで、1分子の NH3 付加を達成できます。
芳香族アミン、アミド、または第三級アルキル一次アミンの付加は、酸によってより効果的に促進されます。アミンはビニル基とカルボキシル基の両方を攻撃する可能性がありますが、その結果生じる生成物は分解してN-置換アミドを与えます。
塩基性条件下では、アルコール、フェノール、硫化水素、チオールも付加反応を受けます。硫化水素は、硫黄と多硫化アンモニウムまたはアミン触媒を組み合わせることで、ポリチオジプロピオン酸を与えます。一方、芳香族炭化水素の付加は、ルイス酸によってより効率的に促進されます。
付加生成物中にさらに酸性水素原子が利用可能な場合、アクリル酸の2分子目(および3分子目)が付加することがあります。これは、H2S、NH3、RNH2、およびピロールとアクリル酸の反応で見られます。
複素環式物質は、特に二官能性求核剤を用いたカルボキシル基の後続反応を通じて形成されることが多いです:
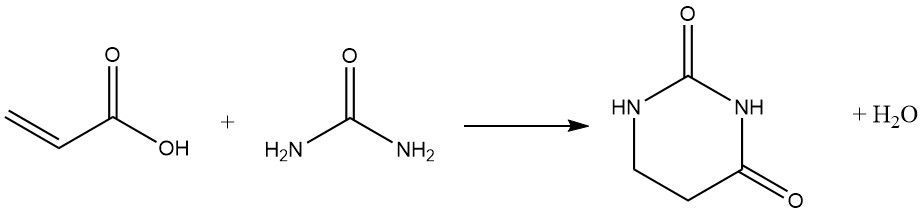
高温下や長期間の保管中、アクリル酸は二量化します:
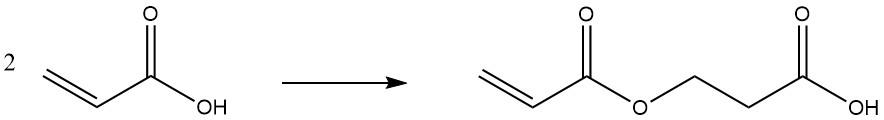
2.2. カルボキシル基の反応
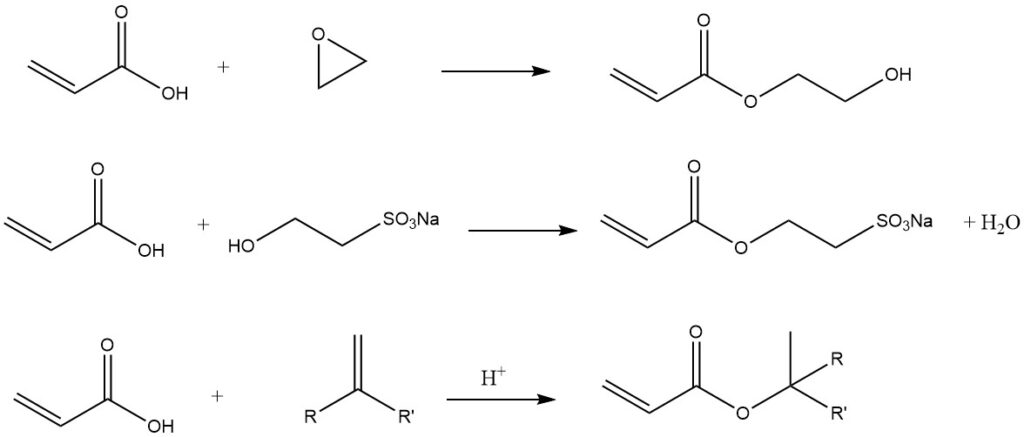
アクリル酸は容易に対応する塩に転換されるほか、無水酢酸との反応で無水アクリル酸に、あるいは塩化ベンゾイルや塩化スルフリルとの反応でアクリル酸クロリドに転換されます。アクリル酸のエステル化およびアクリル酸エステルのエステル交換反応は、経済的に極めて重要な反応です。
カルボキシル基のその他の反応例には以下のようなものがあります:
3. アクリル酸の製造
工業用アクリル酸は主にプロペンから製造されます。プロペンはアクロレイン製造の原料としても利用されます。過去にはアクリル酸とそのエステルの製造に様々なプロセスが採用されており、その一部は現在も限定的に使用されています。
1. アセチレンベースのプロセス:
アセチレンから、酸とニッケルカルボニルの存在下、常圧かつ 40°C でアクリル酸とそのエステルを合成できます:
4 C2H2 + 4 ROH + 2 HCl + Ni(CO)4 → 4 H2C=CHCOOR + NiCl2 + H2
しかし、この方法は毒性が強く腐食性の高いニッケルカルボニルの取り扱いに伴う課題のため、廃止されました。
2. 高圧レッペ法:
BASF社は、約 14 MPa、200 °C で臭化ニッケル・臭化銅(II)触媒を用い、アセチレン、CO、水からアクリル酸を製造するプロセスを採用していました。しかし、このプロセスはより経済的なプロペンの直接酸化法に置き換わりました。
3. アクリロニトリルの加水分解:
この方法は、収率が低く多量の NH4HSO4 廃棄物が発生するため、経済的に魅力がないと判断されました。旭化成を除き、多くの企業がこのプロセスを廃止しました。
4. ケテン法:
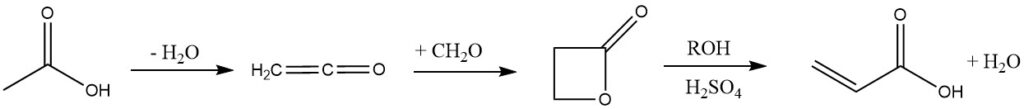
このプロセスでは、酢酸またはアセトンを熱分解してケテンを得ますが、工程数の多さと β-プロピオラクトンの毒性のため、セラニーズ社やB.F.グッドリッチ社などの企業によって廃止されました。
5. ポリプロピオラクトンの熱脱重合:
Novomer社は、中間体としてポリプロピオラクトン(PPL)を製造し、これを熱的に脱重合してアクリル酸またはアクリル酸エステルとする独自の触媒を開発しました。これにより、輸送の課題に対処し、製造の複雑さを軽減しています。
6. エチレンシアノヒドリン法:
エチレンオキシドにシアン化水素を付加してエチレンシアノヒドリンを生成し、硫酸を用いて接触脱水してアクリル酸を製造します。ユニオンカーバイド社やローム・アンド・ハース社が使用していましたが、HCNの取り扱いと NH4HSO4 廃棄物の問題で廃止されました。
7. アリルエーテルの部分酸化:
Liをドープしたメソポーラス酸化マンガンベースの触媒システムは、アセトニトリル溶媒中の穏和な条件下で、ジアリルエーテルをアクリル酸アリルへと空気部分酸化することができます。
3.1. プロペン酸化によるアクリル酸の製造
プロペンからのアクリル酸製造は、空気と水蒸気を用いた気相での不均一系接触酸化によって行われます。生成物は通常、水に吸収させた後、適切な溶媒で抽出、蒸留を経て、工業グレードの氷アクリル酸として得られます。
プロペン酸化用触媒の研究は1950年代後半に始まり、プロペンの不均一系接触気相酸化には単段法と二段法の2つの方法があります。
単段法では、収率が最高でも約 50-60% に限定され、また昇華しやすい酸化テルルが含まれるため触媒寿命が短いという欠点があります。
二段法では、各段階で最適な転換率と選択率を達成するために、異なる反応条件と触媒を使用します。第一段階の触媒はアクロレイン選択的なプロペン酸化に使用され、アクロレインとアクリル酸を合わせて 85% 以上の収率を得ます。
アクロレインからアクリル酸への酸化を行う初期の第二段階触媒は主にコバルト・モリブデン酸化物ベースで、収率は 70 mol% 未満でした。しかし、その後の研究により、モリブデンやバナジウムを含む多成分金属酸化物触媒が活性と収率を向上させることが示されました。
酸の回収と精製では、流出ガスを冷却し水で洗浄してアクリル酸水溶液を得ます。この溶液は、有機溶媒による抽出、蒸留、および蒸留中の重合を防ぐための重合禁止剤の添加を経て精製されます。得られるアクリル酸の純度は通常 99.5 wt% を超え、精製収率は約 98% です。
オリゴマー化や直接エステル化などの様々な精製方法が検討されてきましたが、エネルギー効率と製品品質の観点から、軽溶媒抽出プロセスが商業プラントにおいて依然として最も適した手法となっています。
3.2. バイオベースアクリル酸
アクリル酸製造のためのバイオベース技術は、糖などのバイオマス由来物質を発酵させて乳酸、3-ヒドロキシプロパン酸、3-ヒドロキシプロパナールなどを製造することを含みます。その後、これらの中間体が化学的転換を経てアクリル酸を与えます。
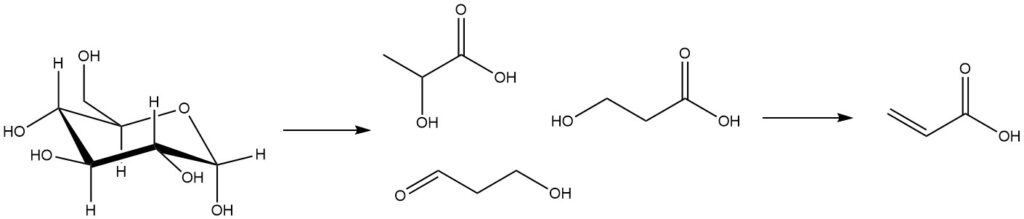
中間体である乳酸の脱水は通常、アセトキシ化を経て行われ、そこでは酢酸が共沸溶媒として使用されます。
2008年から2010年にかけて、グルコース、グリコール、乳酸、バイオマスを原料とする複数のバイオベースアクリル酸製造技術が開始されました。
Cargill/Novozymes/BASF、OPXBio/Dow、Arkema/HTE、日本触媒、Genomatica、Chorenなどの合弁企業や個別企業が、これらの技術開発に積極的に取り組んでいます。これらのアプローチの一部は2025年までに商業化されることが期待されています。
Arkema社はHTE社と協力し、アクロレインを経由してグリセロールからアクリル酸を製造する触媒の開発に取り組んでいます。日本触媒は、植物油からのバイオディーゼル製造の副産物として得られるグリセロールからアクリル酸を製造する気相プロセスを探索しています。これらのプロセスの商業化の可能性は、グリセロールの供給量と価格に依存します。
Genomatica社のアプローチは、糖を発酵させてフマル酸にし、次いでエチレンとのクロスメタセシスを行ってアクリル酸を製造するものです。この技術は特許を取得していますが、依然として克服すべき重要な技術的課題が残っています。
4. アクリル酸の用途
アクリル酸はアクリル酸エステル製造の中間体として機能します。アクリル酸エステルは、その多用途性と性能特性により、様々な産業で広く使用されています。
さらに、アクリル酸とそのナトリウム塩は、凝集剤や分散剤としての用途が拡大しています。これらの重合体、特にポリアクリル酸ナトリウム塩は、様々なプロセスにおいて凝集(粒子の塊形成)や分散(粒子の均一分布)を促進する効果的な特性を持つため、工業的重要性が高まっています。
2014年時点で、アクリル酸とそのエステルの世界生産能力は、それぞれ年間520万トン、360万トンを超えています。
中国はアクリル酸の高成長市場として台頭しており、北米と欧州の合計需要を上回っています。2002年から2014年の間に、中国のアクリル酸生産能力はほぼ4倍に拡大しました。
2014年において、アクリル酸の全消費量の50%はエステル製造の中間体として利用され、残りの50%は氷アクリル酸として処理されました。
5. 毒性および労働衛生
アクリル酸は中程度の毒性があり、腐食性が非常に高い物質です。摂取すると深刻な消化管の火傷を引き起こす可能性があり、その蒸気は目や気道を刺激します。皮膚に接触すると火傷の原因となることがあります。以下の生理学的反応データが報告されています:
- LD50:340 mg/kg(ラット、経口)
- LC50:3600 mg/m³(ラット、吸入、5 L、4時間)
- LD50:280 mg/kg(ウサギ、経皮)
アクリル酸の許容濃度(TLV)は、時間加重平均(TWA)で 10 ppm または 30 mg/m³ に設定されています。この値は、職場環境における曝露レベルを制御するための指針として機能します。
参考文献
Acrylic Acid and Derivatives; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a01_161.pub4