アニリン:性質、反応、製法、および用途
アニリン(別名:アミノベンゼン)は、化学式 C6H5NH2 で表される芳香族アミンです。甘いアミン様の臭気を持つ、無色から微黄色の可燃性液体ですが、空気や光にさらされると茶色に変色します。
アニリンの単離は19世紀初頭に遡りますが、その構造は1843年、A. W. フォン・ホフマンがニトロベンゼンの還元を通じて決定的な裏付けを与えました。
アニリンを合成する最初の工業的手法は、早くも1854年には確立されていました。過去145年間で、アニリンは化学分野における「最も不可欠なビルディングブロック100選」の一つとして確固たる地位を築いています。
アニリンは、イソシアネート、ゴム加工剤、染料・顔料、農薬、医薬品など、極めて多岐にわたる用途の中間体として欠かせない存在です。
目次
1. アニリンの物理的性質
アニリンは水にわずかに溶け、ほとんどの有機溶媒(エタノール、アセトン、ベンゼンなど)と混和します。
アニリンの主要な物理的性質は以下の通りです:
| 項目 | 値 |
|---|---|
| 分子量 | 93.13 g/mol |
| 沸点 (101.3 kPa) | 184.4 ℃ |
| 凝固点 | -6.2 ℃ |
| 引火点 (DIN 51758) | 76 ℃ |
| 発火温度 (DIN 51758) | 540 ℃ |
| 臭気閾値 | 0.5 mL/m3 |
| 液体密度 (20 ℃) | 1.022 g/cm3 |
| 溶解度 (20 ℃、対水) | 3.6 % |
| pH値 (20 ℃、アニリン 3.6 g/L溶液) | 8.8 |
2. アニリンの化学反応
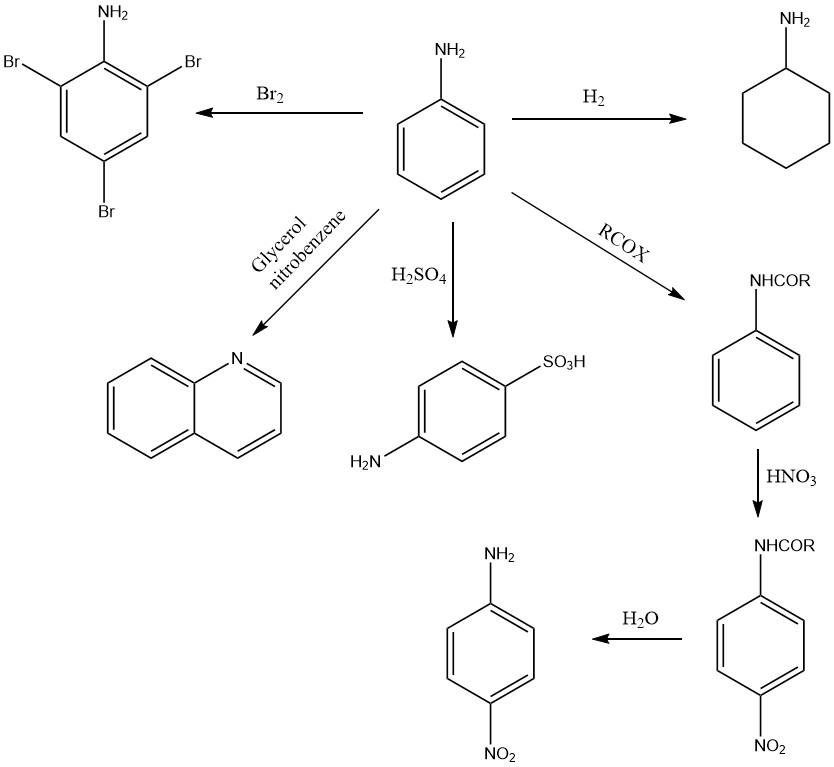
アニリンの化学的挙動は、第一級アミノ基(図1)と活性化されたベンゼン核(図2)によって決定されます。
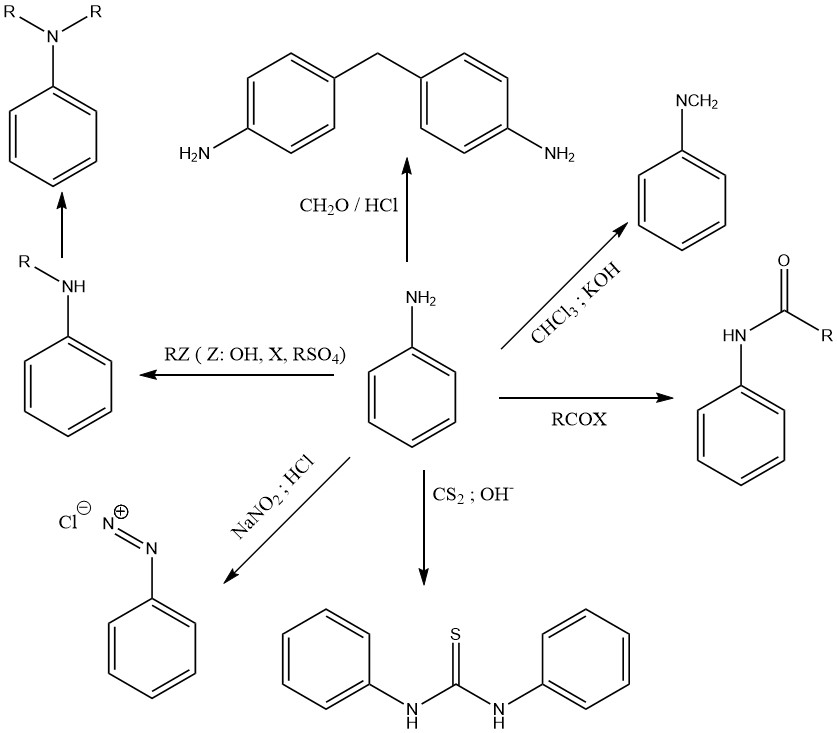
アミノ基の窒素上にある孤立電子対は、芳香族環系に部分的に非局在化しています。そのため、アニリンはシクロヘキシルアミン(pKa = 10.64)のような脂肪族アミンと比較して、弱い塩基(pKa = 4.60)としての性質しか持ちません。
それにもかかわらず、アニリンは強酸(塩酸や硫酸など)と安定した水溶性の塩を形成します。硫酸アニリンの形成は、その後の合成ステップにおいてアミノ基を酸化から保護するために利用されることがあります。
さまざまなアルキル化剤(アルコール、ハロゲン化アルキル、硫酸アルキル、オレフィンなど)は、ルイス酸触媒を用いた高温高圧下での反応により、アミノ基をアルキル化して N-アルキルアニリンおよび N,N-ジアルキルアニリンを生成します。
苛性カリ(水酸化カリウム)溶液中でアニリンとクロロホルムを反応させると、フェニルイソシアニドが生成されます。
アルカリ性のアルコール溶液中でアニリンと二硫化炭素を反応させると、N,N-ジフェニルチオ尿素が得られます。
アニリンのような第一級芳香族アミンの特徴的な反応は、亜硝酸との反応によるジアゾニウム塩の形成です。
アニリンはアルキルアルデヒドと縮合反応を起こします。最も重要な反応は、塩酸の存在下でのアニリンとホルムアルデヒドの縮合による、4,4′-メチレンジアニリン(MDA)の生成です。
アニリンは有機酸およびその誘導体と反応してアミドを形成します。
アニリンは酸化剤や反応条件に応じて、多様な酸化反応を起こします。p-ベンゾキノン(MnO2, H2SO4)のような単核生成物、アゾベンゼン(空気)のような二分子化合物、あるいはアニリンブラック(Cu または V, Na2Cr2O7 または NaClO3)のような高分子物質が形成されることがあります。
アニリンの芳香環は、触媒を用いて高温高圧下で水素化され、条件や触媒の種類に応じてシクロヘキシルアミンやジシクロヘキシルアミンを与えます。
アミノ基の存在により芳香環のオルト位とパラ位が活性化されるため、アニリンは親電子物質と容易に反応します。例えば、臭素によるアニリンの臭素化では、穏やかな条件下で 1,3,5-トリブロモアニリンが生成されます。
高温での硫酸との反応では、ほぼ排他的に 4-アミノベンゼンスルホン酸(4-スルファニル酸)が形成されます。
アニリンを(アセトアニリドの形成によってアミノ基を酸化から保護した後に)ニトロ化すると、4-ニトロ化合物が生成されます。
アニリンからは数多くの N-複素環化合物を得ることができます。例えば、ニトロベンゼン中でアニリンとグリセリンまたはアクリルアルデヒド(アクロレイン)を縮合させるスクラープ合成により、キノリンが製造されます。
3. アニリンの製造
商業的に利用されているアニリン合成プロセスの大半は、ベンゼンを出発原料としています。
ベンゼンを直接アミノ化する試みもありますが、高温高圧、および大過剰のアンモニアが必要であるため、経済的に実行可能な手法の開発には至っていません。
代わりに、デュポン社や三井東圧化学(当時)は、副産物として水を生成するベンゼンの酸化アミノ化を研究してきました。
現在、三井石油化学(日本)を除き、世界のすべてのメーカーがアニリン生産の原料としてニトロベンゼンを利用しています。
三井石油化学はフェノールも出発原料として採用しており、アリステック・ケミカル社(米国)はフェノール法を独占的に使用しています。
3.1. ニトロベンゼンの触媒水素化によるアニリンの製造
商業プロセスにおけるニトロベンゼンの強力な発熱を伴う接触水素化(200 ℃で ΔH = -544 kJ/mol)は、気相および液相の両方で実施されています。
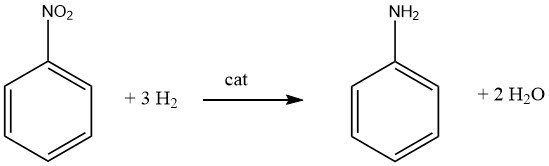
ニトロベンゼンを原料とするプロセスにおいて、効率的な熱交換と反応熱の利用は極めて重要な課題です。
3.1.1. 接触気相水素化
水素化プロセスを用いることで、ニトロベンゼンを高収率でアニリンに転換できます。
通常、固定床または流動床の気相技術が用いられます。活性炭や酸化物担体に担持された銅またはパラジウム触媒が最も効果的であり、活性と選択性を高めるために Pb、V、P、Cr などの調整剤(モディファイアー)や助触媒が組み合わされます。
ファースト・ケミカル社が運用しているロンザ法では、水素とニトロベンゼンの均一混合物を、軽石に担持した銅の固定床触媒に通します。
均一性を確保するため、ニトロベンゼンは一定の位置で新鮮な水素の加熱循環ガス流にスプレーされます。
リアクター入口におけるニトロベンゼン供給量と全水素のモル比は約 1:100 であり、反応生成物は 300 ℃以上の温度でリアクターを出ます。水素化によって発生した熱は、蒸気の生成や循環ガス流の加熱に利用されます。
過剰な水素、粗アニリン、および水は、コンデンサーでリアクター出口を冷却することで分離され、アニリンは蒸留によって精製されます。
バイエル社(現ベンビストロ等)は、バナジウムと鉛を添加して修飾したアルミナ担持パラジウム触媒を用いる、従来の固定床リアクターを活用しています。
このプロセスは、コークスに担持した 1.5~4 wt% のパラジウムと、調整剤として 0.1~2 wt% の鉛を含む固定床触媒上でのニトロベンゼンの断熱水素化を特徴としています。
気化したニトロベンゼンと水素の混合物(モル比 1:120 ~ 1:200)を、100~700 kPa の圧力、入口温度 250~350 ℃で断熱リアクターに供給します。
リアクター内の触媒層の高さは 0.1~1.0 m であり、反応生成物は冷却されることなく、最高 460 ℃の温度でリアクターを出ます。
冷却後、粗アニリン、粗廃水、および回収水素が加圧下で分離されます。粗アニリンは蒸留によって精製されます。
BASF社は気相流動床プロセスを採用しており、ニトロベンゼンは主に水素で構成される熱ガス流による噴霧によって部分的に蒸発します。
ガス流は流動触媒の存在下で循環し、反応生成物は凝縮され、粗反応生成物からアニリンが分離されます。シリカに担持し、クロム、亜鉛、バリウムの助触媒を加えた銅触媒が好んで用いられます。
ニトロベンゼンと水素の二相混合物は、流動床のさまざまな高さにあるノズルから注入され、水素過剰の条件下、250~300 ℃、400~1000 kPa で水素化が進行します。反応熱は蒸気生成に利用され、高温の製品ガスは熱交換器で冷却されます。
触媒の再生時には、触媒表面に堆積した有機物が 200~250 ℃で空気によって燃焼除去され、その後、200~300 ℃で水素を用いて酸化銅を銅に還元することで触媒が再活性化されます。
3.1.2. 接触液相水素化
ICI社(当時)やデュポン社が採用しているアニリンの水素化プロセスは、液相で実施されます。これらのプロセスは、通常 90~200 ℃の温度、100~600 kPa の圧力で運転されます。
液相反応は、スラリー床または流動床リアクターを用いて行われます。ニトロベンゼンのアニリンへの転換は通常、リアクターを一度通過するだけで完了し、収率は 98~99 % に達します。
1960年代にICIは、液相の 95 wt% 以上を占める溶媒としてアニリンを使用する連続水素化プロセスを開発しました。
このプロセスは、溶媒の沸点付近または沸点(通常 100 kPa 未満の圧力)で運転され、反応混合物を蒸発させることで反応熱の一部または全部を放散させます。
水は流出蒸気とともに除去される一方、定常状態を維持するのに十分な量のアニリンがリアクターに戻されます。触媒としては、珪藻土に担持した微細なニッケルが好んで用いられます。
一方、デュポン社は、炭素担体に白金-パラジウム触媒を担持し、調整剤として鉄を用いたニトロベンゼンの液相水素化プロセスを採用しています。
この調整剤により、良好な触媒寿命、高い活性、および芳香環の水素化に対する保護機能が得られます。プロセスにはプラグフローリアクターが用いられ、ほぼ定量的な収率を達成し、リアクター出口ではニトロベンゼンが実質的に含まれない製品が得られます。
ニトロベンゼンの接触液相水素化と気相水素化を比較すると、収率や製品品質において大きな差はありません。
しかし、液相プロセスは時間空間収率(スループット)が高く、ガス循環ループを必要としないため、エネルギー要求量が少なくなります。
逆に、気相プロセスは反応熱を効果的に利用して製品と触媒の分離を必要とせずに蒸気を生成でき、触媒寿命が長いという利点があります。
3.2. 鉄および鉄塩によるニトロベンゼンの還元によるアニリンの製造
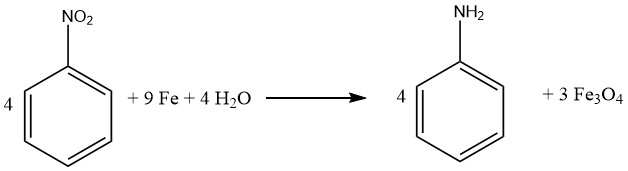
ベシャン法(Bechamp process)は、鉄と塩化鉄(II)を用いる歴史的なニトロベンゼンの還元法です。1世紀以上前の方法ですが、バイエル社のアニリンプラント2カ所では、副産物として着色鉄酸化物顔料を製造するために現在も使用されています。
ベシャン法を実施するため、攪拌機付きの反応容器内で、ニトロベンゼンを塩化鉄(II)溶液と粉砕された鉄粉を用いて還元します。
リアクターには、アニリン蒸留由来のアニリン水を含む水、鉄の 20 %、必要な量の触媒、および全ニトロベンゼン供給量の約 5~10 % が充填されます。
反応混合物を強力に攪拌しながら還流温度まで加熱し、還元が始まった後、過度な温度・圧力上昇を防ぐために残りのニトロベンゼンと鉄をゆっくりと添加します。
鉄とニトロベンゼンの添加終了後、さらに2時間容器を 100 ℃に加熱することで、約 8~10 時間で反応が完了します。石灰で中和した後、反応混合物をセパレーターに移し、アニリンを含む有機相を引き抜きます。
アニリンは、水蒸気蒸留および精留によって有機相から回収されます。セパレーターに残った材料から残留アニリンを回収した後、酸化鉄粉末のスラリーを微細な着色顔料へと加工します。
副産物である酸化鉄の色は、添加剤による反応媒体の変更、使用する鉄の種類、および焼成条件の制御によって調整可能です。
3.3. フェノールのアミノ化によるアニリンの製造

ハルコン社(当時)は、シリカ・アルミナ触媒とともにアンモニアを用いて、フェノールを気相でアミノ化する商業的なフェノールルートを開発しました。
この反応は発熱を伴う可逆反応(ΔH = -8.4 kJ/mol)であるため、高い転換率を達成するには、アンモニアの解離を抑えるための過剰なアンモニア(モル比 20:1)と低い反応温度が必要です。
不純物としてジフェニルアミン、トリフェニルアミン、およびカルバゾールが副生しますが、過剰なアンモニアの使用はこれらの不純物の生成も抑制します。収率はフェノール基準で 96 % 以上、アンモニア基準で 80 % です。
このプロセスでは、収率低下を避けるためにフェノールと新鮮なアンモニア、および循環アンモニアを別々に気化させます。その後、シリカ・アルミナ触媒を充填したアミノ化リアクター内で混合されます。
反応後、ガスを冷却して部分的に凝縮させ、過剰なアンモニアを分離塔で回収し、圧縮してリサイクルします。
凝縮生成物は乾燥塔を通って水分が除去され、さらに真空(80 kPa 未満)の仕上げ塔を通って、残留フェノールや不純物からアニリンが分離されます。一部のアニリンを含むフェノール(共沸混合物)はリサイクルされます。
ベンゼンを出発原料とするニトロベンゼンルートと比較して、フェノールルートは4つのステップ(クメンから中間体のクメンヒドロペルオキシドを経てフェノールまで)を要しますが、ニトロベンゼンルートは2つのステップで済みます。
全体的な収率と総エネルギー要求量ではニトロベンゼンルートが優位にありますが、フェノールルートは触媒寿命が長く、製品品質が高いという利点があります。
フェノール生産者から低価格のフェノールが入手可能な場合には、フェノールルートが好まれます。
4. アニリンの用途
アニリンは300種類以上の最終製品に使用されていますが、最も重要なのはポリウレタンのビルディングブロックである 4,4′-メチレンジフェニルイソシアネート(MDI)です。
4.1. メチレンジフェニルイソシアネート(MDI)
MDI は、ポリオールやポリエーテルオールなどのアルコールと組み合わされてポリウレタン(PU)を形成する極めて重要なイソシアネートです。MDI ベースの PU システムは、建設、家具、自動車、断熱材などの業界で広く採用されています。
これらの用途に加え、新しい応用分野も、特に新興市場において MDI-PU の力強い成長を支えると予測されています。
典型的な商業的 MDI プロセスでは、塩酸の存在下でアニリンとホルムアルデヒドを縮合させることにより、高分子メチレンフェニルアミンの混合物を調製します。
この反応により中間体としてアミン塩酸塩が形成され、これを苛性ソーダで中和します。反応は通常、アニリン過剰の条件下、減圧下かつ 70~105 ℃の温度で行われます。収率は約 96 % です。
その後、生成されたポリアミンを溶媒中でホスゲンと反応させ、イソシアネートの粗混合物を生成します。反応温度は約 120 ℃、圧力は 345 kPa で、収率は約 97 % です。
クロロベンゼンを蒸留で除去した後、粗製物は真空蒸留によって純粋な MDI とポリメリック MDI に分離されます。この反応の副産物として塩化水素が生成されます。
4.2. ゴム加工薬品
20世紀の最初の10年間、純粋なアニリンは加硫促進剤として利用されていました。より高い効果と安全な取り扱いへの要求から、アニリンベースのメルカプトチアゾール系およびスルフェンアミド系促進剤が開発され、現在、世界で使用されている全加硫促進剤の約 80 % を占めています。
ゴム加工薬品分野におけるアニリンのより大きな重要性は、パラフェニレンジアミン(PPD)、キノリン、ジフェニルアミンなどの老化防止剤にあります。
アニリンは、世界で消費されるすべての老化防止剤の約 70 % の原料となっています。ゴム産業における将来のアニリン需要は、合成ゴムおよび天然ゴムの需要の世界的な伸びに合わせ、年間 2~3 % の成長が見込まれています。
4.3. 染料および顔料
アニリンは染料や顔料の中間体の原料であり、既知の全処方の 50 % 以上を占めています。ただし、そのほとんどはマイナーな重要性しかありません。最大のクラスはモノアゾ、ジアゾ、およびトリアゾ化合物です。
染料・顔料の生産は、中国やインドなどのアジア諸国へシフトしています。それでも、欧州や NAFTA(米国、カナダ、メキシコ)にあるいくつかの世界規模の染料・顔料プラントでは、依然としてインジゴの製造などにアニリンが利用されています。
19世紀後半に BASF がインジゴの化学合成を工業的に実現して以来、インジゴはアニリンをベースとする最も重要な染料となりました。
この用途の世界的な成長は、年間 1~2 % の低い成長率にとどまると予想されています。
4.4. 農業用化学品(農薬)
40種類以上の殺虫剤(除草剤、殺菌剤、殺虫剤)の有効成分がアニリンを原料としており、特にアミド系および尿素系除草剤が重要です。NAFTA 内の企業は、世界の農薬用アニリン消費量の 50 % 以上を占めています。
アニリンベースの有効成分は主にライフサイクルの後半にあり、代替されつつあります。世界の消費量は年間 1~2 % 減少すると予測されています。
4.5. 医薬品
アニリンは、鎮痛剤、解熱剤、抗アレルギー剤、ビタミンの調製における安定的ではあるものの、小規模な供給源です。今後5年間、医薬品向けのアニリン生産は増加すると予想されていますが、発酵技術の普及により、ビタミン生産向けの利用は相応に減少するでしょう。
4.6. シクロヘキシルアミン / ジシクロヘキシルアミン
1990年代、アニリンはシクロヘキシルアミンおよびジシクロヘキシルアミンの生産における好ましい原料となりました。これらのアミンは、主にスルフェンアミド系加硫促進剤の中間体として利用されます。シクロヘキシルアミンは、腐食抑制剤やサイクラメート(人工甘味料)の原料としても大量に使用されています。
促進剤や水処理におけるこれらのアミンの使用は年間約 3~4 % 増加すると予測されていますが、サイクラメート製造用のシクロヘキシルアミン需要は大きく変動しており、予測が困難です。米国 FDA が人工甘味料としてのサイクラメートの禁止を解除すれば、需要の増加が期待できます。
4.7. その他
その他の多様な用途(アルキルアニリン生産、蛍光増白剤、スルホン酸など)の中で、アラミド繊維の合成におけるアニリン消費は特筆に値します。
アラミドは多才であり、同等の補強特性を大幅に軽量で実現できるため、鋼鉄の代替として使用できます。アラミドは、ブレーキライニングのアスベスト代替など、さまざまな業界での応用により健全な成長率を維持しています。
参考文献
Aniline; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a02_303.pub2