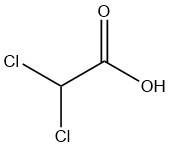
モノクロロ酢酸:反応、製法、および用途
モノクロロ酢酸とは何か?
モノクロロ酢酸は、化学式 CH2ClCOOH で表される有機化合物です。無色で吸湿性の結晶性固体であり、いくつかの異なる結晶形態で存在します。
モノクロロ酢酸は合成化合物であり、1841年に N. LEBLANC によって酢酸の塩素化生成物として初めて発見されました。その後、1857年に R. HOFFMANN が太陽光を利用して酢酸の塩素化を開始させることで合成に成功しました。
モノクロロ酢酸とそのナトリウム塩は、産業および経済的な重要性の観点から、酢酸の塩素化生成物の中で最も重要なものと見なされています。
目次
1. モノクロロ酢酸の性質
モノクロロ酢酸は水に対して非常に優れた溶解性を示し、メタノール、アセトン、ジエチルエーテル、エタノールにも良好に溶解しますが、炭化水素や塩素化炭化水素にはわずかに溶ける程度です。
2. モノクロロ酢酸の化学反応
モノクロロ酢酸の化学的特性は、カルボキシ基の高い反応性と、α位の塩素原子の置換の容易さに起因します。
モノクロロ酢酸およびその誘導体(塩、エステル、酸無水物、酸塩化物、アミド、ヒドラジドなど)は、有機合成中間体として広く利用されています。
モノクロロ酢酸の工業的応用には、無機および有機塩基との反応による塩の生成が含まれます。一部の塩はモノクロロ酢酸と付加物を形成することもあり、モノクロロ酢酸ナトリウムは重要な商業製品です。
モノクロロ酢酸メチル、エチル、tert-ブチルなどのエステルは、アルコールまたはオレフィンとの反応によって合成されます。
クロロアセチルクロリドは、モノクロロ酢酸を POCl3、PCl3、PCl5、チオニルクロリド(SOCl2)、またはホスゲン(COCl2)などのさまざまな試薬と反応させることで製造されます。
また、モノクロロ酢酸はクロロアセチルクロリドと反応してビス(クロロ酢酸)無水物を生成します。これは、P2O5 によるモノクロロ酢酸の脱水、または無水酢酸との反応によっても得られます。
クロロアセチルクロリドは、他のカルボン酸と混合無水物を形成します(例:酢酸クロロ酢酸無水物)。
塩素原子の求核置換反応は、モノクロロ酢酸を有機合成の中間体として使用する際の重要な反応です。
例えば、モノクロロ酢酸の中性または塩基性水溶液を加水分解すると、グリコール酸(ヒドロキシ酢酸)およびジグリコール酸(2,2′-オキシ二酢酸)が得られ、これがこれらの化合物の工業的な製造方法となっています。
モノクロロ酢酸の塩を加熱すると、グリコリド(1,4-ジオキサン-2,5-ジオン)が生成します。水硫化ナトリウムまたは水硫化カリウムとの反応により、チオグリコール酸およびチオジグリコール酸が形成されます。
モノクロロ酢酸はアンモニアとも反応し、反応条件に応じてアミノ酢酸(グリシン)を主生成物として、あるいはニトリロ三酢酸を生成します。
モノクロロ酢酸メチルを低温でアンモニアと反応させると、クロロアセトアミドが得られます。アルカリ溶液中で第三級アミンと反応させることにより、N-ラウリルベタインなど、商業的に重要なさまざまなベタインが形成されます。
さらに、ナフタレンのような芳香族化合物は、適切な触媒存在下でモノクロロ酢酸と求電子的置換反応を起こし、アリール酢酸を形成します。
合成カフェインの製造中間体として使用される商業的に重要なシアノ酢酸は、中性溶液中でモノクロロ酢酸とシアン化カリウムを反応させることで合成されます。
ヨード酢酸はヨウ化カリウムとの反応によって形成され、フェノキシ酢酸類は水酸化ナトリウムの存在下でのフェノールエーテル化によって合成されます。
加えて、セルロース、デンプン、グアーガムなどの多糖類を強アルカリ性の水酸化ナトリウム媒体中で反応させることにより、エーテル化度の比較的高いカルボキシメチル誘導体が合成されます。
3. モノクロロ酢酸の製造
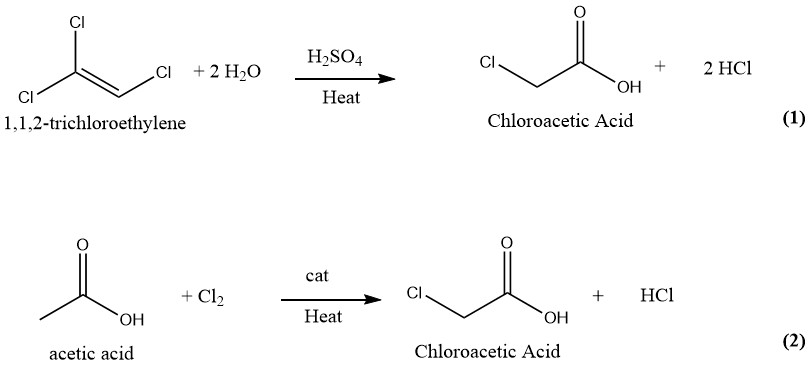
モノクロロ酢酸の製造については、数多くの技術が提案され、特許を取得しています。かつて、モノクロロ酢酸の工業的生産には、硫酸を触媒とした 1,1,2-トリクロロエチレンの加水分解(1)と、塩素を触媒とした酢酸の塩素化(2)が含まれていました。しかし、現在工業規模で採用されているのは、後者のより古いプロセスのみです。
3.1. トリクロロエチレンの加水分解によるモノクロロ酢酸の製造
モノクロロ酢酸は、同量のトリクロロエチレンと 75 % 硫酸を 130–140 ℃で反応させる連続プロセスで製造できます。トリクロロエチレンの転換が完了すると、反応混合物には約 50 % のモノクロロ酢酸と 1–2 % の水が含まれます。
その後、この混合物を真空蒸留にかけ、純粋なモノクロロ酢酸を得ます。このプロセス中、蒸気は水で洗浄され、その水は後に硫酸の希釈剤として再利用されます。
プロセス中に発生する塩化水素ガスは、新鮮なトリクロロエチレンで洗浄された後、冷凍および水への吸収によって精製されます。
この方法では、1500–1850 kg のトリクロロエチレンと 600 kg の H2SO4 (95 %) から、1000 kg の最終製品と 700–750 kg の HCl ガスが副産物として得られます。
トリクロロエチレン法は、ジクロロ酢酸やトリクロロ酢酸を含まない非常に純度の高いモノクロロ酢酸を生成します。しかし、トリクロロエチレンの高コストと、副産物として生成される多量の HCl のため、この方法は現在使用されていません。
精製手順には、トリクロロエチレン、硫酸、および水からのモノクロロ酢酸の分離が含まれます。
3.2. 酢酸の塩素化によるモノクロロ酢酸の製造
3.2.1. 合成
適切な触媒を用いた酢酸の塩素化により、酢酸からモノクロロ酢酸への極めて選択的な転換が可能です。この反応では無水酢酸が触媒として使用され、特定の反応メカニズムを促進します。
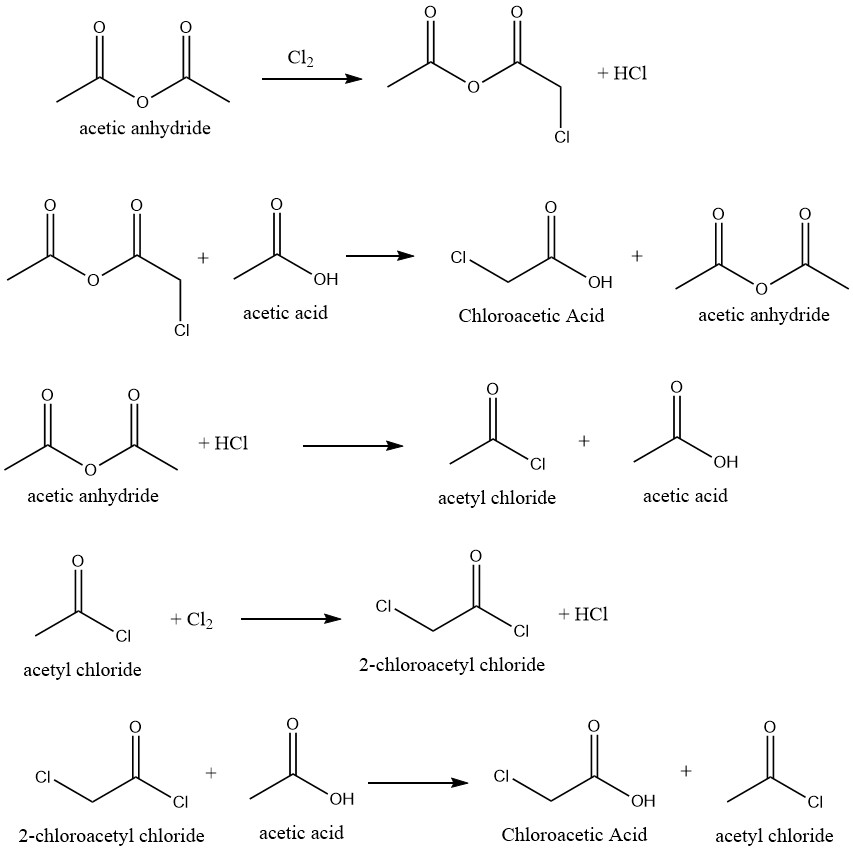
粗混合物中のモノクロロ酢酸がさらに塩素化されることで生成するジクロロ酢酸の形成を阻止するために、いくつかの抑制剤が提案されています。これにより、工業グレードの製品を製造するための精製工程の必要性を排除または減少させることができます。
3.2.2. 精製
多くの製品で求められる純度レベルを達成するには、ジクロロ酢酸およびトリクロロ酢酸の分離が必要です。しかし、これらの塩素化酢酸の沸点は非常に近いため、分留(分別蒸留)は実用的ではありません。
ジクロロ酢酸の分離のために共沸蒸留や抽出蒸留などの代替技術が提案されていますが、その有効性は不透明なままです。
重要な工業的精製プロセスの一つに、溶媒を用いない結晶化があります。これは、モノクロロ酢酸の α 修正体(α-modification)が高い融点を持つことを利用しています。結晶化後、母液からジクロロ酢酸およびトリクロロ酢酸が除去されます。
結晶化は、静置式のフィンガークリスタライザーまたは攪拌式のクリスタライザーで行われます。後者の場合、結晶化後に遠心分離機を使用して結晶スラリーから母液を分離します。
その後、製品は水または酢酸で洗浄されます。純粋なモノクロロ酢酸は通常、溶融されてフレーク状に加工されます。静置式の機械では、冷却フィンガーを使用して結晶化が行われます。
すべてのモノクロロ酢酸が結晶化した後、母液が排出され、純粋な結晶製品が溶融・フレーク化されます。
代替の精製方法として、原料を用いた薄膜結晶化プロセスも提案されています。
さらに、四塩化炭素、ジクロロメタン、または3つの塩素原子を持つ炭化水素を使用した溶媒ベースの結晶化プロセスも報告されており、濾過しやすい結晶が得られます。
どの方法を使用しても、酢酸、モノクロロ酢酸、ジクロロ酢酸、およびトリクロロ酢酸からなる母液が発生します。理想的な条件では、この混合物をさらに塩素化して、有用なトリクロロ酢酸を得ることができます。
より重要な精製方法として、ジクロロ酢酸やトリクロロ酢酸などの不要な副産物の触媒的水素化脱塩素(hydrodechlorination)があります。ジクロロ酢酸およびトリクロロ酢酸は、通常、担体(カーボンやシリカゲルなど)に保持されたパラジウム触媒を用いた高温での接触水素化によって脱塩素化できます。
気相での接触水素化脱塩素を使用する場合、ジクロロ酢酸は主に酢酸に変換されます。しかし、液相において 130–150 ℃で Pd を微分散させた不活性担体を使用すると、選択的な脱塩素が起こりモノクロロ酢酸が形成されます。
この手順の改良版として、粗酸に真空下で水素ガスを噴霧する方法や、固定床の触媒上に酸を滴下する方法なども提案されています。固定床の触媒に接触させる前に粗酸に HCl を添加すると、選択性が向上し、脱塩素の前に酸塩化物や酸無水物がケン化されます。
シリカゲル担体(粒径 40–200 μm)上の Pd 触媒は高い活性と選択性を示し、酢酸ナトリウムのような助触媒効果のある添加剤によって結果をさらに改善できます。
貴金属の表面濃縮は触媒効率を高め、使用済み触媒は塩素処理によって再活性化できます。
最適化された活性炭担体上の Pd 触媒を使用すると、水素化工程中の過剰還元副生成物(アルデヒドなど)を減少させることができ、これはループリアクターを使用して実施可能です。
非貴金属触媒を用いて 100 ~ 140 ℃で水素を使用せずに、モノクロロ酢酸中のジクロロ酢酸濃度を 2000 ppm から 210 ppm に減少させる方法も達成されています。
図1は工業的な塩素化プロセスを示しています。リアクター (a) 内で、酢酸、無水酢酸、およびリサイクルされたアセチルクロリドの混合物が 90–140 ℃で塩素化されます。生成された HCl ガスに含まれる塩素は微量のみです。
得られたモノクロロ酢酸、酢酸、および無水酢酸の混合物は、水冷コンデンサー (b) を使用して凝縮され、リアクターに戻されます。HCl ガスに同伴したアセチルクロリドは、その後の低温プロセス (c) で回収され、リサイクルされます。
HCl ガスは精製され、濃縮された塩酸水溶液に変換されます。
粗酢酸類は、水素化脱塩素工程の前に真空蒸留 (d) されることがあります。脱塩素は 120–150 ℃でパラジウム触媒と大過剰の水素を用いて行われます。酢酸は真空分留塔 (i) の塔頂から取り出され、塔底製品が純粋なモノクロロ酢酸となります。
必要に応じて、水素化工程中に形成されたアルデヒドの縮合生成物などの高沸点不純物を除去するために、モノクロロ酢酸をさらに蒸留して精製することもできます。
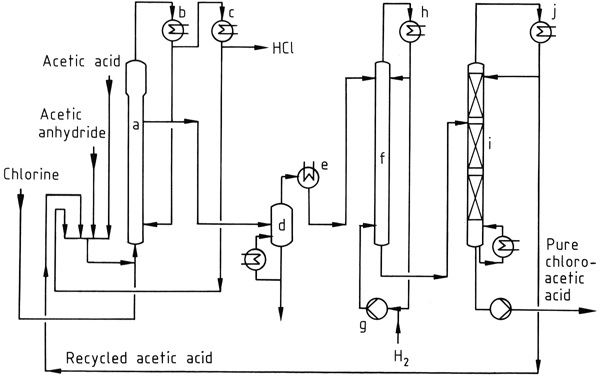
a) 塩素化リアクター、b) 酢酸・無水酢酸・モノクロロ酢酸用コンデンサー、c) アセチルクロリド用コンデンサー、d) 蒸発器、e) モノクロロ酢酸用コンデンサー、f) 水素化リアクター、g) 水素コンプレッサー、h) コンデンサー、i) 蒸留塔、j) 酢酸用コンデンサー
4. モノクロロ酢酸の用途
モノクロロ酢酸は、幅広い産業用途に利用される多才な化学化合物です。主要な用途の一つはカルボキシメチルセルロース(CMC)の製造であり、その量は年間数十万トンに達します。
CMC に加えて、モノクロロ酢酸はデンプンと反応してカルボキシメチルデンプンを生成することもでき、これは CMC と同様に広く使用されています。他の多糖類もモノクロロ酢酸で修飾できますが、それほど一般的ではありません。
モノクロロ酢酸のもう一つの重要な用途は、アリールヒドロキシ酢酸、具体的にはクロロフェノキシアルカン酸をベースとした除草剤の製造です。これらの除草剤は農業分野で最も広く使用されているものの一つです。
さらに、モノクロロ酢酸およびモノクロロ酢酸メチルは、殺虫剤ジメトエート、ならびに除草剤ベナゾリンや β-ナフチルオキシ酢酸メチルの製造に使用されます。
モノクロロ酢酸の第三の重要な用途は、メルカプト酢酸としても知られるチオグリコール酸の製造です。これは、モノクロロ酢酸を水硫化ナトリウム、水硫化カリウム、または他の硫黄化合物と反応させることで達成されます。
チオグリコール酸は、その塩、エステル、または誘導体を含むさまざまな形態で使用されます。生産されるチオグリコール酸の大部分は、ポリ塩化ビニル(PVC)用の安定剤の製造に使用されます。
また、毛髪用化粧品(パーマ剤など)や、クリーナーやパーソナルケア製品に使用される界面活性剤である N-ラウリルベタインなどの長鎖ベタインの製造など、他の工業用途にも使用されます。
これらの用途に加えて、モノクロロ酢酸は有機合成反応において多数の他の用途を持っています。例えば、シアノ酢酸やそのエステルは、重要な催眠剤であるカフェインやバルビツール酸類の製造に利用されます。
モノクロロ酢酸は、芳香族炭化水素と縮合してアリール酢酸を形成することができます。
ナフタレンと反応させると、1-ナフチル酢酸が主生成物として、2-ナフチル酢酸が副生成物として生成されます。両物質とも植物の成長を促進することが知られています。
最後に、モノクロロ酢酸はクマリンやビタミン B6 の合成において不可欠な役割を果たしています。
参考文献
Chloroacetic Acids; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a06_537.pub3