塩酸:性質、製造および用途
塩酸(別名:ムリアチン酸)は、化学式 HCl で表される強無機酸の溶液です。刺激臭のある無色の液体であり、皮膚、目、および金属に対して非常に強い腐食性を示します。
発見の歴史
15世紀、ドイツの錬金術師バレンティン(VALENTIN)は、緑ばん(FeSO4・7 H2O)と食塩を一緒に加熱しました。その結果、彼は「塩の精(spirit of salt)」と呼ばれる物質を得ました。
17世紀には、グラウバー(GLAUBER)が食塩と硫酸を組み合わせて塩酸を合成しました。1790年には、デービー(DAVY)が水素と塩素の合成を通じて塩化水素の組成を確立しました。
同年、ルブラン(LEBLANC)は自身の名を冠したソーダ製造プロセスを発見しました。このプロセスは食塩と硫酸を反応させるもので、副産物として塩化水素が放出されました。当初、これは不要な副産物と見なされ、大量に大気中へ放出されていました。
しかし1863年、アルカリ法(Alkali Act)により英国のソーダ製造業者は塩化水素を水に溶解させることが義務付けられ、これにより製造された酸の広範な工業利用が始まりました。塩酸として利用しきれない余剰の塩化水素は、塩素へと酸化されました。
20世紀初頭、クロルアルカリ電解プロセスの発展とともに、塩化水素の工業的合成が登場しました。この手法は、塩化物と硫酸または硫酸水素ナトリウムの反応に基づく方法に加え、より純度の高い製品をもたらしました。
現在、これらのプロセスの重要性は徐々に低下しています。これは、エチレンからの塩化ビニル製造などの塩素化プロセスにおいて、副産物として膨大な量の塩化水素が発生するためです。さらに、塩素を含む廃棄物の焼却時に発生するガスから塩酸を回収することも可能であり、これは環境保護への関心の高まりとも一致しています。
目次
1. 塩酸の物理的性質
塩化水素(HCl)は標準状態において、強い臭気と呼吸器粘膜への高い腐食性を特徴とする透明な気体として存在します。
塩化水素の主な物理的性質を以下の表に示します:
| 性質 | 値 |
|---|---|
| モル質量 | 36.461 g/mol |
| 融点 | -114.22 °C |
| 沸点 | -85.05 °C |
| 蒸気密度 | 1.639 g/L |
| 液体密度 | 1.18 g/mL |
| 臨界温度 | 51 °C |
| 臨界圧力 | 81.6 bar |
2. 塩酸の化学的性質
塩化水素は約1500 °Cまで熱的に安定していますが、それを超えると顕著な解離が起こります。完全に乾燥した状態の塩化水素は反応性が限定的であり、軟鋼に対してもほとんど腐食を示しません。
さらに、無水塩化水素を伴う反応には通常、触媒の存在が必要となります。逆に、塩化水素が水などの極性溶媒に溶解すると、強力な酸へと変化し、非常に反応性の高い試薬となります。
塩化水素の水への溶解度は非常に大きく、溶解時には多量の熱を放出します。これにより、極めて攻撃的な性質を持つ塩酸が形成されます。
塩酸は、市販されているほとんどの金属や合金をさまざまな程度で腐食させる能力を持ちます。したがって、金属材料を使用する場合は、適切な非金属ライニングや非金属建設材料による保護が必要となります。
厳密に定義された条件下では、タンタルや、ハステロイBのような極めて耐性の高いニッケル合金を使用することができます。しかし、卑金属は溶解し、水素ガスを発生させます。
3. 塩化水素(HCl)の製造
自然界における遊離塩化水素の存在は限られており、低濃度でしか発生しません。成層圏では約10–11体積パーセントのレベルで検出されています。
一方で、無機塩化物は広く分布しており、塩素は11番目に豊富な化学元素です。アルカリ金属およびアルカリ土類金属の塩化物、特に岩塩は、塩化水素または塩酸製造のさまざまな方法における主要な原料となります。
これらの方法には、塩素や塩素化有機化合物を中間物質として介するプロセスが含まれます。
自然現象では、火山噴火や地下ガスの放出時に塩化水素が放出されます。生成される塩化水素の量は、二酸化硫黄の量に匹敵することもあります。
塩酸は哺乳類の胃液中に自然に存在し、ヒトの胃内では約0.1 mol/Lの濃度で含まれています。
3.1. 塩化水素(HCl)の調製方法
塩化水素(HCl)は以下のようないくつかの反応によって調製されます:
1. 元素からの合成:
水素ガスと塩素ガスの結合により、塩化水素ガスが形成されます:
H2 + Cl2 → 2 HCl
2. 金属塩化物と硫酸の反応:
金属塩化物、特に塩化ナトリウムは、硫酸または硫酸水素塩と反応して塩化水素を生成します:
金属塩化物 + H2SO4 → HCl + 金属硫酸塩
3. 塩素化の副産物:
ジクロロメタン、トリクロロエチレン、パークロロエチレン、または塩化ビニルなどのさまざまな塩素化有機化合物の製造中に、一連の反応を通じて塩化水素が副産物として形成されます:
C2H4 + Cl2 → C2H4Cl2
C2H4Cl2 → C2H3Cl + HCl
4. 含水重金属塩化物の熱分解:
金属処理に使用された廃酸液に含まれる含水重金属塩化物の熱分解から、塩化水素を得ることができます。
5. 塩素化有機廃棄物の焼却:
塩素化有機廃棄物を焼却すると、結果として塩化水素が生成されます:
C4H6Cl2 + 5 O2 → 4 CO2 + 2 H2O + 2 HCl
今日、塩化水素の主な供給源は塩素化プロセスから得られる副産物です。必要とされる精製レベルは用途によって異なります。現在、廃棄物からの塩化水素の回収が増加しています。
さらに、フリーデル・クラフツ触媒の加水分解のような望ましくない反応でも塩化水素が形成されることがあります:
AlCl3 + 3 H2O → Al(OH)3 + 3 HCl
3.2. 塩酸(HCl)の工業的製造
3.2.1. 水素と塩素から
塩化水素を製造する最も直接的な方法は元素成分からの直接合成であり、非常に純度の高い製品が得られます。この反応は強い発熱反応で、標準反応エンタルピー(ΔH)は -184 kJ です。
水素と塩素の混合物は、広い組成範囲において極めて爆発しやすいため注意が必要です。光が爆発の開始剤となることもあります。したがって、工業プロセスでは反応性の高い塩素と水素の混合物形成を防ぐための予防措置を講じなければなりません。
工業生産ではバーナーが使用され、塩素と水素は同心円状の管を通って燃焼室に個別に供給されます。点火されると、塩素は水素の存在下で燃焼し、2000 °Cを超える温度で高温かつ静かな炎を発生させます。
シリカはバーナーの構造材料として有効であることが実証されています。鋳鉄や鋼(水冷式の場合もある)、あるいはグラファイトも利用されています。
通常、バーナーは円筒形の燃焼室の底部に配置され、炎は垂直上方に向けられます。燃焼室自体は鋼製で、耐火煉瓦がライニングされています。燃焼室には、適切なサイズと形状の冷却セクションが接続されています。反応物が非常に湿っていたり汚染されていたりする場合は、シリカやグラファイトなどの耐食性材料を使用する必要があります。
既存の製造プラントは主に炭素鋼で建設されており、生成された塩化水素は、水性塩酸が凝縮しない温度まで水冷されるのみです。
主な不純物は水素中の水分と塩素中の酸素ですが、一酸化二塩素(Cl2O)や二酸化炭素などの酸素化合物も、水を形成することで問題を引き起こす可能性があります。
原料の混合比は、生成される塩化水素の用途に基づいて調整されます。水素または塩素をわずかに過剰に使用することもあります。正確に等モルの混合物で作業することは推奨されません。反応が完全に定量的ではなく、爆発性混合物の形成を防ぐことがより困難になるためです。
制御の偏差により、水素過剰と塩素過剰の間で断続的なシフトが生じると、時折爆発性混合物が発生することがあります。通常、塩化水素中の水素は塩素よりも問題が少ないため、1~2%のわずかな水素過剰が一般的に用いられます。原料の純度によっては、塩素を完全に含まない塩化水素を得ることが可能であり、その場合の不純物は過剰な水素のみとなります。
この高純度塩化水素は、極めて純粋な塩酸の製造に使用されるほか、液化されたり、乾燥ガスとして鋼製パイプラインを通じて直接ユーザーに供給されたりします。
合成炉と冷却器に鋼を使用することは魅力的な選択肢です。これにより、塩素と水素の圧力、およびパイプライン内の温度と圧力によって決定される高圧下での運転が可能になります。
水性塩酸の凝縮を防ぐために、圧力を十分に低く、または温度を十分に高く維持することが極めて重要です。例えば、ヒュルス(Hüls)で稼働している鋼製炉は、それぞれ1日あたり30~40トンの塩化水素を生産できます。
生成された塩化水素ガスは最大0.7 MPaの圧力を持ち、水分含有量は50 ppm(体積比)未満であるため、プラントからの輸送には鋼管の使用が必要となります。
化学的に関連するプロセスには、塩素と炭素(コークスの形態)および水蒸気の反応があります:
C + 2 H2O + 2 Cl2 → 4 HCl + CO2
別の関連プロセスとして、塩素と二酸化硫黄および水の反応があります:
SO2 + 2 H2O + Cl2 → 2 HCl + H2SO4
3.2.2. 金属塩化物と硫酸の反応
硫酸塩法はエネルギー消費量が多いことが特徴です。その結果、副産物として大量の塩化水素を発生させる他のプロセス(特に有機塩素化)と比較して、その重要性は徐々に低下しています。
さらに、「硫酸塩法による塩酸の方が純度が高い」という主張もはや妥当ではありません。現在では、副生酸も高品質基準の要件を満たすよう十分に精製できるためです。したがって、ここでは最も重要な硫酸塩・塩酸プロセスのみを取り上げます。
食塩と濃硫酸の反応は比較的低い温度(150~300 °C)で起こり、塩化水素と硫酸水素ナトリウムが形成されます。後者は、最低550~600 °Cの温度で過剰な塩化ナトリウムと反応し、中性の硫酸ナトリウムを生成します。
現在、硫酸のみが原料として使用されています。マンハイム法(Mannheim process)では硫酸ナトリウムが製造され、ベルリン塩酸法(Berlin process)では硫酸水素ナトリウムが利用されます。
マンハイム法では、煉瓦ライニングを施した外部加熱式のマッフル炉が使用されます。これらの炉には、ペースト状の塊に固まりができるのを防ぎ、生成された硫酸ナトリウムを排出するための、掻き取り作用を持つ攪拌機構が備わっています。
塩化水素はマッフルの側面から排出され、ファンによって次段へと送られます。炉内はわずかな減圧状態に維持されます。炉からの排ガス混合物には、最大85%の塩化水素のほか、空気、硫酸ミスト、および微細な塩粒子が含まれています。通常、ガスはコークスや活性炭によるろ過、湿式洗浄、または化学反応を含む複数の精製段階を経て処理されます。
ベルリン塩酸法では、マンハイム法よりも大幅に高い純度の塩化水素ガスが得られます。食塩と硫酸の反応は、鋳鉄製のレトルト内で約300 °Cに保たれた溶融硫酸水素ナトリウム中で行われます。
あるいは塩化カリウムを使用することもでき、その場合は塩化水素と硫酸水素カリウムが生成されます。このプロセスは、主な製品が形成されるカリウム塩(すなわち KHSO4 および K2S2O7)であり、塩化水素は副産物と見なされるため、一定の商業的意義を保っています。
3.2.3. 塩素化副産物としての回収
塩化水素および塩酸の主要な供給源は、塩素化プロセスの副産物です。1,2-ジクロロエタンを熱分解して塩化ビニルを製造する工程は、塩化水素生産の最大の貢献者です。
発生および消費される塩化水素の量は膨大になる可能性があり、多くの施設で約10,000 m3/h(16 t/h または 140,000 t/a)以上を生産しています。そのため、塩化水素は原料として利用する化学プラントへ直接供給されることがよくあります。塩化水素の貯蔵容量は通常比較的小さいため、生産速度と消費速度のバランスを維持することが極めて重要です。
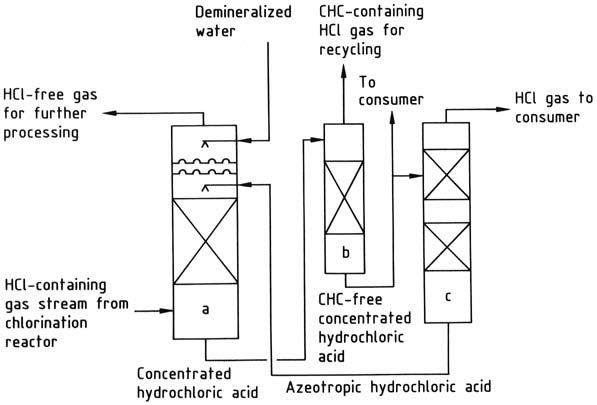
a) 塩化水素吸収塔; b) 塩素化炭化水素ストリッピング塔; c) 塩化水素脱着塔
有機塩素化を通じて生成された塩化水素は、さまざまな処理方法を経ることがあります:
1. 塩素化炭化水素の単純凝縮:残留する塩素化炭化水素や他の副産物が、ガスとして供給される塩化水素にとって問題とならない場合に使用されます。
2. 蒸留による塩化水素の分離・精製:より純度の高い製品が必要な場合は、液化ガスの分留が用いられます。例えば、1,2-ジクロロエタンの熱分解から得られるガス状生成物は液化され、蒸留によって塩化ビニルと塩化水素に分離されます。極低温での液化は経済的に現実的ではないため、凝縮と蒸留は加圧下で行われます。この方法の利点は、塩化水素ガスが後続の処理に十分な圧力(通常1~2 MPa)で生成されるため、追加の機械的圧縮が不要になることです。
3. 塩化水素の水吸収:この方法は中間製品として塩酸を生成しますが、建設材料に関連する課題があります。しかし、フッ素樹脂の導入により、これらの問題は大幅に緩和されました。水または20重量%の塩酸溶液を使用して塩化水素を吸収させることができます。最終製品として30~35重量%の塩酸を製造することが主な目的である場合に適しています。
塩酸中に塩素化炭化水素が存在することが望ましくない場合は、それらを除去するためのストリッピング工程を実施できます。ガス流から塩化水素を除去するために、吸収塔に少量の水が導入されます。これにより、ガス流から塩化水素が取り除かれます。
生産ガス流からの塩化水素の水吸収における経済性を評価する上で、いくつかのプロセス・装置パラメータが重要です:
- ガス流中の塩化水素濃度により、吸収塔内で維持すべき圧力と温度が決定されます。
- 形成される濃縮酸の濃度が高くなるほど、純粋な塩化水素ガスを遊離させるために必要なエネルギーは減少します。
- 塩化水素濃度の低いガス流から濃塩酸を製造するには、圧力の上昇や温度の低下といった多大な労力が必要となります。
吸収装置の構造材料の選択は、濃塩酸と塩素化炭化水素の両方による攻撃の可能性があるため制限されます。酸の冷却にはグラファイト熱交換器が利用されます。ポンプには、伝統的に特殊セラミック材料が経済的な選択肢となってきました。蒸留塔には耐酸煉瓦またはグラファイトブロックがライニングされ、煉瓦はフェノール樹脂を用いて接合されます。鋼製ケーシングと煉瓦壁の間には、細孔や亀裂からの酸の攻撃を防ぐために、耐酸性ゴムライニングがしばしば施されます。
フェノール樹脂のみで作られた装置は優れた耐薬品性を示しますが、脆くて機械的に弱いため、通常はガラス繊維強化ポリエステル樹脂の外殻などの支持が必要です。同様の考慮事項は塩素化炭化水素ストリッピング塔にも当てはまります。脱着塔は、運転温度が高いためグラファイトで作られます。あるいは、内面に煉瓦ライニングを施したゴムライニング塔も使用可能です。
フッ素樹脂、特にポリテトラフルオロエチレン(PTFE)をライニングした鋼製カラムは優れた結果を示していますが、ミクロ多孔性、引き裂き耐性、および流動特性に関して製造メーカー間で製品のばらつきが存在する場合があります。
フッ素樹脂コーティングされた鋼鉄製カラムは、高圧での運転が可能であるという点でグラファイト製カラムよりも優位性がありますが、PTFEライニングが損傷すると鋼鉄製の外筒が急速に腐食されるというリスクを伴います。これらのカラムは小さな個別ユニットで構成できるため、迅速な交換が可能であり、メンテナンスによるダウンタイムを最小限に抑えることができます。
いずれの場合も、熱交換器にはグラファイトが使用されます。タンタルライニングやタンタル製蒸発器の採用も可能ですが、水素吸収による脆化(ぜいか)を避けるための注意が必要です。さらに、フッ化水素が混入していないことが絶対条件となります。
完全に乾燥した塩化水素は、鋼鉄製の配管や圧縮機を腐食させません。以前は塩化水素ガスの乾燥に濃硫酸が用いられていました。別のアプローチとして、HCl-H2O 系の物性を利用する方法があります。
低温下では、高濃度塩酸上の水の分圧は極めて低くなります。これを利用し、塩化水素を十分に低い氷点下の温度まで冷却することで乾燥させることが可能です。
わずかに加圧された状態(P ≈ 0.3 MPa)では、-10 ℃まで冷却すれば通常は十分な結果が得られます。ただし、深刻な腐食を防ぐために、塩酸ミストは完全に除去しなければなりません。
3.2.4. 廃棄物焼却からの回収
あらゆる塩素化プロセスにおいて、目的の生成物とともに不要な塩素化炭化水素の生成は避けられません。これらの利用不可能で、しばしば有害な物質は、環境保護の観点から適切に処理する必要があります。
一つの手法として焼却処理があり、これにより塩素化炭化水素を塩化水素、水、および二酸化炭素へと変換します。経済的および環境的な配慮から、塩化水素の回収は不可欠です。
採用される具体的な技術は多岐にわたりますが、基本的な原理は共通しています。燃焼は、1000 ℃を超える温度で耐火材料をライニングした炉内で行われます。
通常、最大 70 wt % の塩素を含む廃棄塩素化炭化水素は、良好な燃焼特性を示す傾向があります。しかし、塩素含有量がさらに増加すると発熱量が低下し、燃焼プロセスを維持するために燃料油やガスの添加が必要になります。
最適な反応条件は以下の範囲に収まります:
1. 塩素化炭化水素を完全に分解するために、過剰な酸素が存在しなければなりません。生成された塩化水素ガスは、以下のディーコン反応(Deacon equation)に従って酸素と反応します:
2 HCl + 0.5 O2 ↔ Cl2 + H2O
温度を上げると平衡は左に移動し、塩化水素の生成が促進されます。塩素の生成を防ぐため、構造材料が許容する範囲内でできるだけ高い温度が維持されます。
水の分圧が高く酸素過剰率が低い場合でも、目的の平衡移動を達成するには 1000 ℃以上の温度が必要です。このアプローチにより、塩素濃度を許容範囲内に保ち、完全燃焼を確実にします。
2. 窒素酸化物(NOx)の生成を防ぐため、反応温度は 1200 ℃を超えないようにすべきです。これらの酸化物は製品である塩酸を汚染し、廃ガス浄化において課題となります。空気の代わりに純酸素を使用することも解決策の一つとなり得ます。
これらの理由から、廃棄塩素化炭化水素の焼却は通常 1000 ℃から 1200 ℃の間で行われます。燃焼ガスの冷却や蒸気の発生については、構造材料に関連する課題が生じることがあります。腐食性の燃焼生成物が存在しないことを確認することが重要です。
処理される廃棄物は、予想される燃焼生成物とその濃度、挙動を正確に予測するために、微量不純物を含めた組成が明確である必要があります。また、塩素の再生成を防ぐため、緩慢な冷却ではなく急速冷却(急冷)が好まれます。
塩化水素は、吸収プロセスを通じて燃焼ガスから回収されます。回収プロセスは塩素化プロセスで用いられるものと類似していますが、いくつかの例外があります:
- 水蒸気が常に存在するため、乾式プロセスは不可能です。
- できるだけ高濃度の塩酸が形成されるようにガスを凝縮させる必要があります。これにより、塩化水素ガスまたは濃塩酸のいずれかを回収できます。希塩酸は商業的価値が限られているためです。
- 酸の凝縮が起こりうる箇所では、特有の腐食問題に対処する必要があります。これは定常的には起こらなくても、リスクとして存在します。
- 燃焼ガスを直接使用する場合は、運転温度を常に塩酸の凝縮温度以上に維持しなければなりません。
塩素化炭化水素の焼却を通じて 33 wt % の工業用塩酸を製造している最も古いプラントの一つは、フランスのサン・トバン(St. Auban)にあり、アトケム(Atochem)社によって運営されています。1975年に設立されたこのプラントは、年間約 16,000 トンの塩素化炭化水素を処理しています。
3.3. 塩酸の精製
活性炭は、吸着によって塩化水素ガス中の SO2、As、Cl2 などのさまざまな不純物を効果的に除去できます。硫酸法プロセスの重要性が低下するにつれ、塩化水素ガスまたは塩酸からの塩素化炭化水素の除去が実用上より重要になっています。
塩化水素ガスは、高沸点溶媒を用いた低温スクラビング(洗浄)によって精製できます。溶媒としては、別の塩素化炭化水素(例:ヘキサクロロブタジエンやテトラクロロエタン)または特定の石油留分が用いられます。このような処理を施した後では、活性炭の使用が不要になることも多いです。
塩素は、四塩化炭素を用いることで除去可能です。これは、塩素が塩化水素ガスに比べて四塩化炭素に対して格段に高い溶解度を示すためです。
直接使用される塩酸、あるいは塩化水素発生用に供される塩酸には、主に塩素化炭化水素などの揮発性不純物が含まれています。このような場合、不純物は酸をストリッピング(放散)することで除去できます。
不活性ガスを用いたストリッピングは、エネルギー消費を抑えられる実行可能な選択肢です。しかし、多くの場合、環境への配慮からガスの加熱が好まれます。鉄をはじめとする無機不純物は、イオン交換によって除去できます。
4. 塩酸の用途
塩酸および塩化水素は、さまざまな工業プロセスにおいて極めて重要な化学物質です。
有機塩素化プロセスの副産物を完全に活用する必要があるため、通常、塩化水素の大部分は製造者によって即座に消費されます。これは、オキシ塩素化法やヒドロ塩素化法、あるいは KEL法、改良ディーコン法、塩酸電解などの塩素回収法を通じて達成されます。
水溶液としての塩酸は、強無機酸として広範な用途を持ちます。塩化物の製造、鉱物の溶解、金属の酸洗い(ピックリング)およびエッチング、水処理用のイオン交換樹脂の再生、アルカリ性製品や廃棄物の中和、クロルアルカリ電解における塩水の酸性化、その他多くの工業プロセスで使用されています。
5. 毒性学および産業衛生
塩化水素は、目、呼吸器、および(程度は低いものの)皮膚に対して強い刺激を引き起こすことが知られています。その蒸気にさらされると角結膜炎を引き起こす可能性があり、吸入すると粘膜の刺激や損傷を招く恐れがあります。塩化水素の臭気は通常 1-5 ppm の濃度で感知され、5-10 ppm になると不快感を伴うようになります。
高レベルの塩化水素に職業的に長期間さらされると、一見許容できるように思える濃度であっても、慢性気管支炎、胃腸障害、および歯の腐食のリスクが高まる可能性があります。10 ppm を超える濃度では、たとえ体が慣れていたとしても強い刺激が生じます。
塩酸を扱う作業者は、適切な保護メガネ、防護服、ゴム手袋、およびブーツを着用する必要があります。蒸気の吸入は避けなければならず、無機ガス用の吸収缶を備えた防毒マスクの使用が推奨されます。
ドイツ連邦共和国では、EEC指令に基づき、塩化水素および塩酸(>10 wt %)に対して危険物質規制が適用されています。これらの規制では、ハザードシンボル、安全上の指示、および取り扱い上の注意事項が規定されています。
皮膚や目に付着した場合は、直ちに大量の水で十分に洗い流すことが不可欠です。汚染された衣類も同様に処理し、アルカリ性の洗浄液を使用する場合もあります。
特に高圧下で塩化水素を扱う際は、事故に備えて独立した空気源を持つ呼吸器(空気呼吸器)と全身防護服を即座に使用できる状態にしておくことが極めて重要です。
ドイツにおける塩化水素の最大許容濃度(MAK)は体積比で 5 ppm(7 mg/m³ に相当)です。米国でも同様の値が閾値(TLV)として採用されています。ソビエト連邦では、制限値は 3 ppm(5 mg/m³)と定められていました。
大気汚染防止規制では、大気中の塩化水素濃度制限を年平均 0.1 mg/m³、短期間で 0.2 mg/m³ などと定めています。植物の種によって塩化水素曝露に対する耐性は異なります。
産業廃ガスに関しては、ドイツの規制によれば、塩化水素濃度は一般に 30 mg/m³ を超えてはなりませんが、廃棄物焼却施設では制限値が 50 mg/m³ となっています。ガスの洗浄コストは、これらの基準によって大きく変動します。
塩化水素の除去には水によるスクラビングで十分な場合が多いですが、最終段階でアルカリ溶液を用いたスクラビングを含む多段処理が必要になることもあります。
場合によっては工業用塩酸を製造できず、希薄な酸を中和してから廃水として処理することもあります。苛性ソーダ(水酸化ナトリウム)による中和を行えば、塩素プラントへのリサイクルに十分な純度の食塩水が得られる場合もあります。
参考文献
Hydrochloric Acid; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a13_283