水酸化ナトリウムの工業的製法
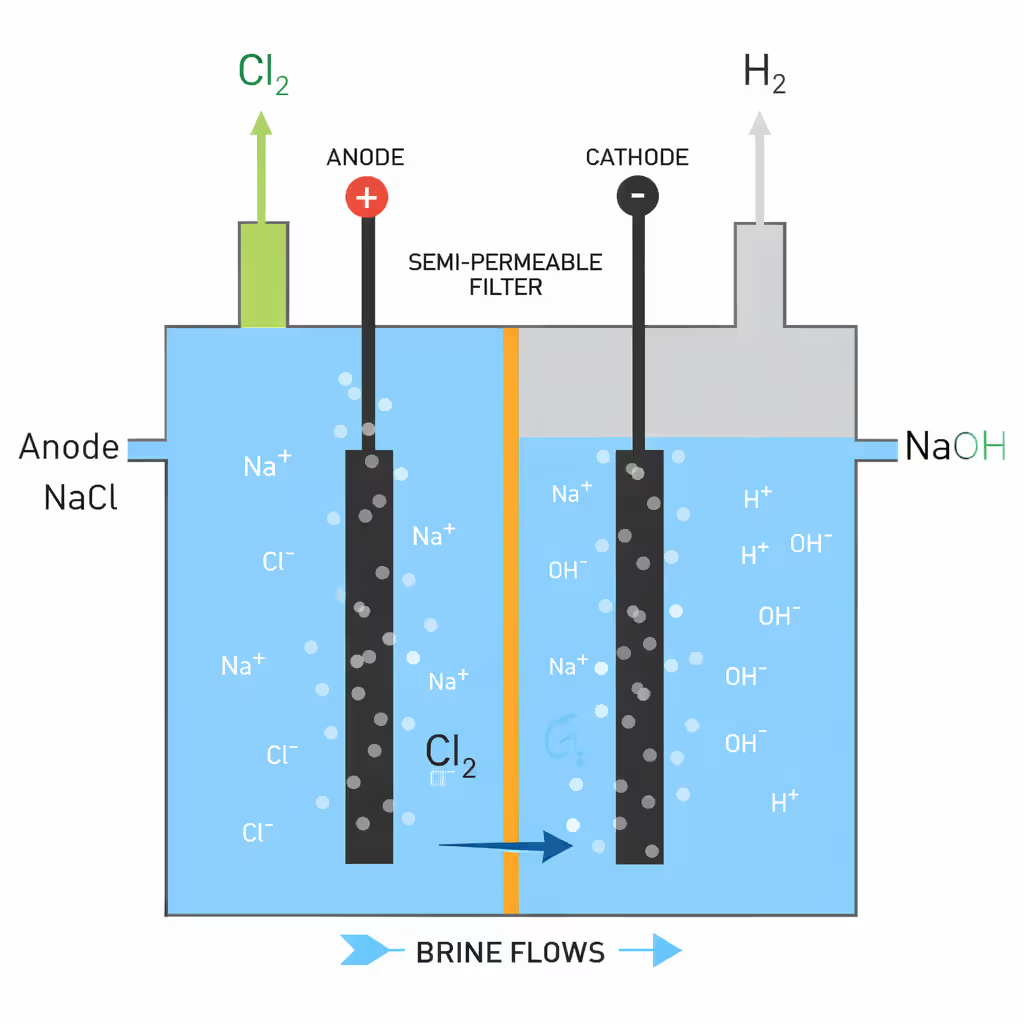
1. 水酸化ナトリウム溶液の製造
1.1. 塩化ナトリウムの電解
水酸化ナトリウム溶液の工業的生産は、主に塩化ナトリウムの電気分解によって行われます。
この反応では、以下の総括反応式に示されるように、水酸化ナトリウム溶液、塩素ガス、および水素ガスが 1 : 0.88 : 0.025 の質量比で得られます。
2 NaCl + 2 H2O → 2 NaOH + Cl2 + H2
イオン交換膜法(膜法)は、クロルアルカリ生産におけるアマルガム法や隔膜法の代替手段として、1980年代初頭に導入されました。
2004年には、膜法は全クロルアルカリ設備容量の44%以上を占めるようになりました。このプロセスは約30%の電力を節約でき、現在では「利用可能な最良の技術(BAT)」と見なされており、新規プラントでの採用が増えています。
日本では、コストと品質の検討の結果、1988年までにアマルガム法が段階的に廃止され、一部の隔膜法プラントも膜法プラントへと転換されました。
アマルガム法では、80~120 ℃で黒鉛触媒を用いてナトリウムアマルガムと水を反応させることで、水酸化ナトリウム溶液が製造されます。これにより得られる 50 wt% の溶液は、冷却後、遠心分離または濾過によって水銀を除去しただけで、そのまま製品として販売されます。
隔膜法では、約 18 wt% の塩化ナトリウムと 10~15 wt% の水酸化ナトリウムを含む溶液が生成されます。
蒸発工程において、希薄な塩化ナトリウム溶液と共に持ち込まれた不純物は、分別結晶によって溶解度限界まで除去されますが、塩化ナトリウム含有量は 1~1.5 wt% 程度までしか下げることができません。
膜法は、電解液の混合を防ぐために、水力学的に不透過性の膜を使用するのが特徴です。
このプロセスでは、アマルガム法に匹敵する、実質的に塩化物を含まない高純度の水酸化ナトリウム溶液が製造されます。ただし、セルの運転が中断されると、Cl– イオンが膜を透過して拡散するため、塩化物含有量が約10倍に増加することがあります。
アノライト(陽極液)中に存在する硫酸塩や塩素酸塩も、膜法セルから得られる苛性液中の不純物濃度に影響を与えます。これは、陽イオン選択性膜であっても、陰イオンに対してわずかな残留透過性を持つためです。ほとんどの膜型電解槽は、NaOH 濃度が 30~35 wt% の時に最も優れた経済性を示します。
セル内で 50 wt% の水酸化ナトリウム溶液を直接製造できるイオン交換膜も開発されていますが、電圧が大幅に上昇するという代償が伴います。このような膜は、蒸気コストが高く電気コストが低い場合にのみ実現可能です。
通常、30~33 wt% の水酸化ナトリウム溶液は、蒸気コストやプラント規模に応じて、2段または3段の流下膜式蒸発器(フォーリングフィルム・エバポレーター)で濃縮され、商用の 50 wt% 溶液となります。
3段蒸発器の蒸気消費量は NaOH (100%) 1トンあたり 0.55トン、2段蒸発器の場合は 0.71トンであり、水酸化ナトリウム溶液と蒸気は向流(カウンターカレント)で流されます。
隔膜法の液とは異なり、膜法液の蒸発では、熱交換器を汚染したり配管を摩耗させたりするような固体物質は生成されません。
ニッケルやステンレス鋼などの適切な建設材料を使用すれば、蒸発工程中の金属混入は約 1 wt ppm 程度に抑えられます。
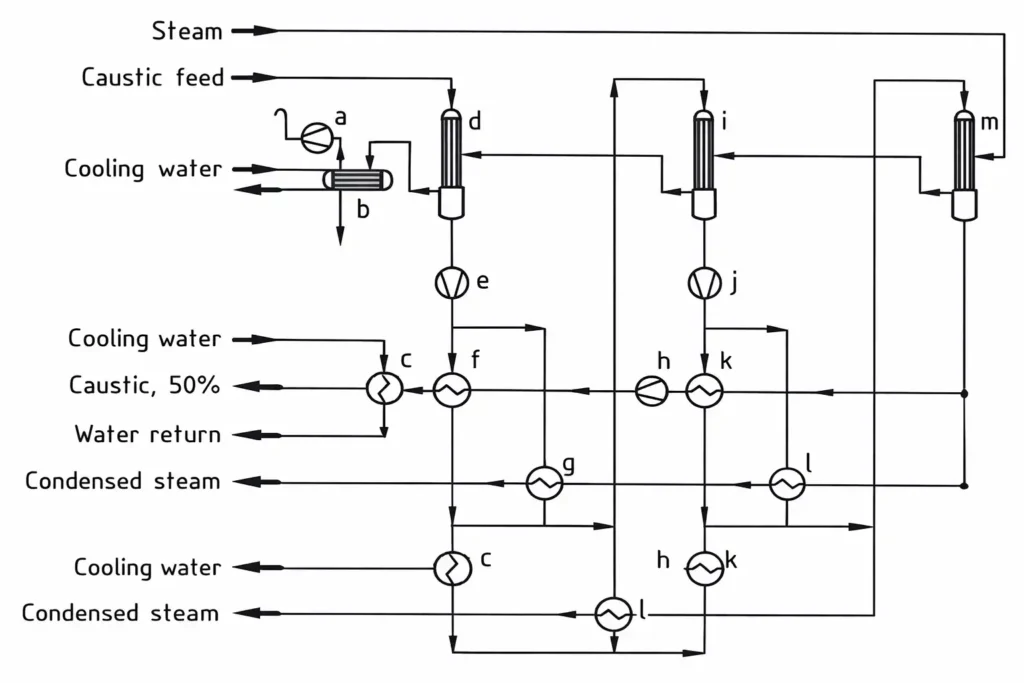
a) 真空ポンプ、b) コンデンサー、c) 苛性冷却器、d) 第一蒸発器、e) 苛性ポンプ、f) 第一苛性熱交換器、g) 第二熱交換器、h) 苛性ポンプ、i) 第二蒸発器、j) 苛性ポンプ、k) 第二苛性熱交換器、l) 第一熱交換器、m) 第三蒸発器
水酸化ナトリウムの製造に使用される3つの異なる電解プロセスは、それぞれエネルギー要件が異なります。
膜法は電気エネルギーの必要量が最も少なく、NaOH 1トンあたり 2200~2500 kWh の範囲です。ただし、50 wt% 溶液を作るには、蒸気の形で NaOH 1トンあたりさらに 200~300 kWh 相当のエネルギーが必要です。
対照的に、隔膜法はアマルガム法よりも電気エネルギーの使用量は少ないですが、蒸発段階で NaOH 1トンあたり 700~900 kWh を必要とします。その結果、隔膜法が総エネルギー消費量で最も高くなります。
電気エネルギーへの需要が高いため、研究者はセル電圧の低減に注力してきました。膜型セル法では、燃料電池に似た酸素陰極(ガス拡散電極)を使用することで、電圧を約 1 V 低減できます。ただし、この場合は副産物としての水素は生成されません。
この技術は大きな関心を集めています。電解槽の設計、酸素陰極の開発、およびそれらの電解槽への組み込みが主要な焦点となっています。また、運転パラメータや電解槽周辺機器の探索にも研究努力が向けられています。
β-Al2O3 隔膜を用いた 350 ℃での溶融 NaCl 電解は有望な技術です。ラボスケールのセルでは、NaOH 1トンあたり 2350 kWh の消費電力を達成しています。しかし、この技術はまだ商業規模では使用されていません。
1.2. その他のプロセス
炭酸ナトリウム溶液の苛性化による水酸化ナトリウムの製造は、最も古くから知られている方法です。電解法が登場するまでは、これが唯一の利用可能な方法でした。合成または天然の炭酸ナトリウムにアクセスできる企業の間で、この手法は再び関心を集めています。
このプロセスでは、約 12% の熱い炭酸ナトリウム溶液に生石灰を混合します。沈殿した炭酸カルシウムを除去し、約 12% の水酸化ナトリウム溶液を数段階で蒸発させます。
Na2CO3 + CaO・H2O → 2 NaOH + CaCO3
NaCl や Na2SO4 など、沈殿する不純物は濾過して取り除かれます。
電解セルと透析セルを組み合わせることで、ナトリウム塩を対応する酸とアルカリに分離することができます。
Na2SO4 + 2 H2O → 2 NaOH + H2SO4
2室型セルでは陽イオンまたは陰イオン交換膜を使用でき、3室型セルでは陽イオンおよび陰イオン交換膜を使用できます。あるいは、陽イオン、陰イオン、およびバイポーラ膜を組み合わせた多室型セルを使用することも可能です。
しかし、工業的に運転されているすべてのセルにおいて、得られるのは原料の塩を一部含む希薄な水酸化ナトリウム溶液(15~30 wt%)です。
したがって、このタイプのプロセスは、得られた希薄水酸化ナトリウム溶液を中和目的でリサイクルできるような、ナトリウム塩を含む廃水の処理に最も適しています。
フェライト回収法は、小規模な製紙パルププラントに適した、水酸化ナトリウム溶液製造の代替手段を提供します。
このプロセスでは、ナトリウム塩と有機物質を含む廃液を蒸発させます。得られた残渣を Fe2O3 と混合して焼成し、フェライト酸ナトリウムを形成させ、これを水で分解することで NaOH と Fe2O3 を得ます。
2. 無水水酸化ナトリウムの製造

固形水酸化ナトリウム(苛性ソーダ固形物)は、水酸化ナトリウム溶液を水分含有量が 0.5~1.5 wt% 未満になるまで蒸発させることで得られます。
スイスのバーゼルにあるベルトラム社が建設したプラントのフロー図(図1)に示されるように、多段式の装置を使用することで最も効率的なエネルギー利用が達成されます。
第一段階では、主濃縮器からの蒸気の熱を利用し、予備濃縮ユニットにおいて 50 wt% 溶液を真空蒸発させ、濃度を約 60 wt% まで高めます。
第二段階では、流下膜式蒸発器において、溶融塩熱媒体(NaNO2 – NaNO3 – KNO3)を用いて 400 ℃を超える温度で加熱することにより、約 99 wt% の濃度を達成します。
濃縮された製品は、ガスリフトポンプとして機能するフラッシュ蒸発器に送られ、溶融 NaOH は真空によって加熱されたライザー管内を上昇し、残りの水分が蒸発します。蒸気の気泡が溶融 NaOH をシステムの最高点まで押し上げ、そこで蒸気がポンプで排出されます。
ほぼ無水の溶融物はダウンカマー管を通って保持容器に入り、そこから成形プラントへと送られます。
早期の結晶化を防ぐため、保持容器、ポンプ、および配管は加熱しておく必要があります。
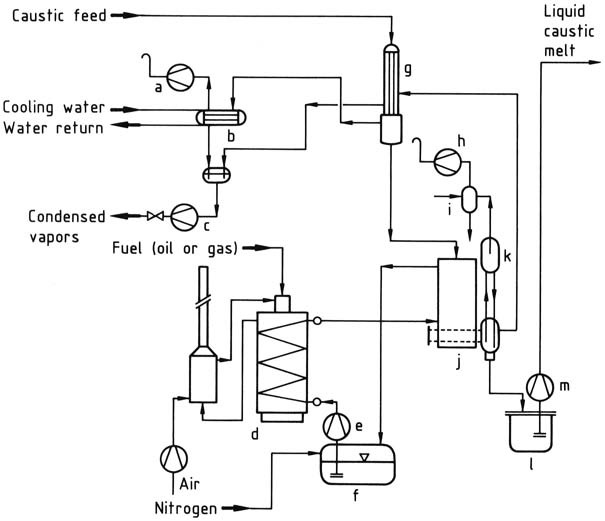
a)真空ポンプ、b)凝縮器、c)凝縮ポンプ、d)炉ユニット、e)塩溶融ポンプ、f)加熱塩溶融タンク、g)予備濃縮ユニット、h)真空ポンプ、i)凝縮器、j)流下膜濃縮装置、k)フラッシュ蒸発器、l)加熱苛性溶融タンク、m)苛性溶融ポンプ形成
成形
固化していない1水和物による固結(ケーキ化)を防ぐため、NaOH 溶融物の冷却と固化は、NaOH の凝固点(322 ℃)と1水和物(NaOH・H2O、62 ℃)の凝固点の両方を速やかに通過するように行う必要があります。
市販されている固形水酸化ナトリウムには、フレーク、プリル、鋳造ブロック、タブレット、ブリケット、顆粒など、さまざまな形状があります。
フレークの厚さは約 1.5 mm、直径は 5~20 mm で、かさ密度は約 0.9 kg/dm3 です。壊れやすく、取り扱い中に粉塵が発生しやすい傾向があります。
プリルのかさ密度は 1 kg/dm3 以上で、直径 0.1~0.8 mm(マイクロプリル)または 0.5~2.5 mm の球状をしています。
1. フレーク
フレークの製造では、溶融 NaOH を、内部冷却された回転ドラムが一部浸漬している槽に供給します。溶融物質はドラム表面で固化し、ナイフで削り取られます。
得られた NaOH のシートはフレーク状に砕かれ、中間貯蔵サイロへ輸送されます。ブリッジ現象を防ぐため、材料は小さなサイロに保管され、できるだけ早く袋またはスチールドラムに梱包されます。
2. プリル
プリルは、約 360 ℃の溶融 NaOH を噴霧して液滴にすることで製造されます。回転ディスクまたはバスケットを使用して微細な液滴を作り、表面張力によって均一な球体を形成させます。
プリルがシャフト内を落下する際、空気を上方へ吹き付けて約 250 ℃まで冷却します。完成した製品はロートで回収され、冷却ドラムに移されて約 50 ℃まで冷却されます。
プリルはフレークよりも固結しにくく、流動性が高く、ほとんど粉塵が出ないため、サイロやコンテナでの貯蔵や輸送に理想的です。
3. 鋳造ブロック
鋳造ブロックの場合、溶融 NaOH は鉄製ドラムまたは同様の容器に直接流し込まれます。鉄によるさらなる汚染を防ぐため、ドラムは外部から水のスプレーで冷却され、容器の壁面に水酸化ナトリウムの固化膜を即座に形成させます。
4. 特殊形状
タブレット、ピル、またはペレットは液滴法によって製造されます。銀製の特殊な装置から溶融 NaOH を、ゆっくり回転する冷却テーブルまたはコンベアベルトの上に滴下します。
このプロセスでは金属不純物の含有量が少ない製品が得られるため、分析用の少量生産に理想的です。
参考文献
“Sodium Hydroxide”. Ullmann’s Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH.- https://onlinelibrary.wiley.com/doi/10.1002/14356007.a24_345.pub2