無水酢酸:性質、反応、製造および用途
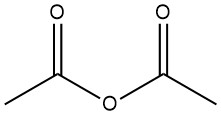
無水酢酸は、化学式 (CH3CO)2O で表される有機化合物です。刺激臭を持つ無色の液体で、一般にアセチル化剤や脱水剤として使用されます。1852年に塩化ベンゾイルと溶融した酢酸カリウムの反応によって初めて合成されました。
それ以来、無水酢酸は様々な研究や工業用途において極めて重要な有機中間体として台頭してきました。現在では、学術的な合成と工業的な合成の両方で広く利用されています。
無水酢酸はワイン用のブドウ(Vitis vinifera)に微量に含まれていますが、主に工業的に生産されています。
目次
- 1. 無水酢酸の物理的性質
- 2. 無水酢酸の化学反応
- 3. 無水酢酸の製造
- 4. 無水酢酸の用途
- 参考文献
1. 無水酢酸の物理的性質
無水酢酸は、刺激臭を特徴とする無色の液体であり、強い催涙性を有します。無水酢酸に関連する主な物理データを以下に示します。
表1:無水酢酸の物理的性質
| 項目 | 値 |
|---|---|
| 分子式 | (CH3CO)2O |
| 分子量 | 102.09 g/mol |
| 外観 | 無色液体 |
| 密度 | 1.08 g/cm3 |
| 沸点 | 140.1 °C |
| 融点 | -73.1 °C |
| 水への溶解性 | 激しく反応、混和 |
| 臭気 | 刺激臭 |
| 蒸気圧 (25 °C) | 13 mmHg |
| 引火点(密閉式) | 49 °C |
| 発火温度 | 485 °C |
| 屈折率 | 1.392 |
| 粘度 (25 °C) | 1.3 cP |
| 爆発限界 | 2.3 – 10.6% (容量) |
-73.1 °Cの温度で、無水酢酸は固体から液体への相転移(融点)を起こします。一方、101.3 kPaの圧力下では140 °Cで沸騰します(沸点)。
無水酢酸は極性溶媒と混和し、冷アルコールにはゆっくりとした分解を伴いながら溶解します。20 °Cの水に溶解した場合、溶解度は約2.6 wt %であり、徐々に分解プロセスが進行します。
逆に、15 °Cにおいて無水酢酸中への水の溶解度は約10.7 wt %であり、これも同様に徐々に分解する傾向があります。
2. 無水酢酸の化学反応
無水酢酸は幅広い化学反応を示し、脂肪族カルボン酸無水物として広範に研究されてきました。
過去25年間、無水酢酸は数多くの論文や特許で使用されており、特にヒドロキシル基(OH)やアミノ基(NH)のアセチル化における主要なステップとして活用されています。
2.1. アセチル化
ピリジン中の無水酢酸は、ヒドロキシ基、アミノ基、チオール基を含む様々な分子にアセチル基を導入するために使用されます。
2.1.1. O-アセチル化
無水酢酸はアルコールとのエステル化反応に非常に適しており、酢酸では達成が困難または不可能な反応も可能です。この過程で酢酸が遊離します。触媒としては、塩基、強酸、および酢酸ナトリウムのような塩が一般的に用いられます。
無水酢酸とヒドロキシル基との反応の顕著な例としては、アセチルセルロース、アセチルサリチル酸(一般にアスピリンとして知られる)、およびトリアセチン(グリセロールトリアセテート)の生成が挙げられます。
無水酢酸が過酸化水素と反応すると、反応物のモル比に応じて過酢酸または過酸化ジアセチルが生成されます:
(CH3CO)2O + 2 H2O2 → 2 CH3CO3H
(CH3CO)2O + H2O2 → CH3COOH + CH3CO3H
(CH3CO)2O + CH3CO3H → CH3COOOOCOCH3 + CH3COOH
2.1.2. N-アセチル化
NH基を含む化合物をアセチル化すると、次の一般式に従ってアセトアミドが得られます:
RR’NH + (CH3CO)2O → RR’NCOCH3 + CH3COOH
ここで、RおよびR’は水素(H)またはアルキル基を表します。脂肪族アミンは通常、加熱を必要とせずに反応します。例えば、アニリンからはアセトアニリドが生成され、これはその後のニトロ化中の酸化を防ぐ役割を果たします。
N-アセチル化反応は一般にOH基のアセチル化よりも速く進むため、複数の官能基を持つ化合物の部分的なアセチル化が可能です。例として、N-アセチルメチオニン-S-オキシド (1) やN-アセチルアントラニル酸 (2) などのN-アセチルアミノ酸の製造が挙げられます。
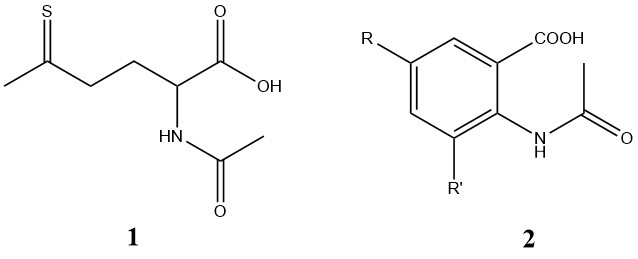
脂肪族および芳香族の両方において、遊離のNH基を持つアミドやカルバミドは無水酢酸を用いてアセチル化できます。
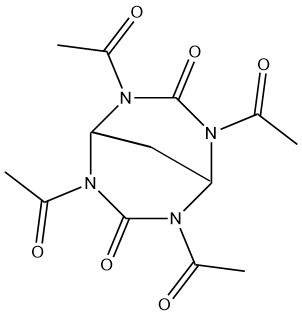
触媒としては硫酸がよく使われます。この反応は、N,N,N’,N’-テトラアセチルエチレンジアミン ((CH3CO)2NCH2CH2N(COCH3)2) や 2,4,6,8-テトラアセチルアザビシクロ[3.3.1]ノナン-3,7-ジオンなどの様々な製品の合成に応用されています。
2.1.3. C-アセチル化
反応性の高いCH結合を持つ化合物は、無水酢酸によってアセチル化を受けることがあり、時には触媒を必要とします。著名な例としては、炭酸カリウムを触媒としたα-シアノアセト酢酸エチル (CH3COCH(CN)COOC2H5) の製造や、無水酢酸とベンゼンのような芳香族炭化水素との間のフリーデル・クラフツ反応によるアセトフェノンの形成が挙げられます。
塩化アルミニウム存在下での2,3-ジメチルブタジエントリカルボニル鉄のアセチル化により、以下の錯体が得られます:
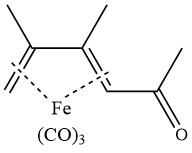
三フッ化ホウ素を触媒としたケトンと無水酢酸の反応は、β-ジケトンの形成をもたらします。
トリアセチルメタンは、酢酸イソプロペニル、無水酢酸、および塩化アルミニウム触媒から直接合成できます。
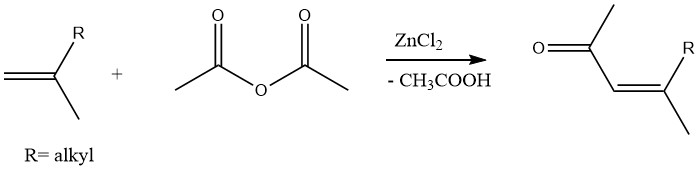
同様に、塩化亜鉛を触媒とした無水酢酸によるオレフィンのアセチル化を通じて、不飽和メチルケトンを製造することができます。
2.1.4. 無機酸のアセチル化
無水酢酸と硝酸の反応は硝酸アセチルを生成し、これは有機化学においてニトロ化剤として頻繁に使用されます。硝酸アセチルは、五酸化二窒素と無水酢酸を用いても合成できます。
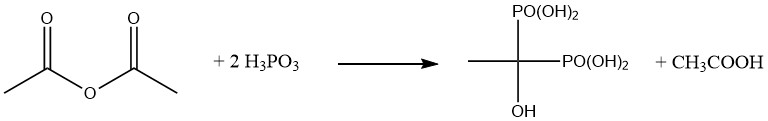
硫酸、スルホン酸、塩酸などの他の強酸も、無水酢酸と混合酸無水物を形成することがあります。無水酢酸を亜リン酸と反応させると、1-ヒドロキシエタン-1,1-ジホスホン酸が生成されます。
2.1.5. 酸化物のアセチル化
三酸化アンチモンは無水酢酸と反応して酢酸アンチモン (Sb(OCOCH3)3) を生成します。三酸化クロムとの同様の反応では酢酸クロミル溶液が得られ、オレフィンや炭化水素の酸化によく利用されますが、時に爆発の危険があるため注意が必要です。
2.1.6. 塩のアセチル化
様々な塩が、対応する遊離酸と同様の方法でカルボン酸無水物と反応します:
Li−C−CR + (CH3CO)2O → CH3CO−C−CR + CH3COOLi
過酸化バリウムを無水酢酸で処理すると、過酸化ジアセチルが生成されます:
BaO2 + (CH3CO)2O → (CH3CO)2O2 + BaO
ビニルケトンを製造する一般的な方法には、ビニルマグネシウムブロミドと無水酢酸の反応が含まれます。
2.1.7. アセトキシシランの製造
無水酢酸はシランと以下の式に従って反応します:
≡Si−X + (CH3CO)2O → ≡Si−OCOCH3 + CH3COX
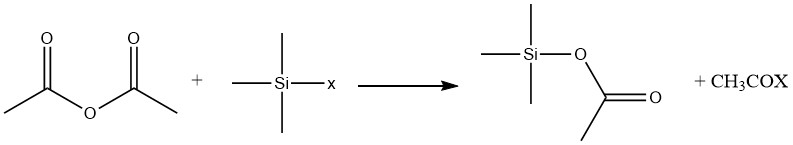
ここで X = H, Cl, OR, NR2 です。
2.1.8. 環開裂を伴う複素環化合物への付加
これらの反応は概念的には上述のものと似ています。例えば、強酸性または強塩基性触媒の存在下でエチレンオキシドからエチレングリコールジアセテートを製造でき、トリオキサンからはオキシメチレンジアセテートを得ることができます。
2.1.9. 炭素-炭素二重結合への酸化的付加
酸化的付加反応により、対応するジアセテートが形成されます。例えば、無水酢酸へのエチレンの付加はエチレングリコールジアセテートを与えます。同様に、ブタジエンは同様のプロセスを経て 1,4-ジアセトキシ-2-ブテンに変換できます。
2.1.10. 混合ジアシル過酸化物の製造
ジアシル過酸化物は、酢酸ナトリウムの存在下で酸素を脂肪族アルデヒドと無水酢酸の混合物と反応させることにより合成できます。
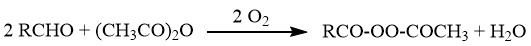
2.1.11. N-オキシドとの反応
N-オキシドとの反応では、特定のN-オキシドの種類に基づいて様々な生成物が得られます。例えば、ピリジン-N-オキシドは2-アセチルオキシピリジンを生成し、4-ピコリン-N-オキシドは4-アセチルオキシメチレンピリジンと3-アセチルオキシ-4-メチルピリジンの混合物を形成します。N-オキシドのポロノフスキー反応は、ホルムアルデヒド、不飽和アルデヒド、および酸アミドの形成をもたらします。
2.1.12. S-オキシドとの反応
無水酢酸を用いたスルホキシドのスルフィドへの還元は、プンメラー反応として知られています。例えば、CH3SORは無水酢酸と反応して CH3COOCH2SR と CH3COOH を生成します。
この反応は、ジメチルスルホキシドまたはテトラメチレンスルホキシドと無水酢酸の混合物を用いて、立体障害のあるものも含めた第一級および第二級アルコールを酸化し、対応するカルボニル化合物を形成するためにも利用されます。
2.1.13. アシラールおよび酢酸ビニルの製造
アルデヒドは酸触媒の存在下で無水酢酸と反応し、アシラールを形成します。アルデヒドがα-水素原子を持つ場合、酢酸の脱離により対応する酢酸ビニルが形成されます。亜鉛の添加は酢酸部位の切断を促進します。このプロセスは、特に2,2-ジクロロ酢酸ビニルの合成に適しています。
2.1.14. 三フッ化ホウ素
無水酢酸および置換無水酢酸は、温水中で分解する三フッ化ホウ素錯体を用いてアセチルケトンに変換できます。
2.2. 脱水反応
無水酢酸は、火薬工業を含む様々な産業で脱水剤として応用されています。その脱水性質の顕著な一例は、ヘキソーゲン(1,3,5-トリニトロヘキサヒドロ-1,3,5-トリアジン)の製造です。
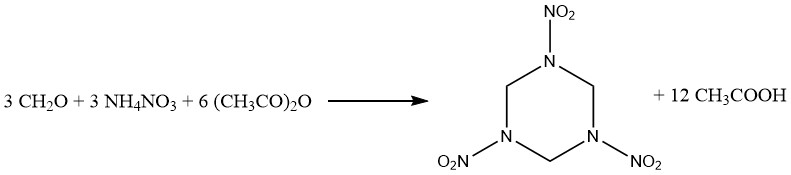
1,2,4,5-テトラヒドロキシ-3,6-dinitroシクロヘキサンのニトロエステルの合成において、無水酢酸はその水結合能力のために採用されています。
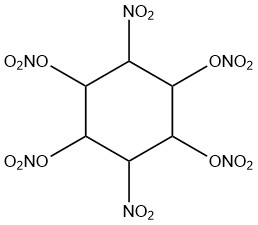
さらに、無水酢酸はアルドキシムを脱水することによるアルキルシアニドの製造に利用されます:
RCH=NOH + (CH3CO)2O → RCN + 2 CH3COOH
加えて、無水酢酸は数多くの環化反応において脱水剤として機能します。
2.3. α-プロトンの反応
ペルキン反応は、ベンズアルデヒドを含む芳香族アルデヒドからα,β-不飽和酸を合成するために広く採用されている方法です。この反応は通常、酢酸カリウムまたは酢酸ナトリウムの存在下で行われます。また、シンナマル酢酸の製造にも使用されます。
同様の反応には、無水酢酸と酸化剤を使用する酸化的カルボキシメチル化や、長鎖アルケンを対応するカルボン酸誘導体に変換する反応などがあります。
2.4. 単一のカルボニル基の反応
特定の場合において、無水酢酸中のカルボニル基の一方のみが反応に関与することが可能です。例えば、塩基の存在下で無水酢酸がシアン化水素と反応すると、化合物 (3) を形成します。同様に、グリニャール試薬 (RMgBr) の存在下では、無水酢酸は化合物 (4) を与えます。
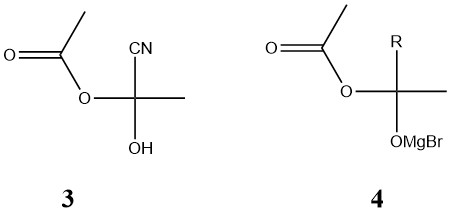
2.5. シルバーケテニドの製造
酢酸銀と無水酢酸を室温でピリジンの存在下で反応させると、シルバーケテニドのピリジン錯体が形成されます。過剰の無水酢酸を用いた場合、得られた混合物をピリジンと酢酸の分留に供することで、シルバーケテニドを単離することができます。
3. 無水酢酸の製造
歴史的に、無水酢酸の最も古い製造方法は、酢酸ナトリウムを過剰の塩化チオニル、塩化スルフリル、または塩化ホスホリルなどの無機塩化物で変換することでした。
このプロセスでは、酢酸ナトリウムの半分が塩化アセチルに変換され、それが残りの酢酸ナトリウムと反応して無水酢酸を形成します。
別の発展形として、塩化アルミニウムの存在下で酢酸をホスゲンと反応させる方法があり、これにより連続運転が可能となりました:
2 CH3COOH + COCl2 → (CH3CO)2O + 2 HCl + CO2
過去に利用された他の2つの方法には、塩化亜鉛のような酸触媒の存在下でエチリデンジアセテートを分解してアセトアルデヒドと無水酢酸を形成する方法や、パラジウム(II)触媒上で酢酸ビニルを酢酸と反応させてアセトアルデヒドと無水酢酸を形成する方法がありました。しかし、これらのプロセスはもはや工業的な重要性を持ちません。
現在、無水酢酸の製造は主にケテン法またはアセトアルデヒドの酸化のいずれかを通じて行われています。また、酢酸メチルのカルボニル化(ハルコン法)として知られる別の方法が1983年に導入されました。
西欧では、無水酢酸の約77%がケテン法で製造され、23%がアセトアルデヒドの酸化で製造されています。
米国では、テネシー・イーストマン工場でのハルコン法の導入以来、無水酢酸の25%がこの方法で製造され、75%がケテン法で製造されています。
3.1. ケテン法による無水酢酸の製造
ケテン法は2つのステップを含みます:酢酸の熱分解によるケテンの形成と、それに続くケテンと酢酸の反応による無水酢酸の生成です。全体の反応は以下のように要約されます:
- 酢酸の熱分解:
CH3COOH → CH2=C=O + H2O (ΔH = 147 kJ/mol) - ケテンと酢酸の反応:
CH2=C=O + CH3COOH → (CH3CO)2O (ΔH = -63 kJ/mol)
ケテンと水を生成するための酢酸の熱分解は、微量のリン酸触媒の存在下、700-750 °Cの温度で高温の酢酸蒸気を加熱することによって行われます。
反応器の圧力は通常、ケテンが酢酸や水と反応する前に単離できるように減圧されます。分解プロセスは、シクロマール(Sicromal)などの高度に耐熱性のある鋼合金製のコイルを備えたマルチコイル反応器で行われます。
ケテン法は、希望する生産能力に応じて複数のステップと機器構成を含みます。小規模な操業では別々の予熱炉と分解炉が利用されますが、中規模の炉はしばしばガスまたは石油で加熱される単一チャンバー炉として建設されます。大規模な炉は、3つまたは4つのチャンバーシステムと部分的なガス流を用いて効果的に機能します。
酢酸の熱分解後、得られたケテンを酢酸と反応させて無水酢酸を生成します。この反応には、スクラバー法とワッカー法の2つのプロセスが一般的に使用されます。
スクラバー法では、ラシヒリングを充填したスクラバー内で循環する氷酢酸によってケテンを吸収させます。ワッカー法では、ケテンを液封ポンプに送り込み、制御された温度と圧力下で酢酸と反応させます。
反応から得られた粗製無水物は、さらに蒸留によって精製されます。連続蒸留と回分蒸留の両方の方法が使用されます。無水物の純度は通常、回分蒸留で約99%ですが、減圧下で操作することで改善可能です。
100 kgの無水酢酸を製造するには、再濃縮された希酢酸を考慮して約122 kgの酢酸が必要です。プロセスの収率は、約75%の分解率において96%を超えます。
3.2. アセトアルデヒドの酸化による無水酢酸の製造
無水酢酸は、アセトアルデヒドの液相酸化によって直接製造することもできます。このプロセスでは、酸素とアセトアルデヒドから形成された過酢酸が、2番目のアセトアルデヒド分子と反応して無水酢酸と水を生成します。
効率的な冷却と適切な触媒の使用が、このプロセスでは極めて重要です。マンガンと銅、コバルトとニッケル、または高級脂肪酸のコバルト塩と銅塩などの金属塩の組み合わせが一般的に触媒として使用されます。
反応温度を維持し、無水酢酸の急速な加水分解を防ぐために、プロセスは通常40 °Cから60 °Cの間で操作されます。反応の放熱性が高いため効果的な冷却が必要であり、水と共沸混合物を形成する酢酸メチルや酢酸エチルのような低沸点溶媒の添加が、反応混合物からの水の分離を助けます。実際には、アセトアルデヒドと酢酸エチルの混合物を、酢酸コバルトおよび酢酸銅触媒の添加により酸化します。
3.3. 酢酸メチルのカルボニル化による無水酢酸の製造
無水酢酸を製造する従来のプロセスは酢酸の熱分解を含み、多大なエネルギーを必要とします。しかし、モンサントによる酢酸製造プロセスや酢酸メチルのカルボニル化などの代替プロセスが開発されました。
酢酸メチルをカルボニル化して無水酢酸を形成する方法は1973年にハルコン(Halcon)によって特許を取得し、1983年に最初のプラントが稼働しました。このプロセスでは、160-190 °Cの温度範囲および2-5 MPaの一酸化炭素分圧下、液相で酢酸メチルをカルボニル化します。
ヨウ化物や他のヨウ素含有物質によって活性化されたロジウムやニッケル化合物を含む様々な触媒を使用できます。ロジウム触媒はニッケル触媒よりも高い活性を示し、両触媒とも95%以上の選択性を示します。合成に使用される一酸化炭素に数パーセントの水素を添加すると、触媒の活性と寿命が向上します。
ハルコン法(図1)の例では、乾燥した酢酸メチルをハステロイ張りの反応器に連続的に供給し、触媒混合物の存在下175 °Cでカルボニル化します。反応中に発生した熱は熱交換によって除去され、酢酸メチルの予熱や低圧蒸気の発生に利用されます。未反応の一酸化炭素は回収・再循環されます。粗製無水物は3つの連続したカラムでの蒸留を通じてさらに精製され、最終的なカラムで純度99%の無水酢酸を生成します。
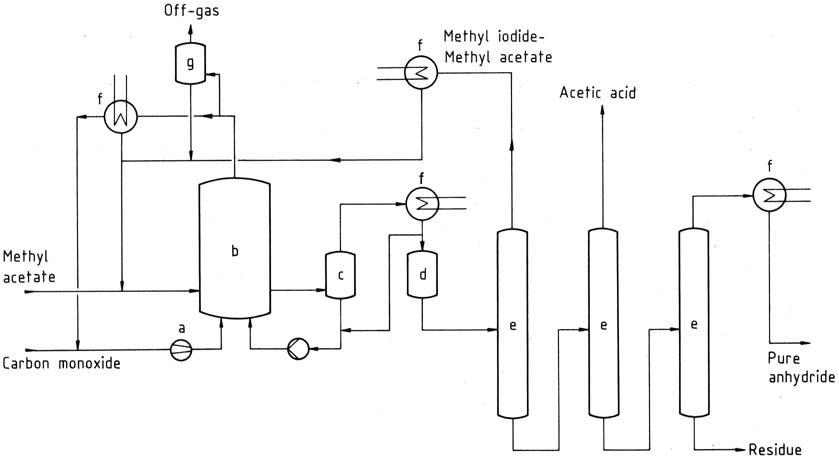
a) 圧縮機、b) カルボニル化反応器、c) 蒸発器、d) 吸着器、e) 蒸留塔、f) 凝縮器、g) スクラバー
これらの代替プロセスは、エネルギー消費や原料利用の面で従来の熱分解ルートに対して利点があり、石油以外の供給源(石炭など)からの無水酢酸の製造を可能にします。
4. 無水酢酸の用途
無水酢酸はアセチル化剤および脱水剤の両方として使用されます。一つの顕著な用途は大スケールでのセルロースのアセチル化ですが、他にも無水酢酸が採用されている分野は数多くあります:
- ポリ(メチルアクリルイミド)硬質フォーム: アミド基からイミド基への変換中に遊離するアンモニアの結合剤として機能します。
- アセチル化プラスチック助剤: トリアセチン、アセチルクエン酸トリブチル、およびアセチルリシノール酸エチルなど。
- 火薬製造: 特にヘキソーゲンの製造において。
- ブレーキ液: 特定のタイプのブレーキ液の製造。
- 掘削流体助剤: 石油・ガス掘削用助剤の製造。
- 洗剤工業: 特にテトラアセチルエチレンジアミンのような低温漂白活性化剤の製造において。
- 染色工業: 硝酸との組み合わせでニトロ化剤として使用され、溶媒特性と脱水特性を活用します。
- 有機中間体: 塩化クロロアセチル、過酸化ジアセチル、高級カルボン酸無水物、酢酸塩、および三フッ化ホウ素錯体などの調製。
- 医薬品: アセチルサリチル酸(アスピリン)、p-アセチルアミノフェノール、アセトアニリド、アセトフェナセチン、テオフィリン、塩化アセチルコリン、スルホンアミド、ホルモン、ビタミン、およびX線造影剤である2,4,6-トリヨード-3,5-ジアセチルアミド安息香酸など。
- 食品工業: 主に動物および植物脂肪のアセチル化による溶解性の調整、アセトステアリン(可食性包装材料)の製造、および植物油の清澄化。
- 香料・フレグランス: エステル類やクマリンの製造に使用されます。
- 除草剤: メトラクロール(Dual)やアラクロール(Lasso)など。
参考文献
- Acetic Anhydride and Mixed Fatty Acid Anhydrides; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a01_065
- https://lotus.naturalproducts.net/compound/lotus_id/LTS0216280