硝酸アンモニウム:性質、製造および用途
硝酸アンモニウム(NH4NO3)は、アンモニウムイオン(NH4+)と硝酸イオン(NO3–)からなる化学化合物です。無色で結晶性の物質であり、農業、工業、爆薬など、さまざまな用途で広く使用されています。
硝酸アンモニウムは重要な化学化合物です。その主な製造方法は、硝酸とアンモニアの反応によるもので、主に高品質な肥料として利用されています。直接施用される肥料として、この化合物は世界の窒素肥料消費量の約24%を占めています。
硝酸アンモニウムは、さまざまな配合肥料や複合肥料の不可欠な成分であり、世界の人々の栄養ニーズに応える上で重要な役割を果たしています。
農業用途以外では、硝酸アンモニウムは酸化剤として使用され、数多くの爆薬組成物の主要な一部を構成しています。
目次
1. 硝酸アンモニウムの物理的および化学的性質
分子量80.05 g/molの硝酸アンモニウムは、無色の塩として存在します。20 ℃における密度は1.725 g/cm³であり、0から31 ℃の温度範囲における比熱容量は1.70 J/g・Kです。
融点は169.6~170 ℃です。アンモニアと硝酸から硝酸アンモニウムを合成するプロセスは、以下の反応式に示されるように、非常に強い発熱反応であることが特徴です。
NH3 + HNO3 → NH4NO3 ΔH = -146 kJ/mol
32.3 ℃で起こる相転移は、硝酸アンモニウムを含む肥料の保管において重要な意味を持ちます。この相転移を繰り返し経験すると、密度差によって肥料粒子が劣化し、最終的に崩壊を招く可能性があります。
硝酸アンモニウムは水に非常によく溶け、吸湿性を示します。そのため、輸送や保管の際には湿気の吸収を防ぐための予防措置が必要です。
硝酸アンモニウムが水に溶解する際は熱を吸収するため、塩化ナトリウムと氷を用いたものと同様の寒剤として有用です。
硝酸アンモニウムは、さまざまな非水溶媒にも溶解します。液体NH3は溶媒として機能し、本塩を溶解するとともに容易にNH3を吸収して、「ダイバース液体(Divers liquid)」として知られる溶液を生成します。
濃度50~70重量%の硝酸アンモニウム水溶液は、NH3を激しく吸収し、ガスからのNH3ストリッピング剤として機能します。これらの溶液は、過リン酸石灰のアンモニア処理にも利用されます。
メタノール中では、硝酸アンモニウムは30 ℃で約20%、60 ℃で約40%の溶液を形成します。エタノールへの溶解度は20 ℃で約4%ですが、アセトンにはさらに溶けにくくなります。エーテルには不溶です。
強力な酸化剤である硝酸アンモニウムは、標準的な温度および圧力条件下では安定しています。しかし、170 ℃以上に加熱するとガスへと分解します。この分解は、少量の塩素や遊離酸によって加速されます。
2. 硝酸アンモニウムの製造
硝酸アンモニウムは、アンモニアと硝酸の反応によって製造されます。また、窒素・リン(NP)肥料および窒素・リン・カリウム(NPK)肥料の製造工程においても生成されます。
この生成は、リン鉱石の硝酸による分解過程で起こり、得られた塩が肥料の成分となります。
欧州地域では、硝酸カルシウム、NH3、およびCO2の反応を用いてNH4NO3が製造されています。
2.1. アンモニアと硝酸から
硝酸アンモニウムは、気体アンモニアと硝酸の反応によって形成され、NH4NO3 1モルあたり100~115 Jの熱放出が特徴です。さまざまな製造プロセスにおいて、この発熱エネルギーは水の一部または完全な蒸発に利用されます。
圧力条件や使用する硝酸の濃度に応じて、95~97%の硝酸アンモニウム溶液を得ることが可能です。
中和プロセスの間、局所的な過熱、窒素損失、および硝酸アンモニウムの分解を防ぐために、反応器内で反応物を迅速かつ徹底的に混合することが不可欠です。
従来の設備では、ウーデ法(Uhde process)やSBA法(Société Belge de l’Azote process)などの手法が用いられており、これらは反応温度が比較的低く、腐食の影響を受けにくいという特徴があります。
反応熱を最適に活用することは、加圧中和によって達成されます。
UCB法(図1)は、加圧反応器内に熱交換器を備えており、反応熱の一部を利用して蒸気を発生させます。予熱されたアンモニアと52~63%のHNO3が反応器の底部に注入され、約0.45 MPa(4.5 bar)の圧力と170~180 ℃の温度で運転されます。
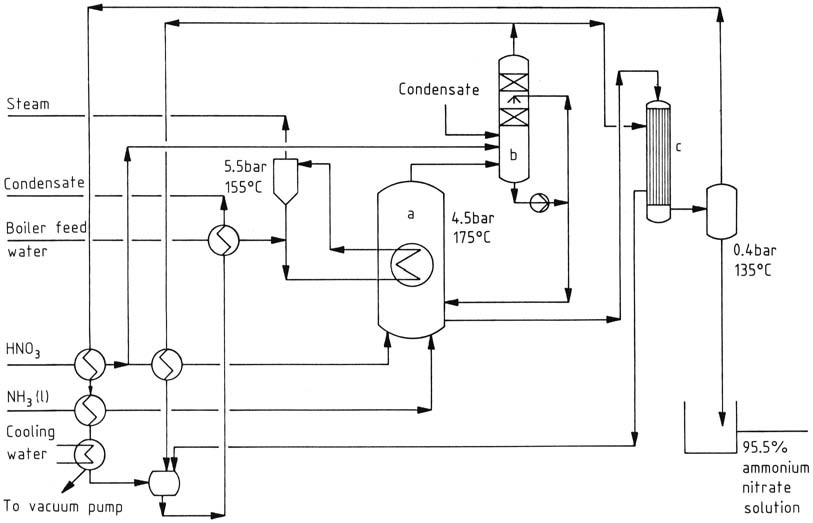
得られた75~80%のNH4NO3溶液は、流下膜式蒸発器によって95%まで濃縮されます。ここで、反応熱により硝酸内の水分からプロセス蒸気が発生します。
このプロセス蒸気は、ボイラー給水や硝酸の予熱、および流下膜式蒸発器の運転に使用されます。さらに、反応熱の一部で純粋な蒸気が生成され、これは他の用途のために蒸気系へ送ることができます。
pH範囲を3~5に維持することでプロセス蒸気への窒素損失を軽減し、運転条件は過剰なプロセス蒸気の蓄積を防ぐように細かく調整されます。
もう一つの加圧プロセスはスタミカーボン法(図2)であり、分離器に繋がるループ反応器を採用しています。反応溶液の循環は、システム内で発生する熱によって維持されます。
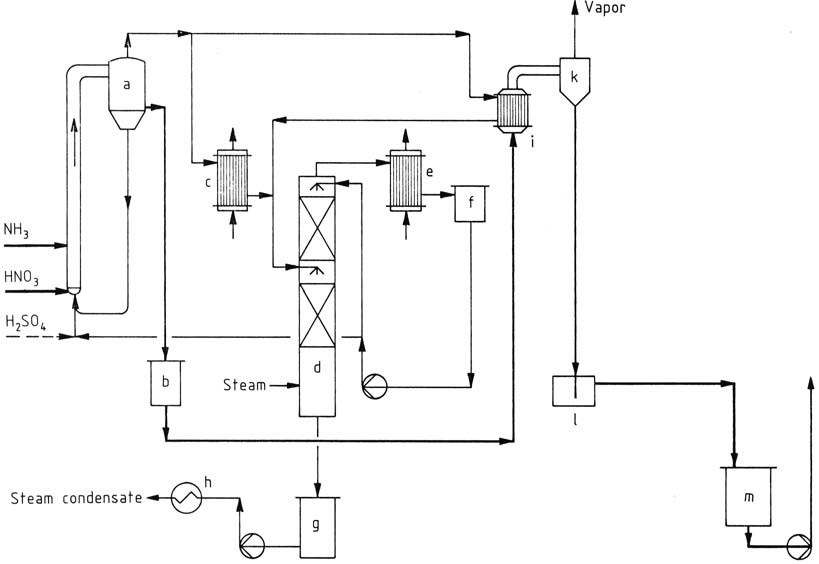
a) 中和器; b) 中間タンク; c) 余剰蒸気凝縮器; d) アンモニアスクラバー; e) 凝縮器; f) 希アンモニア溶液タンク; g) 凝縮水タンク; h) 冷却器; i) 蒸発器; k) 分離器; l) シールポット; m) 95%硝酸アンモニウム溶液貯蔵タンク
ループの下端から、予熱された硝酸(60重量%)、アンモニア、および少量の硫酸が導入されます。0.4 MPa(4 bar)および178 ℃で運転され、反応器から濃度78%の硝酸アンモニウム溶液が得られます。
分離器の頂部から取り出された蒸気は、真空蒸発器でNH4NO3溶液を95%に濃縮するために使用されます。さらに、過剰な蒸気は凝縮され、回収されたアンモニアは反応器へと再循環されます。
さらに98~99.5%への濃縮は、新鮮な蒸気を用いた後続の蒸発器で行われ、中和および蒸発の間、硝酸アンモニウム溶液の温度は180 ℃以下に厳密に維持されます。
NSM/ノルスク・ハイドロ加圧法(図3)は、予熱されたアンモニアと硝酸を使用することを特徴としています。0.4~0.5 MPa(約4.5 bar)の圧力と170~180 ℃の温度で運転され、この方法により70~80%の溶液濃度が得られます。
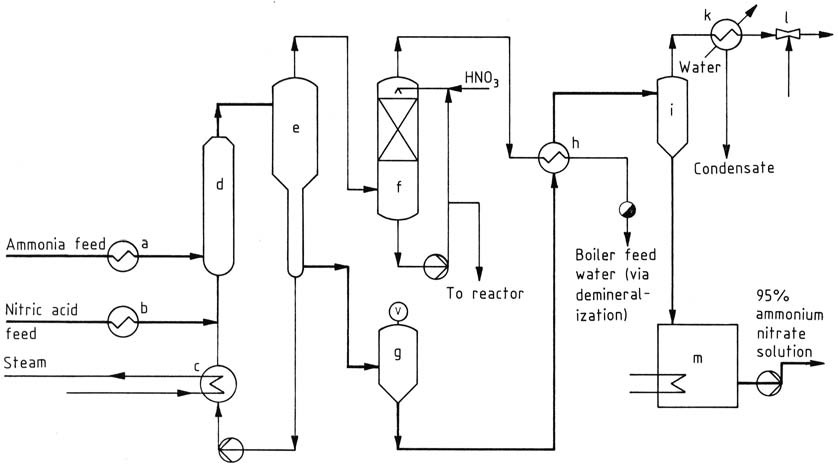
a) アンモニア蒸発器/過熱器; b) 硝酸予熱器; c) ボイラー; d) 反応器; e) 反応器分離器; f) スクラバー; g) フラッシュタンク; h) 蒸発器; i) 分離器; k) 凝縮器; l) エジェクター; m) タンク
強制循環とサーモサイフォン効果の組み合わせにより、溶液は反応器内を駆動されます。反応熱の一部は外部ボイラー内での純粋蒸気生成に寄与し、一部は反応器内の水を蒸発させて、硝酸アンモニウム溶液を95%まで濃縮するためのプロセス蒸気を発生させます。
アンモニア損失の最小化は、循環する硝酸アンモニウム溶液に加えられた硝酸によるプロセス蒸気の洗浄によって達成されます。最終段階である99.5%までの濃縮は、専用の真空蒸発器内で蒸気を用いて行われます。
米国では、ステンゲル法(Stengel process)により無水硝酸アンモニウムの直接製造が可能です。予熱されたアンモニアと約58%の硝酸が、0.35 MPa(3.5 bar)および240 ℃で作動する充填層式縦型管状反応器に導入されます。
遠心分離器内での真空膨張後、得られたNH4NO3と蒸気の混合物は熱風によるストリッピングを受け、99.8%のNH4NO3溶融物が排出されます。
この溶融物はその後、冷却されたスチールベルト上で固化され、破砕または造粒によってさらに加工されます。蒸気の除去はこのプロセスの頂部で行われます。
これらすべてのプロセスにおいて、目的のpH範囲を注意深く維持することが重要です。170 ℃以下の反応温度では、pHを2.4~4の間に保つことで窒素損失を最小限に抑えます。
より高温になり分解の可能性が高まる加圧型中和器では、4.6~5.4というわずかに高いpH範囲が必要になります。
2.2. 硝酸カルシウム四水和物の転換
オッダ法(Odda process)では、リン鉱石の硝酸分解によってニトロリン酸肥料が製造され、副産物として硝酸カルシウム四水和物(Ca(NO3)2・4H2O)が大量に生成されます。
ニトロリン酸肥料の生産が増加する一方で、硝酸カルシウムの需要は減少しています。数年前に導入された方法では、硝酸カルシウム四水和物をアンモニアと二酸化炭素で処理し、以下の化学反応によって硝酸アンモニウムと炭酸カルシウムを形成します。
Ca(NO3)2・4 H2O + 2 NH3 + CO2 → 2 NH4NO3 + CaCO3 + 3 H2O ⇒ ΔH = -126 kJ/mol
この反応で放出される熱は、付随するすべての水を完全に蒸発させるのに十分な大きさです。しかし、高温下では好ましくない平衡条件が支配的であるため、この手順への直接的なアプローチは不可能です。
BASF法は、Ca(NO3)2と(NH4)2CO3の反応に伴う除熱を分離しています。この方法では、NH3とCO2が循環するNH4NO3溶液内に溶解され、発生した熱は効率的に管理されます。
同時に、硝酸カルシウム四水和物は別のNH4NO3溶液に溶解されます。その後、これら2つの溶液を混合し、約50 ℃で反応させることで、発熱を最小限に抑えます。
沈殿する方解石(カルサイト)の粒径は、反応物の導入方法を通じて制御できます。反応後、濃度約65%の得られたNH4NO3溶液は、ベルトフィルターを使用してCaCO3から分離され、その後蒸発によって濃縮されます。
残留するCaCO3には微量のアンモニウム化合物やリン酸塩が含まれていることがありますが、これは石灰窒素硝酸アンモニウムの製造に特に適しています。転換前に硝酸カルシウムを調製することで、比較的純粋なCaCO3の生成が可能となります。
硝酸カルシウムの直接転換を可能にすると同時に反応熱に対処する別の独自のアプローチとして、ヘキスト社(Hoechst)は特殊な縦型反応器を開発しました。
この反応器設計では、気体CO2が下部セクションから導入され、アンモニアの導入は3つの異なるゾーン内で行われ、各ゾーンは水循環によって積極的に冷却されます。
3. 硝酸アンモニウムの用途
硝酸アンモニウム(AN)は、主に肥料として、純粋な形態、希釈された形態、または多成分混合物中の成分として使用されます。液体肥料としては尿素とともに配合され、米国、東欧、フランスなどの地域で重要視されています。
米国、英国、フランスの農業部門では、窒素含有量が33.5%以上の硝酸アンモニウムが広く採用されています。米国では32.5% Nを含む肥料も利用されています。
ドイツ連邦共和国では、硝酸アンモニウムは石灰、ドロマイト、硫酸アンモニウム、またはカリ(加里)とともに混合物に組み込まれており、特に石灰窒素硝酸アンモニウム(CAN)に重点が置かれています。
3.1. 石灰窒素硝酸アンモニウム(CAN)
硝酸アンモニウム溶液(約95~97%)は、粉砕された石灰石由来、または硝酸カルシウムの転換によって得られた微細な炭酸カルシウムと組み合わせることで、粒子状(顆粒)に変換できます。
後続の工程には、乾燥、冷却、スクリーニング、および固結防止のための処理が含まれます。硝酸アンモニウムと石灰石の反応によって生じる吸湿性の硝酸カルシウムの形成は、(NH4)2SO4、MgSO4、FeSO4などの添加剤を加えることで防止されます。
ドイツでは、石灰窒素硝酸アンモニウムの窒素含有量は、当初の20.5% Nから現在の27.5% Nまで段階的に引き上げられており、欧州経済共同体(EEC)の規制で定義された上限である28% Nを遵守しています。
3.2. 硫酸硝酸アンモニウム
この硫酸塩・硝酸塩混合肥料は、約95%の硝酸アンモニウム溶液に硫酸アンモニウムを加えるか、HNO3-H2SO4混合液をアンモニアで中和することによって作られます。
造粒された製品は性質上わずかに吸湿性があり、複塩 2NH4NO3・(NH4)2SO4 と少量の硫酸アンモニウムの混合物で、硝酸アンモニウム含有量が45%未満の場合、窒素含有量は26% Nとなります。
時間の経過とともに、この混合物はさらなる反応によって硬化する傾向があります。このような硬化は、Mg、Fe、またはAlの塩を導入することで回避できます。
3.3. カリ硝酸アンモニウム
カリ硝酸アンモニウムは硫酸硝酸アンモニウムと同様の方法で合成され、カリウム塩(塩化物または硫酸塩)を加えることで、20–0–20(N–P2O5–K2O)のような肥料が得られます。
3.4. ニトロマグネシア
ニトロマグネシアは、硝酸アンモニウム、硫酸アンモニウム、およびドロマイト、炭酸マグネシウム、硫酸マグネシウムなどのマグネシウム化合物に由来する肥料です。一例として、約20% N、8% MgO、および通常0.2% Cuを含む配合があります。
3.5. その他の用途
硝酸アンモニウムは、爆発温度が比較的低いため、鉱業で使用される安全爆薬の主要成分として機能します。NaClと組み合わせることで爆発温度が下がり、炭鉱ガスの引火リスクを軽減します。
一部のケースでは、安全爆薬は補完的な塩ペア NaNO3 + NH4Cl → NH4NO3 + NaCl に基づいて配合されます。
鉱業(岩石爆薬)などの用途でより大きな爆発力を得るためには、約6%の軽油(ディーゼルオイル)を含む多孔質プリル状硝酸アンモニウムが使用されます。
少量の硝酸アンモニウムは、亜酸化窒素の製造に関与しています。この場合、塩は有機物質、鉄、塩化物、硫酸塩を含まず、99.5% NH4NO3 という極めて高い純度である必要があります。
4. 安全性
硝酸アンモニウムは、通常の状態では安定していますが、高温下では以下のような特異な分解反応を起こします:
1. 169 ℃以上での吸熱的解離とpH低下:
NH4NO3 → HNO3 + NH3 ΔH = +175 kJ/mol
2. 200 ℃での注意深い加熱によるN2Oの発熱的脱離:
NH4NO3 → N2O + 2 H2O ΔH = -37 kJ/mol
3. 230 ℃以上でのN2およびNO2の発熱的脱離:
4 NH4NO3 → 3 N2 + 2 NO2 + 8 H2O ΔH = -102 kJ/mol
4. 窒素と酸素の発熱的脱離による爆轟:
NH4NO3 → N2 + 1/2 O2 + 2 H2O ΔH = -118.5 kJ/mol
純粋な硝酸アンモニウム、濃縮された熱溶液、特定の混合物、および非安定化肥料形態はすべて、衝撃波によって爆轟する可能性のある爆発物となり得ます。放出される熱量はヘキソーゲン(RDX)などの化合物と比較すれば比較的小さいものの、大量に保管することは重大なリスクを伴います。水素イオン、塩化物、重金属などの要因は分解を触媒する可能性があります。
汚染された、または固まった硝酸アンモニウムの加熱は特に危険です。ワックスでコーティングされた肥料用硝酸アンモニウムが火災によって爆発した1947年のブレストおよびテキサスシティの惨事を受けて、現在の規制では可燃性物質は0.2%または0.4%に制限されています。
ドイツでは、作業材料法(Working Materials Act)が硝酸アンモニウムの保管、積み込み、および輸送に関するプロトコルを規定しています。例えば、爆轟の可能性がある硝酸アンモニウムの保管は、特別に装備された施設内での少量に制限されています。
同様の規則は他の欧州諸国にも適用されますが、米国、フランス、ノルウェー、英国では、特定の条件下で比較的大きな保管が許可されています。
ドイツでは、肥料用途(石灰窒素硝酸アンモニウム)として、石灰石粉末やドロマイトなどの不活性材料が硝酸アンモニウムに加えられます。最大80%の硝酸アンモニウム、最大0.4%の可燃成分、および少なくとも18%のマグネシウムまたは炭酸カルシウムを含むこれらの肥料は、非爆轟性と見なされます。
安全に関するヒントは以下の通りです:
- 保管中に固化した硝酸アンモニウム含有製品を爆破(衝撃で崩すこと)しないでください。
- 硝酸アンモニウム製品は、酸化されやすい物質や可燃物から離して保管してください。
- 硝酸アンモニウムを加熱する際は、少量で行い、触媒を避けてください。
参考文献
Ammonium Compounds; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a02_243