臭素:反応、製法、および用途

臭素は、高密度で暗赤色の液体であり、強い発煙性を持つとともに、高い腐食性と催涙性を備えています。臭素の臭気は非常に刺激的で、空気中に 1 ppm 存在するだけで感知できるほどです。
臭素の色は温度に依存し、20 K では黄橙色ですが、温度上昇に伴い橙赤色、赤褐色へと変化し、融点付近ではほぼ黒色になります。液体状態では暗赤色を保ちますが、その蒸気は一般に橙色から赤褐色を呈します。
1824年、フランスのモンペリエ近郊にある塩湿地の植物を研究していた A. J. バラール(Balard)によって発見されました。研究中、彼は食塩から得られた母液の入った皿の中に、結晶化した硫酸ナトリウムの堆積物を観察しました。
廃棄液の潜在的な用途を調査していたバラールは、塩素を飽和させると蒸留可能な新しい赤色の液体が生成されることを発見しました。
目次
1. 臭素の化学反応
臭素の化学反応の多くは、その強力な酸化特性に起因します。臭素の電子親和力は、他の多くの化学的性質と同様に、塩素とヨウ素の中間に位置します。
臭素は中程度の強さの酸化剤として作用し、起電力系列における位置に従って、塩素によって酸化され単体の臭素を生成します。
水中で臭素は臭化物イオンに還元されますが、その際の還元剤は水または残りの臭素のいずれかです。水が還元剤となる場合は、以下の反応式に示すように酸素が生成されます:
2 Br2 + 2 H2O → 4 H+ + 4 Br– + O2 E0298 = +0.25 V
臭素はシアン化水素と反応して臭化シアンを形成します:
Br2 + HCN → BrCN + HBr
炭酸塩は臭素と反応し、その結果、臭化物塩と臭素酸塩を生成します:
3 Br2 + 3 Na2CO3 → 5 NaBr + NaBrO3 + 3 CO2
臭素は二酸化硫黄を硫酸へと酸化させることができ、それは以下の反応式で示されます:
Br2 + SO2 + 2 H2O → 2 HBr + H2SO4
臭素は赤リンや他のリン化合物と反応し、以下のようにリン酸と臭化水素を生成します:
3 Br2 + 2 P + 6 H2O → 6 HBr + 2 H3PO3
H3PO3 + Br2 + H2O → H3PO4 + 2 HBr
H3PO3 + Br2 + NaOH → NaH2PO4
アンモニア、ヒドラジン、亜硝酸塩、アジ化物などの窒素を含む化合物も臭素によって酸化され、これらの反応ではしばしば単体窒素が生成されます。
高温下では、臭素は水素と直接反応して臭化水素を生成します。これは、加熱した木炭や微粉砕された白金金属などの触媒を用いた HBr の商業的生産の基礎となっています。
臭素は多くの金属と反応して臭化物を生成します。ナトリウムはナトリウム蒸気の存在下で激しく反応し、カリウムやセシウムは臭素と爆発的に反応します。
アルミニウムやチタンも臭素に対して極めて高い反応性を示し、アルミニウムは反応時に発光します。一方、マグネシウム、銀、ニッケル、鉛は表面が臭化物で覆われるため、それ以上の反応が進行しなくなります。
鉛の保護被膜特性により、鉛は臭素を保持する容器の材料として有用です。同様にニッケル、タンタル、ハステロイC、モノエル、その他の銅合金も利用されます。
臭素による金属の腐食において水分は重要な要因であり、これはおそらく加水分解生成物である臭化水素酸や次亜臭素酸によるものです。
水分含有量が 40 ppm 以下であれば、臭素の輸送にニッケル容器を使用できますが、臭素蒸気にさらされる計器やゲージに水銀を使用してはなりません。
乾燥した臭素は鉄とゆっくり反応して臭化鉄(III)の保護層を形成しますが、湿っている場合は水和した臭化鉄の混合物が生成され、これは鉄の表面に付着しません。
銅、マンガン、クロム、アンチモン、コバルト、カドミウム、ビスマスなど、他のいくつかの重金属も臭素と反応しますが、反応の進行に高温を必要とする金属もあります。
1.1. アルケンおよびアルキンの臭素化
臭素は不飽和化合物に容易に付加することができます。これらの反応は通常、置換副反応を防ぐために低温で行われます。触媒は通常必要ありませんが、高温や紫外線照射によって反応を加速させることができます。
不飽和化合物の臭素化を通じて、臭化エチレン、四臭化アセチレン、2,3-ジブロモプロパノール、ヘキサブロモシクロデカン、テトラブロモビスフェノールA ビス(2,3-ジブロモプロピルエーテル)など、多くの重要な商業製品が得られます。
1.2. 芳香族化合物の臭素化
芳香族化合物の臭素化は、(1)付加、(2)側鎖への置換、(3)芳香環への置換、という3種類の反応を通じて起こります。
芳香族の二重結合への臭素の付加は、光触媒下では通常遅い反応ですが、塩素を加えることで反応速度を上げることができます。芳香族側鎖の臭素化は、通常、自由基(ラジカル)反応を通じて進行します。
芳香環への親電子置換反応は、芳香族臭素化において最も重要なタイプです。触媒の存在下で、臭素は芳香族化合物と反応し、以下の反応によって臭化アリールと臭化水素を生成します:
ArH + Br2 → ArBr + HBr
芳香族臭素化に適した触媒には、アルミニウム、鉄、亜鉛、アンチモンのハロゲン化物などのルイス酸が含まれます。フェノール、アニリン、芳香族エーテルのような活性化された芳香族化合物は、触媒なしで臭素化できます。
逆に、電子吸引基を持つ非常に強く不活性化された芳香族化合物は、硫酸と硝酸の存在下で臭素化を受けることができます。
系内で臭化水素から発生させた臭素は、芳香族置換反応においてより効率的に使用されます:
ArH + HBr + Cl2 → ArBr + 2 HCl
あらかじめ調製された塩化臭素(BrCl)もこの目的で使用できます。BrCl を使用する置換反応は、一般に臭素単独を使用する場合よりもはるかに高速です。
1.3. ラジカル臭素化
臭素は、自由基(ラジカル)が関与する連鎖反応メカニズムを通じて、飽和炭化水素や芳香族化合物のアルキル側鎖と容易に反応します。反応は以下のステップで進行します:
Br2 → 2 Br•
RH + Br• → R• + HBr
R• + Br2 → RBr + Br•
反応の開始には臭素分子の解離が必要であり、これは熱、光、または過酸化物開始剤によって達成されます。塩素と比較して臭素原子は反応性が低く、水素引き抜きステップが吸熱的であるため、反応速度は比較的遅くなります。
それにもかかわらず、臭素原子は高い位置選択性を示します。例えば、n-ブタンの臭素化では、二級水素原子は一級水素原子よりも 82 倍速く置換されます。芳香族側鎖の臭素化は、アルカンの臭素化よりもはるかに高速です。
1.4. 臭化水素の製造
臭化水素は、医薬品、染料、香料、写真用化学品、および他の多くの化学化合物を含む、さまざまな有機および無機臭化物の製造における重要な中間体です。
臭化水素を調製する一般的な商業的方法は、水素と臭素の直接的な気相反応を伴います。これは、密閉されたバーナー内で自立炎を維持することにより、触媒なしで達成できます。
Br2 + H2 → 2 HBr + 熱
実験室では、臭化ナトリウムまたは臭化カリウムの溶液をリン酸または希硫酸(5.8 M)で蒸留することによって臭化水素を発生させることができますが、より濃い硫酸を使用したり反応温度を 75 ℃以上に上げたりすると、最初に形成された HBr が気体の臭素(Br2)に酸化されるため効果的ではありません。
あるいは、リン酸による臭素の還元によっても臭化水素を発生させることができます:
H3PO3 + Br2 + H2O → H3PO4 + 2 HBr
1.5. 臭素キャリアを用いた臭素化
選択性を必要とする臭素化反応では、臭素錯体やブロモイミドが利用されます。実験室での臭素化において、N-ブロモスクシンイミド(NBS)は最も一般的に使用される臭素キャリアです。
NBS はラジカルアリル位臭素化において独自の用途を持っています:
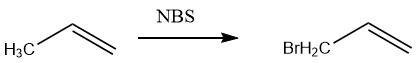
化学反応に有効な他の臭素キャリアには、ジブロモジメチルヒダントイン、ジオキサンジブロミド、ピリジン臭化水素酸塩二臭化物、および数種類の第四級アンモニウムポリブロミドが含まれます。
2. 臭素の製造
臭素は、天然に存在する臭素含有液(かん水)や海水、あるいはカリウム塩の製造過程から生産されます。
ほとんどのかん水や海水では、臭化物イオンに比べて塩化物イオンのモル濃度が著しく高いため、これらの源から臭素を単離することは困難です。
臭素を抽出するには、選択性の高い分離方法が必要です。幸いにも、塩化物と比較して臭化物が酸化されやすいこと、および酸化生成物である臭素が揮発性であることを利用した方法が存在します。
塩素が最も経済的で便利な酸化剤として使用されます。
臭素生産の主要な4つの段階には、臭化物の臭素への酸化、水溶液からの臭素の追い出し(ストリッピング)、蒸気からの臭素の分離、および臭素の精製が含まれます。
臭素回収のために塩素化を利用する2つの一般的なプロセスが、以下の化学反応に基づいて一般的に採用されています:
2 Br– + Cl2 → Br2 + 2 Cl–
第一のプロセスである「スチーミングアウト法(蒸気蒸留法)」は、かん水中の臭化物濃度が 1000 ppm を超える場合に、臭素を含むかん水や廃液に使用されます。このプロセスでは、蒸気を使用して蒸気から臭素を直接凝縮させます。
第二のプロセスである「ブローイングアウト法(空気追い出し法)」は海水に使用され、大量のストリッピングガスが必要となるため、空気を使用します。臭素を濃縮するために、アルカリ性溶液または還元性溶液でトラップする必要があります。
2.1. スチーミングアウト法(蒸気蒸留法)
1–5 g/L の濃度で Br– を含むかん水からの臭素生産は、1906年に KUBIERSCHKY によって初めて記載されたプロセスに従います。
原料のかん水は熱交換器 (a) で加熱され、その後重力流によって2つの充填塔 (b), (c) を通過します(図1)。上部の塔では、かん水は塩素と臭素を吸収するリサイクルガス流と接触します。
下部の塔 (c) の底部付近から塩素と蒸気が導入されます。それらが上昇する際、塩素がかん水中の臭化物と反応し、臭素蒸気と塩素(重量比で約 85:15)および蒸気の混合物が生成され、塔頂から取り出されます。
水と大部分のハロゲンは凝縮され (d)、液相は重力分離器 (e) に入り、ガスは上部の塔へ送られます。
分離器から、溶解したハロゲンを含む水は下部の(スチーミングアウト)塔へ送られ、一部の塩素を含む重い臭素層は精留塔 (g) へ流れます。
塩素蒸気は上部の塔への流れに合流し、純度約 99 % の液体臭素は、臭素化合物の製造に直接使用されるか、さらなる精製のために取り出されます。
高温の脱臭素されたかん水は、必要に応じて酸性を中和し (h)、遊離ハロゲンを還元する処理を受けた後、熱交換器を通過して、流入するかん水を温めます。
オリジナルの Kubierschky プロセスの最近の改良は、現代の操業の大規模化、耐食性材料の使用、および制御に必要な手順と計装に関連しています。
プロセスは、pH、酸化還元電位、流量、温度、圧力などの重要なポイントを測定することによって制御されます。
かん水中の硫化水素などの還元性物質と塩素が反応すると、酸性度が発生します。この酸性度は、次亜臭素酸への加水分解を防ぐことで臭素遊離の効率を高めます。
しかし、かん水にカルシウムやストロンチウムが含まれている場合、硫酸塩として沈殿し、塔の充填物や熱交換面、あるいはかん水処分井を汚損させる可能性があるため、硫酸の使用は推奨されません。かん水に硫化物が含まれている場合、硫酸塩が形成されます。
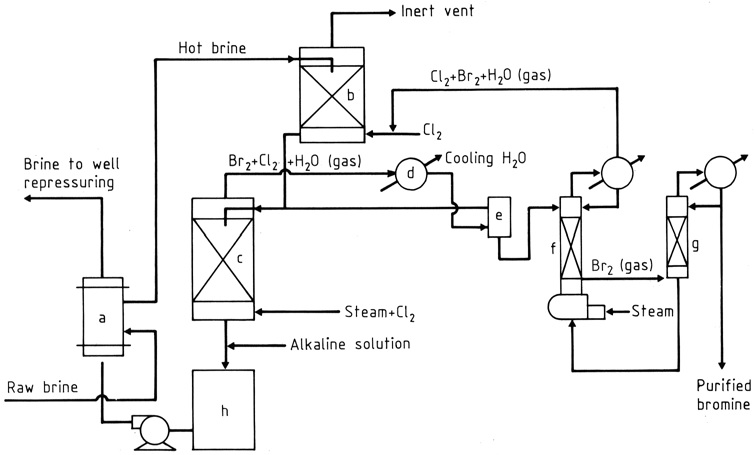
a) 臭素交差熱交換器、b) 塩素吸収器、c) スチーミングアウト塔、d) 凝縮器、e) 分離器、f) ストリッピングカラム、g) 精留塔、h) 中和器
2.2. 海水プロセス
海水から直接臭素を抽出し、商業的な回収に成功したのは、アメリカのノースカロライナ州ウィルミントン近郊が最初でした。これは、もともと H. H. DOW によってかん水処理用に開発された空気追い出し法を用いて達成されました。
臭素を約 65 mg/L しか含まない海水を加熱するために必要な蒸気のコストが高すぎるため、蒸気ではなく空気の使用が必要と判断されました。なお、ウィルミントンのプラントは現在は稼働していません。
海水はブローイングアウト塔の頂部へ汲み上げられ、上昇中に適切に混合されるよう、ポンプの直上で硫酸と塩素が添加されます。
天然の炭酸水素塩を中和して pH を 3.5 にするために、水 1 トンあたり 10 % 硫酸 1.3 kg が必要であり、理論上の必要量に対して 15 % 過剰な塩素が使用されます。
空気が塔内を吸い上げられ、下降する海水から臭素と塩素(または塩化臭素)の混合物を抽出します。その後、空気は吸収塔に引き込まれ、そこで炭酸ナトリウム溶液を用いて向流洗浄されます。
起こるいくつかの反応は、大まかに以下の式で要約されます:
3 Na2CO3 + 2 Br2 + BrCl → NaBrO3 + 4 NaBr + NaCl + 3 CO2
空気からの飛沫を除去するために、吸収塔とファンの間に小さな充填室が設置されています。
洗浄液のアルカリ度がほぼ消失すると、溶液は貯蔵タンク、次いでリアクターへ移され、そこで硫酸で処理され、臭素を放出するためにスチーミングアウトされます。化学反応は以下のように記述されます:
NaBrO3 + 5 NaBr + 3 H2SO4 → 3 Br2 + 3 Na2SO4 + 3 H2O
初期のドイツでの生産における電気分解の使用など、臭化物を酸化するために塩素の代わりに用いられた他の方法も存在します。
米国では、塩化カリウム生産液からの副産物として臭素を回収するために、改良された Kubierschky プロセスが採用されています。
3. 臭素の用途
臭素は多用途な元素であり、幅広い応用分野があります。難燃剤、掘削流体、有機合成、医薬品、水処理用殺生物剤、および農業において広く使用されています。
さらに、染料、防虫剤、香料、および写真材料の製造にも使用されます。
臭素化合物の他の用途には、水銀制御や製紙業が含まれます。
臭素系難燃剤は、臭素誘導体の重要な部分を占めています。1990年代初頭以来、その消費量は大幅に増加し、2013年には総臭素消費量の半分以上を占めるようになりました。
これらは、コンピューター、家具、基板、携帯電話、テレビ、繊維製品などの産業用および家庭用機器に使用されています。
臭素化合物の高密度特性は、油圧作動油、ゲージ液、鉱石浮選、および掘削流体に有効に活用されています。
臭化カルシウム、臭化亜鉛、および臭化ナトリウムは、石油・ガス掘削業界において、高密度の透明な塩水(かん水)掘削、完井、パッカー、および修復用流体を調製するために使用されます。
水処理用の臭素系殺生物剤は、水処理市場の大部分を塩素が占めているものの、重要かつ拡大しているグループです。
一般に、水処理業界の産業分野および消費者分野の両方で、塩素や塩素系化合物から臭素ベースの製品への置き換えが進んでいます。
臭素系殺生物剤は、冷却塔やプロセス水で懸念される幅広い pH レベルに対する耐性が高いため、さまざまな産業用途において塩素系殺生物剤よりも好まれます。
臭素とその化合物は、石炭火力発電所における水銀排出を軽減するために使用されています。
臭化カルシウムや臭化ナトリウムのような無機臭素化合物は、石炭火力発電所からの燃焼排ガス中に存在する水銀と結合して水銀化合物を形成し、これがスクラバーで捕捉されることで、燃焼中に放出される水銀の最大 90 % を除去します。
参考文献
- Bromine; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a04_391.pub2
- Bromine; Kirk-Othmer Encyclopedia of Chemical Technology. – https://onlinelibrary.wiley.com/doi/10.1002/0471238961.0218151310010311.a01.pub3