酒石酸:性質、反応、製造および用途
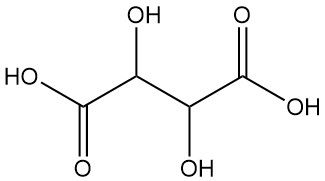
酒石酸(しゅせきさん)は、別名アシドゥム・タルタリクム(acidum tartaricum)や2,3-ジヒドロキシブタン二酸(IUPAC命名法)としても知られ、多くの果実に天然に含まれる白く結晶性の有機酸であり、化学式は C4H6O6 です。この分子は、2つの非対称炭素中心を持ち、同一分子内に2つのカルボン酸基とジアール(2価アルコール)構造を有するため、4つの立体異性体が存在します。
エナンチオマー:
L(+)-酒石酸とD(-)-酒石酸は、偏光面を回転させる光学活性異性体です。これら鏡像関係にある分子(エナンチオマー)は、旋光の方向が逆である点を除き、同一の物理的・化学的性質を共有しています。
ジアステレオマー:
DL-酒石酸(ラセミ混合物)は、L(+)体とD(-)体の等モル組み合わせによる合成品です。内部補償のため光学的に不活性です。
メソ酒石酸(分割不能な酒石酸)は、活性型やラセミ型のいずれとも異なる物理的性質を持つ、もう一つの光学不活性なジアステレオマーです。ラセミ型もメソ酒石酸も、光学活性な酸ではありません。
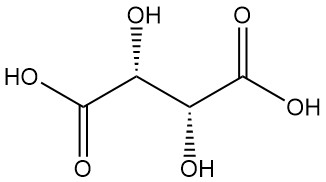
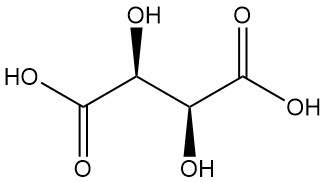
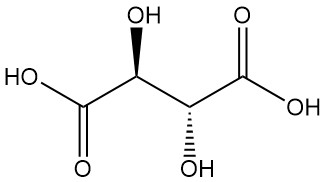
酒石酸は古くからそのカリウム塩(酒石)として知られており、18世紀にシェーレによって初めて単離されました。1830年にはベルセリウスがその構造を決定しました。酒石酸塩に関するパストゥールの画期的な研究(1848–1860年)は、有機化学に革命をもたらしました。
彼は、酒石酸ナトリウムアンモニウムの結晶を分離し、それぞれの旋光性を示すことで、ラセミ体と光学活性体の関係を説明しました。
L(+)-酒石酸は、天然に最も多く存在する形態であり、商業的に生産されている変体です。様々な植物、特にブドウの中に酸または塩として含まれており、ワインの発酵中に酒石酸水素カリウム(酒石)として蓄積します。この不溶性の沈殿物が、商業的なL(+)-酒石酸生産の主要な原料となります。
目次
1. 酒石酸の物理的性質
天然のL(+)-酒石酸の物理的性質を表1に示します。これらはD(-)-酒石酸の性質と同一です。酒石酸は無臭の固体で、強い酸味を持ち、空気中で安定しています。
酒石酸溶液の旋光度は濃度によって異なり、以下の式で表されます:
[α] = 15.050 – 0.1535 c
ここで c は 20–50% wt/vol の範囲における酒石酸の濃度です。
表2は様々な温度における溶解度を、表3は様々な温度(°C)における酒石酸溶液の相対密度を示しています。
表1:物理的性質
| 項目 | 値 |
|---|---|
| 分子量 | 150.09 g/mol |
| 結晶形 | 無水単斜晶系針状(5 °C以上) |
| 密度 | 1.7598 g/cm³ |
| 融点 | 169–170 °C |
| 外観 | 無色結晶 |
| 分解 | 220 °C以上(カラメル臭を伴う) |
| 溶解度(水) | 極めて高い |
| 溶解度(アルコール 18 °C) | 20.4 g / 100 g |
| 溶解度(ジエチルエーテル 18 °C) | 0.3 g / 100 g |
| 旋光度 (20% wt/vol) | +11.98°(D(-)体は -11.98°) |
| 燃焼エンタルピー | 1149.9 kJ/mol |
| 比熱容量 (0-100 °C) | 1237 kJ kg⁻¹ K⁻¹ |
| 酸解離定数 (25 °C) | K1 = 1.17 × 10⁻³ / K2 = 5.0 × 10⁻⁵ |
| 溶液の沸点 (25%) | 102.2 °C |
| 溶液の沸点 (50%) | 106.7 °C |
| 融点における屈折率 (170 °C) | 1.464 |
表2:溶解度 (g/100 g H2O)
| 温度 (°C) | 0 | 5 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| 溶解度 | 115 | 120 | 125 | 139 | 156 | 176 | 195 | 218 | 244 | 273 | 307 | 343 |
表3:相対密度
| 温度 (°C) | 密度 |
| 1 | 1.0045 |
| 10 | 1.0469 |
| 20 | 1.0969 |
| 30 | 1.1505 |
| 40 | 1.2078 |
| 50 | 1.2696 |
2. 酒石酸の化学反応
L(+)-酒石酸は170-180 °Cで融解し、水の損失を伴わずにメタ酒石酸へ異性化(構造再編成)します。さらに加熱すると無定形の酸無水物が生じます。これらの酸無水物は、水と共に沸騰させると酒石酸に戻ります。
220 °Cを超えると、酒石酸は分解、膨張し、発火して炭素質の残渣を残します。
酒石酸は酸化剤に対して非常に敏感です。過酸化水素と硫酸第一鉄(フェントン試薬)による酒石酸の酸化は、ジオキソコハク酸を生成します。
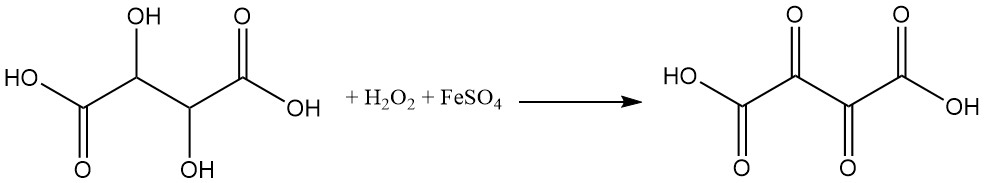
ヨウ化水素による還元では、コハク酸が得られます。
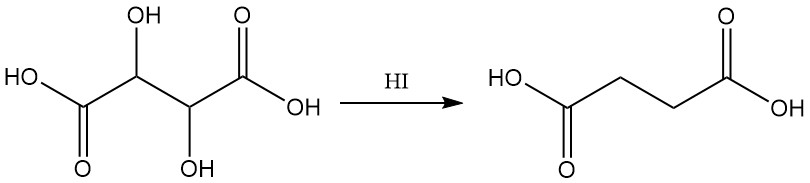
溶液中の酒石酸塩は、アンモニア性硝酸銀と反応して金属銀を生成します(銀鏡反応)。
酒石酸は、塩基による重金属塩の沈殿を抑制するための錯化剤として使用されます。
L(+)-酒石酸溶液をアルカリ(KOHまたはNaOH)と共に長時間沸騰させると、ラセミ酒石酸およびメソ酒石酸が生成されます。
3. 酒石酸の天然資源
L(+)-酒石酸は、大規模に商業生産されている唯一の異性体です。その原料は専らワイン製造過程で発生する天然の残渣に由来します。これらの残渣には、主に酒石酸水素カリウム(クリーム・オブ・ターター)の形で、また少量ながら酒石酸カルシウムの形で酒石酸が含まれています。
酒石酸の供給源は以下の通りです:
- 酒石(タルタル):エタノール濃度の上昇に伴い、ワイン樽の壁面に付着する赤味を帯びた沈殿物です。高濃度(80–90%)の酒石酸水素カリウムを含んでいます。
- 澱(おり):ワイン樽の底に沈殿する堆積物で、酒石酸水素カリウムの含有量はより低く(19–38%)なります。
- 乾燥澱:酒石酸水素カリウム含有量を高める(55-70%)よう処理された澱です。
- 蒸留バイプロダクト:蒸留所がワインの澱やブドウの搾りかすから得る材料です。蒸留によってアルコールを除去した後、消石灰で処理して酒石酸カルシウムとして沈殿させます。
4. 酒石酸の製造
酒石酸には複数の異性体が存在しますが、大規模に商業生産されているのはL(+)-酒石酸のみです。特定の用途のために、ごく少量のラセミ酸も合成されています。
4.1. L(+)-酒石酸の製造
L(+)-酒石酸の主要な生産者はスペイン、フランス、イタリアに位置しています。例えば、1784年設立のSociété Legré-Manteは最も古い生産者の一つです。
L(+)-酒石酸の製造方法はすべて、酒石酸カルシウムを硫酸で分解することに基づいています。歴史的には、原料(酒石酸カルシウム)を得るために、ショイラー・ケストナー酸性法と、シェーレ・ロヴィッツ中性法(デフォッセ変法を含む)の2つの方法が競合していました。現在では、より経済的な中性法が主流となっています。
乾燥した原料(酒石や澱)は、まず粉砕され、焙焼機で160 °C、2時間加熱されます。この工程により、後の段階で濾過を困難にする可能性のある有機不純物が除去されます。
加熱された焙焼品は反応器に移され、水で希釈された後、水酸化カルシウムでpH 5まで中和されます。反応温度は70 °Cに維持されます。
反応効率を高め損失を最小限に抑えるため、化学量論量に対して10%過剰の塩化カルシウムまたは硫酸カルシウムが添加されます。以下の化学反応が進行します:
2 KHC4H4O6 + Ca(OH)2 + CaCl2 → 2 Ca4H4O6 + 2 KCl + 2 H2O
生成した酒石酸カルシウムは、回転濾過機を用いて残りの液体(母液)から分離され、洗浄されます。原料が蒸留所由来の場合、この初期段階は省略されることがあります。
第2段階では、得られた酒石酸カルシウムを水溶液中で硫酸を用いて分解します。この反応により酒石酸溶液と不溶性の硫酸カルシウムが得られます:
CaC4H4O6 + H2SO4 → H2C4H4O6 + CaSO4
反応を最適化するため、酒石酸に対して約5%過剰の硫酸が使用されます。得られた混合物は濾過および洗浄され、不純物が除去されます。
約200 g/Lの濃度を持つ赤色の酒石酸溶液は、真空蒸発器にて70 °Cで650 g/Lまで濃縮されます。さらに真空下70 °Cで、結晶が形成し始める(約1300 g/L)まで濃縮が続けられます。
この固液混合物は、ゆっくりと冷却するために晶析装置に移され、結晶の収量を最大化します。冷却後、遠心分離機で乾燥させ、結晶と母液を分離します。
酒石酸をまだ含んでいる母液は、粒状酒石酸の収量を最大化するために、蒸発、造粒、乾燥のサイクルを繰り返します。得られた粒子は冷却され、650 g/Lの酒石酸溶液を形成します。
この溶液は、活性炭による脱色や、余分な鉄分や硫酸を除去するための化学的精製を経て(すべて70 °Cで実施)、濾過された後、結晶化が始まるまで真空下で濃縮されます。
混合物は再び晶析装置に移されるか、結晶収量を最大化するために冷却されます。その後、混合物は遠心分離によって分離されます。残留酒石酸を含む母液は、再処理される前に蒸発、造粒、乾燥のさらなるサイクルを経ます。
精製された粒子は140 °Cのオーブンで乾燥され、2000 μmから100 μm未満(粉末)までの様々な粒度に篩い分けされます。
上記のプロセスが主要な方法ですが、他の製造プロセスも検討されています。これには、発酵によるL(+)-酒石酸の製造や、ラセミ体であるDL-酒石酸の化学合成が含まれます。
4.2. 発酵によるL(+)-酒石酸の製造
L(+)-酒石酸の従来の製造方法は化学反応に依存していますが、発酵ベースの代替法についての研究も進行中です。
この目的のために主に2つの細菌株が検討されています:
- アセトバクター・スボキシダンス (Acetobacter suboxydans):この菌種は、グルコースをL(+)-酒石酸に転換する能力について調査されています。
- ノカルディア・タルタリカンス (Nocardia tartaricans):この細菌は、シス-エポキシコハク酸およびそのナトリウム誘導体を目的の製品に転換する有望な性質を示しています。
4.3. ラセミDL-酒石酸の化学合成
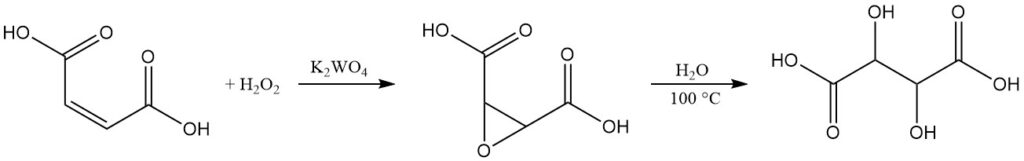
商業市場ではL(+)-酒石酸が主流ですが、ラセミDL-酒石酸については小規模な製造プロセスが存在します。
この方法はマレイン酸またはその塩から始まります。水溶液中で、タングステン酸カリウムを触媒として、マレイン酸を35%過酸化水素で酸化させます。この反応により、中間体としてエポキシコハク酸が得られます。
反応混合物を沸騰させることで、エポキシコハク酸が加水分解され、ラセミ酒石酸が形成されます。冷却後、最終製品は遠心分離、洗浄、および乾燥によって単離されます。
このプロセスのいくつかのバリエーションが研究され、科学文献に記録されています。この研究活動は、この手法に対して出願された多数の特許にも反映されています。
現在、ラセミDL-酒石酸の商業生産は限定的であり、南アフリカで1つの小規模な生産ユニットが稼働しているのみです。
5. L(+)-酒石酸の誘導体
酒石酸は多くの塩やエステルを容易に形成し、そのいくつかは重要な商業用途を持っています。このセクションでは、最もよく知られた化合物について説明します。
5.1. 酒石酸ナトリウムカリウム
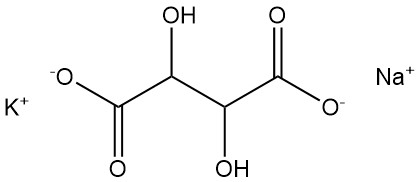
酒石酸ナトリウムカリウムは、セニェット塩(Seignette’s salt)またはロッシェル塩(Rochelle salt)としても知られ、1672年にピエール・セニェットによって発見されました。
物理的性質:
- 化学式:KNaC4H4O6 · 4 H2O
- CAS番号:[6381-59-5]
- モル質量:282.23 g/mol
- 密度:1.79 g/cm³
- 融点:70–80 °C (220 °Cで分解)
- 溶解度:0 °Cで26 g/100 mL、26 °Cで66 g/100 mL(水)
酒石酸ナトリウムカリウム製造の原料は、最低68%の酒石酸含有量を持つ酒石です。
この溶液を水で希釈し、熱い水酸化ナトリウムで中和し、活性炭で脱色した後、濾過します。濾液は蒸発によって濃縮され、冷却によって結晶化して固体の塩を生成します。これを分離、洗浄、乾燥、篩い分けした後に包装します。
市販の粒度は 2000 μm から 250 μm 未満(粉末)の範囲です。
5.2. 酒石酸水素カリウム
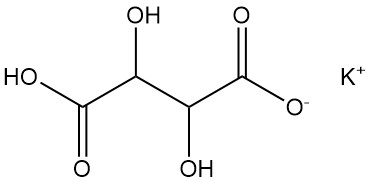
酒石酸水素カリウムは、一般にクリーム・オブ・ターター(cream of tartar)として知られています。
物理的性質:
- 化学式:KHC4H4O6
- CAS番号:[868-14-4]
- 密度:1.96 g/cm³
- 溶解度:20 °Cで0.57 g/100 mL、100 °Cで6.1 g/100 mL(水)
これは主に、ロッシェル塩製造後に残る母液から得られます。酒石酸水素カリウムは脱色、精製、濾過され、塩酸または硫酸で酸性化され、沈殿、遠心分離、乾燥、粉砕を経て、微粉末として包装されます。
5.3. 吐根石(酒石酸アンチモニルカリウム)
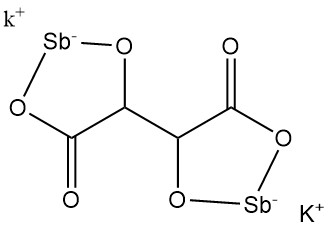
酒石酸アンチモニルカリウムは、1631年にアドリアン・ド・メインシヒトによって発見されました。
物理的性質:
- 化学式:KSbC4H2O6 · 1.5 H2O
- CAS番号:[28300-74-5]
- モル質量:333.93 g/mol
- 密度:2.61 g/cm³
- 溶解度:25 °Cで8.7 g/100 mL、100 °Cで35.7 g/100 mL(水)
酒石酸アンチモニルカリウムは、水中で酸化アンチモンとクリーム・オブ・ターターを反応させ、続いて残液の濃縮と結晶化を行うことで製造されます。濾過後、結晶は乾燥、粉砕されます。
5.4. メタ酒石酸
メタ酒石酸は、酒石酸を170-180 °Cに加熱することによって製造されます。この変換は酒石酸分子内での内部エステル化を伴い、多かれ少なかれ重合した製品となります。メタ酒石酸は、酒石酸塩の沈殿に対して並外れた抑制効果を持っています。
6. 酒石酸の用途
L(+)-酒石酸とその誘導体は、食品、医薬品、ワイン醸造など、様々な産業で使用されています。
L(+)-酒石酸 (E 334) の用途:
- ワインのマスト、キャンディ、ゼリー、ジャム、フルーツネクター、アイスクリーム、ゼラチン、ペーストの酸味剤として、風味を向上させる。
- 相乗的抗酸化剤として果物、野菜、魚を保存し、pH、色、味、栄養価を安定させる。
- 油脂類の抗酸化剤として。
- 炭酸飲料の調製に。
- 医薬品有効成分の賦形剤またはキャリアとして、塩基性の補正を助ける。
- 安定性と高い溶解性から、発泡錠や粉末の酸味剤として。
- セメント産業、特にプラスターや石膏の遅延剤として。
- 金属の研磨および洗浄に。
クリーム・オブ・ターター (E 336) は、ワイン中の酒石酸塩の沈殿を促進するため、また化学酵母(ベーキングパウダー)の製造や、一部の医薬品における緩下剤として使用されます。
セニェット塩 (E 337) は、電着性や収率を向上させるための電気めっきプロセス、電子機器や圧電素子、鏡の銀引きにおける還元剤、およびフェーリング液の構成成分として使用されます。また、シガレットペーパー製造における燃焼調節剤、一部の医薬品の緩下剤、繊維・皮革産業の媒染剤としても利用されます。
少量の酒石酸アンチモニルカリウムは、咳止めシロップの去痰薬として使用され、また一部の熱帯病の治療を助けます。
メタ酒石酸は、テーブルワインにおける酒石酸塩の結晶化を抑制するために使用されます。
脂肪酸モノグリセリドおよびジグリセリドの酒石酸エステルは、製パン業界で乳化剤として使用されます。
7. 酒石酸の毒性
クエン酸とは異なり、酒石酸は人体内のクレブス回路(エネルギー産生経路)に直接関与していません。
天然の形態であるL(+)-酒石酸は、果物やワインに含まれています。経口摂取後、約20%が尿を通じて排出されますが、大部分は腸内細菌叢による細菌分解を受けます。糞便中に痕跡は検出されません。
吸収された酒石酸は速やかに血流から除去され、腎臓から排出されるか、様々な組織で代謝されます。
ラットを用いたL(+)-酒石酸ナトリウムの長期研究では、毒性や発がん性の兆候は見られませんでした。さらに、1日あたり3 g/kg体重の用量において、腎機能や病理への悪影響は観察されませんでした。
ラセミ(DL)-酒石酸については、それほど広範な研究はなされていませんが、天然のL(+)異性体とは挙動が異なることが研究で示唆されています。
DL-酒石酸は血流からの消失速度が遅く、腎臓に長期間蓄積し、これらの臓器の重量増加を引き起こす可能性があります。この腎毒性効果のため、DL体は食品や医薬品への使用が承認されていません。
参考文献
1. Tartaric Acid; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a26_163
2. Tartaric Acid; Van Nostrand’s Encyclopedia of Chemistry. – https://onlinelibrary.wiley.com/doi/full/10.1002/0471740039.vec2453
3. Organic Acids in Fruits. https://onlinelibrary.wiley.com/doi/abs/10.1002/9781119431077.ch8
4. Tartaric acid. https://www.sciencedirect.com/science/article/abs/pii/B9780128190968000197