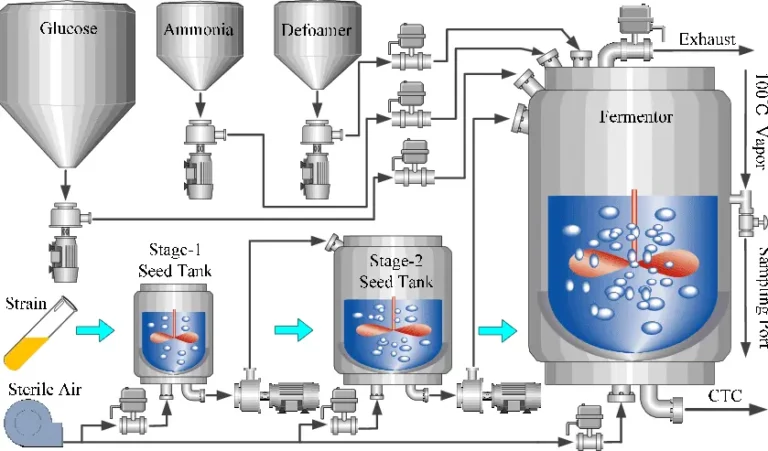
産業プロセスにおける化学反応

化学反応は、多くの産業プロセスの根幹をなす要素です。これらの反応は、一つまたは複数の物質を新しい生成物へと変換するプロセスであり、燃料、プラスチック、医薬品など、多種多様な材料の製造に利用されています。
化学反応の背後にある原理を理解することは、産業プロセスを設計し、最適化するエンジニアや化学者にとって極めて重要です。
産業プロセスで発生する化学反応には、燃焼、酸化還元反応、重合、水素化、カルボニル化、アシル化、アルキル化、ニトロ化、脱水素、エステル化、スルホン化など、いくつかの主要なタイプがあります。
目次
- 1. 燃焼反応
- 2. 酸化還元反応
- 3. 重合反応
- 4. 酸化反応
- 5. 水素化反応
- 6. カルボニル化反応
- 7. アシル化反応
- 8. アルキル化反応
- 9. ニトロ化反応
- 10. 脱水素反応
- 11. エステル化反応
- 12. スルホン化反応
- 参考文献
1. 燃焼反応
燃焼反応は、完全燃焼と不完全燃焼の2つのカテゴリーに分類できます。完全燃焼では、燃料が完全に燃え尽き、最終生成物として二酸化炭素(CO2)と水(H2O)のみが生成されます。
対照的に、不完全燃焼は燃料が完全に燃えない場合に起こり、一酸化炭素(CO)、すす、およびその他の汚染物質の混合物が生成されます。
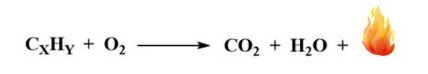
産業プロセスでは、最大のエネルギーを生み出し、汚染物質の排出が最も少ないため、完全燃焼が望まれます。しかし、特に着火が困難な燃料や燃焼効率の低い燃料を使用する場合、完全燃焼を実現することは困難な課題となることがあります。
燃焼反応を最適化するには、反応の化学量論、燃焼温度、燃料と酸化剤の混合状態など、いくつかの要因を考慮する必要があります。
反応の化学量論とは、完全燃焼を達成するために必要な反応物の比率を指します。燃焼温度も、反応速度や最終生成物の品質に影響を与えるため非常に重要です。
燃料と酸化剤の混合も、反応の効率や最終生成物の品質に影響を与えるため不可欠な要素です。
産業プロセスに加えて、燃焼反応は森林火災や火山噴火などの多くの自然現象にも関わっています。これらの反応は、大気汚染や地球温暖化など、環境に重大な影響を及ぼす可能性があります。
燃焼反応による環境負荷を軽減するため、燃焼効率の向上や、汚染物質の排出を抑えるクリーンな技術の開発に多くの努力が払われています。
2. 酸化還元反応
酸化還元反応(レッドクス反応とも呼ばれる)は、2つの種の間での電子の受け渡しを伴います。酸化反応ではある種が電子を失い、還元反応では別の種が電子を受け取ります。
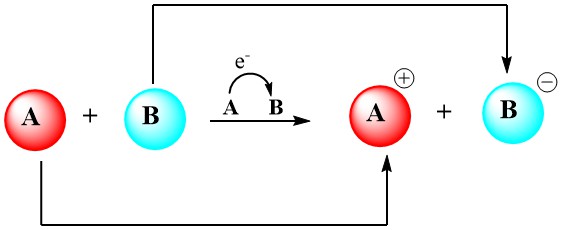
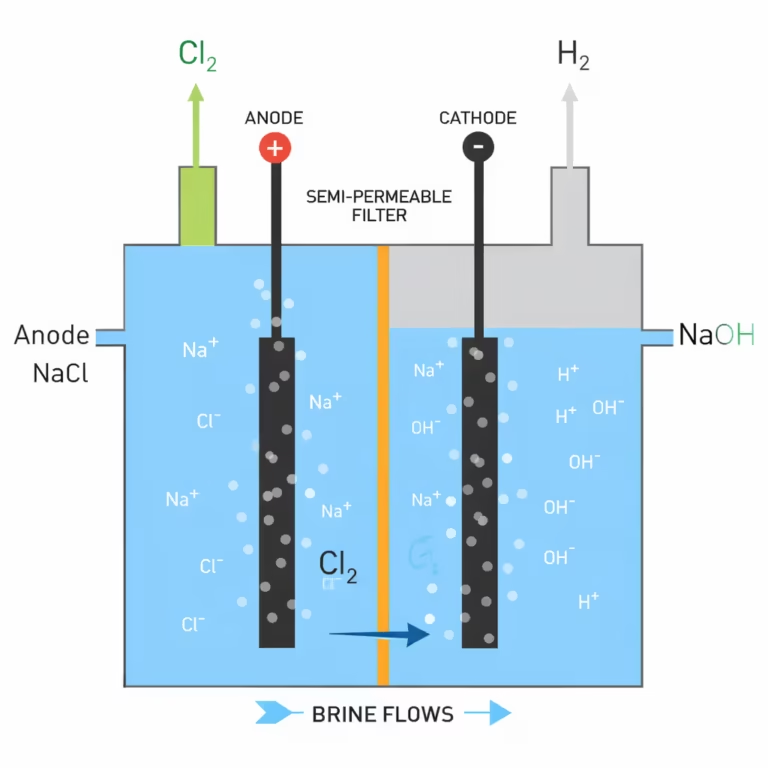
これらの反応は、金属生産、電気めっき、化学品や燃料の製造など、多くの産業プロセスにおいて不可欠です。電気化学反応の重要な産業利用としては、塩化ナトリウム(NaCl)の電解による水酸化ナトリウムの製造、その他のアルカリ金属水酸化物の製造、および漂白剤の製造が挙げられます。
酸化還元反応は、自然に発生するか、進行にエネルギー入力を必要とするかに応じて、自発的または非自発的のいずれかに分類されます。自発的な酸化還元反応は、外部からのエネルギー入力を必要とせずに発生するもので、電池やその他のエネルギー貯蔵デバイスでよく利用されます。
一方、非自発的な酸化還元反応は、進行するために外部エネルギー源を必要とし、電気分解やその他の化学プロセスで使用されます。
酸化還元反応の一般的な例の一つは、先に述べた鉄の錆びです。この反応では、鉄が酸素と反応して酸化鉄を生成します。これが、私たちが錆と呼ぶおなじみの赤褐色の物質です。
錆びは酸化反応の一例であり、鉄が酸素に対して電子を失います。この反応は、金属の腐食の主な原因であり、修理や交換に多大な費用がかかるため重要です。
酸化還元反応のもう一つの例は、プラスチックやその他の材料の製造に使用される塩素ガスの生成です。塩素ガスは塩水の電気分解によって生成されます。これは進行に外部エネルギー源を必要とする非自発的な酸化還元反応です。
この反応では、塩水中の塩化物イオンが酸化されて塩素ガスと水素ガスが生成されます。塩素ガスは強力な酸化剤であり、農薬、医薬品、プラスチックの製造など、多くの産業プロセスで使用されています。
3. 重合反応
重合反応は、モノマー分子が化学的に結合してポリマー鎖を形成する化学反応の一種です。得られるポリマーは、プラスチックや合成繊維から接着剤やコーティング剤まで、幅広い特性と用途を持ちます。
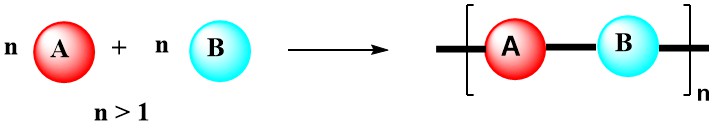
重合反応には、付加重合と縮合重合の2つの主なタイプがあります。付加重合では、二重結合を持つモノマー同士が反応してポリマー鎖を形成します。
この反応は通常、触媒や熱によって開始され、得られるポリマーは元のモノマーの単位が繰り返される長い鎖となります。一方、縮合重合は、共有結合を形成するために反応する官能基を持つ2つの異なるモノマーの反応を伴います。このタイプの反応では、通常、副産物として水などの小さな分子が生成されます。
重合反応は、プラスチックや合成繊維の製造から、医療用インプラントやドラッグデリバリーのための新素材の開発まで、幅広い産業用途で使用されています。
重合反応の一例は、世界で最も広く使用されているプラスチックであるポリエチレンの製造です。ポリエチレンはエチレンモノマーの付加重合によって製造され、包装材から建築資材まで幅広い用途に使用できる長鎖ポリマーとなります。
重合反応のもう一つの例は、テキスタイルやその他の用途に使用される合成繊維であるナイロンの製造です。ナイロンは、ヘキサメチレンジアミンとアジピン酸という2つのモノマーの縮合重合によって製造され、これらが反応してポリマー鎖を形成します。ナイロンはその強度と耐久性で知られており、衣類から自動車部品まで幅広い用途に使用されています。
4. 酸化反応
酸化反応とは、分子が電子を失う反応のことです。これは多くの場合、酸素原子の獲得を伴いますが、必ずしもそうとは限りません。主な側面は以下の通りです:
- 電子移動:酸化の核心的な原理は、分子からの電子の喪失です。これを、負の電荷を取り除き、分子の電荷をより「正」にすることだと考えてください。
- 酸素との関連:多くの場合、酸素原子を獲得することに関連付けられますが、酸化反応に酸素は厳密には必須ではありません。しかし、酸素はその強い電気陰性度、つまり電子を引き付ける力が強いため、一般的な酸化剤となります。
化学産業で使用されるさまざまな酸化剤(分子状酸素 O2、過酸化水素 H2O2、塩素 Cl2 など)は、標的分子から電子を受け取ります。酸化剤の選択は、コスト、選択性、反応条件などの要因によって決まります。
産業用触媒は、それ自体が消費されることなく反応を促進します。銅、マンガン、バナジウムなどの遷移金属が頻繁に使用されます。これらは選択性を高め、エネルギー消費を抑え、プロセスの効率を向上させることができます。
酸化反応はさまざまな産業で使用されています:
1. 汎用化学品の製造:
- アクリル酸は、アクリル繊維、塗料、接着剤に重要です。これは、金属酸化物触媒上でプロピレンを空気酸化することによって製造されます。
- テレフタル酸は PET プラスチックの構成要素です。p-キシレンを空気または酸素を使用して液相酸化することで製造されます。
- 硝酸は、肥料、爆薬、ナイロン製造に使用されます。これは、白金・ロジウム触媒上でアンモニアを空気酸化するオストワルト法を介して合成されます。
2. ファインケミカルおよび医薬品:
- 選択的酸化:複雑な分子内の特定の官能基を精密に変化させることは、医薬品の合成において極めて重要です。酵素や遷移金属触媒により、副反応を最小限に抑えた標的酸化が可能になります。
- ヒドロキシル化:ヒドロキシル基の導入は多くの医薬品にとって不可欠です。シャープレス不斉ジヒドロキシ化などの手法は、高い立体制御のためにキラル触媒を利用します。
3. 環境修復:
- 廃水処理:オゾンや過酸化物による酸化は、水を効果的に消毒し、有機汚染物質を分解します。
- 排煙脱硫:発電所の排出物から硫黄酸化物を除去するために、水酸化カルシウムなどの酸化剤を用いた湿式スクラビングが行われます。
5. 水素化反応
水素化反応は還元反応の特定の一種で、分子が水素原子を獲得する反応です。これは多くの場合、触媒の存在下で行われ、反応分子内の不飽和結合(通常は二重結合または三重結合)の飽和をもたらします。
分子への水素原子(H)の付加は、その飽和度を高め、反応性を低下させます。一部の水素化は触媒なしで高温で行うことができますが、触媒の使用は活性化エネルギーを大幅に下げ、より穏やかな条件下で反応を加速させます。ニッケル、パラジウム、白金などの遷移金属が水素化の一般的な触媒です。
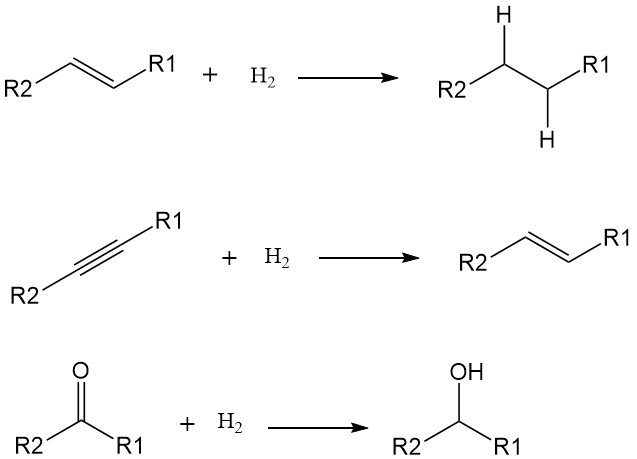
水素化は通常、二重結合や三重結合を標的とし、それらを単結合に変換します。例を挙げます:
- アルケンからアルカンへ:エチレン(C2H4)のような不飽和炭化水素を、エタン(C2H6)のような飽和炭化水素に変換します。
- アルキンからアルケンへ:アセチレン(C2H2)のような三重結合炭化水素を、エチレンのような二重結合アルケンに変換します。
- カルボニル基からアルコールへ:カルボニル基(C=O)を持つケトンやアルデヒドを、ヒドロキシル基(OH)を持つアルコールに還元します。
水素化反応は、以下のようなさまざまな産業で使用されています:
- 植物油加工:マーガリン製造のために、不飽和脂肪を飽和脂肪に変換することで液体油を硬化させます。
- 燃料精製:ガソリンやディーゼル燃料の脱硫と品質向上を行います。
- 医薬品製造:さまざまな医薬品やファインケミカルを合成します。
水素化は以下の分野でも使用されます:
- 食品・飲料産業:食品用の油脂の加工。
- 重合:特定の特性を持つポリマーの作成。
- 水素燃料電池:水素と酸素を電気に変換。
6. カルボニル化反応
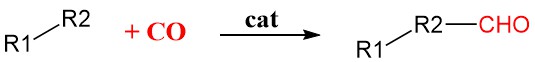
カルボニル化は、ロジウム、イリジウム、パラジウム、ニッケルなどの遷移金属触媒を使用して、有機分子に一酸化炭素(CO)を導入する有機合成の一般的な手法です。これらの触媒は CO 分子を結合して活性化し、反応性を高めることで、有機基質への取り込みを可能にします。
これは選択性が非常に高い反応であり、副反応を最小限に抑えながら、分子内の望ましい位置に CO 分子を正確に付加できることを意味します。
このため、以下のような幅広い重要な化学品の製造に役立っています:
- 酢酸:世界の合成酢酸の 70% 以上が、ロジウムまたはイリジウム触媒によるメタノールのカルボニル化を使用して製造されています。
- アミノ酸誘導体:アミドカルボニル化は、医薬品やその他の産業で使用される価値の高いアミノ酸誘導体を作成するための関心が高まっている分野です。
- 医薬品中間体:芳香族ハロゲン化物のカルボニル化は、ドラッグやその他の生理活性分子の重要な構成要素を作成するための標準的な手順になりつつあります。
7. アシル化反応
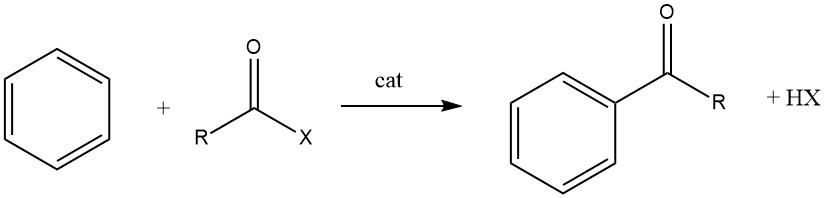
フリーデル・クラフツアシル化は、芳香族化合物と、ハロゲン化アシル、酸無水物、酸、またはエステルといったアシル化剤との反応により、芳香族ケトンを生成する反応です。この反応は酸触媒の存在下で行われます。
芳香族基質のアシル化は、医薬品、殺虫剤、可塑剤、染料、香水、およびその他のさまざまな商業製品の製造で広く利用される芳香族中間体の合成に使用されるため、産業的に非常に重要です。これらの特殊化合物は、通常、アルキル化製品と比較して小規模に生産されます。
フリーデル・クラフツアシル化によって生成される芳香族ケトン
| アシル化剤 | 芳香族化合物 | 生成物 | 最終用途 |
|---|---|---|---|
| 無水酢酸 | ベンゼン | アセトフェノン | 香水、医薬品、溶剤、可塑剤 |
| 無水酢酸 | トルエン | 4-メチルアセトフェノン | 香水 |
| 無水酢酸 | アニソール | 4-メトキシアセトフェノン | 香水 |
| 無水酢酸 | イソブチルベンゼン | 4-イソブチルアセトフェノン | 医薬品 |
| ジクロロアセチルクロリド | 1,2-ジクロロベンゼン | α,α,2,4-テトラクロロアセトフェノン | 殺虫剤 |
| クロロブチロイルクロリド | フルオロベンゼン | クロロプロピル 4-フルオロフェニルケトン | 医薬品 |
| 四塩化炭素 | ベンゼン | ベンゾフェノン | 医薬品、殺虫剤、香水 |
| 塩化ベンゾイル | ベンゼン | ベンゾフェノン | |
| ホスゲン | N,N-ジメチルアニリン | 4,4′-ビス-ジメチルアミノベンゾフェノン | 染料 |
| 無水フタル酸 | ベンゼン | 2-ベンゾイル安息香酸 | アントラキノン |
8. アルキル化反応
芳香族化合物のフリーデル・クラフツアルキル化は、酸触媒による親電子置換反応を伴い、アルキル基が芳香族の水素と入れ替わります。この目的のために、オレフィン、ハロゲン化アルキル、アルコールなどの多様なアルキル化剤が一般的に使用されます。
この反応は、ヘテロ芳香族化合物やフェロセンのような化合物を含む、さまざまな芳香族基質に適用できます。これらの反応は通常、迅速かつ発熱的であり、多くの場合、液相の穏やかな条件下で行われます。
しかし、場合によっては、特定の基質に対してより厳しい条件の気相プロセスが利用されます。オレフィン、ハロゲン化アルキル、アルコールをアルキル化剤として使用した場合、全体の反応は次のように進行します:
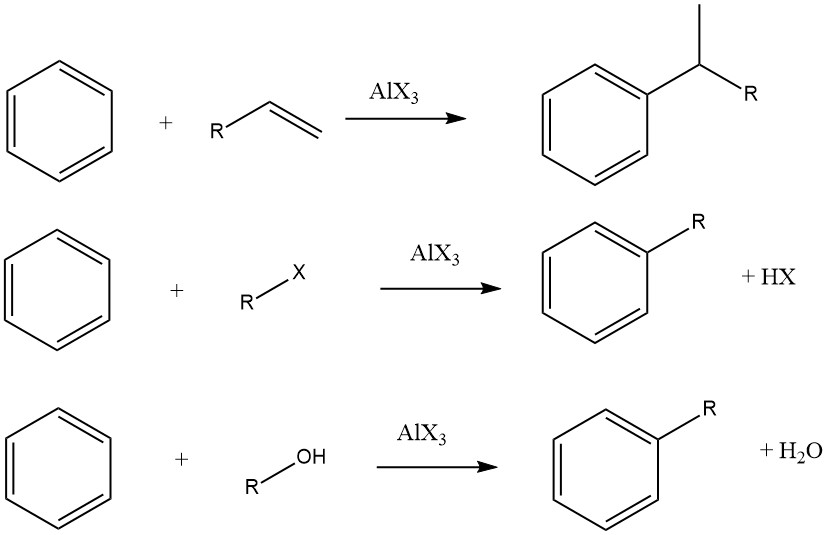
アルキル部位の異性化の程度や、付加プロセス中のマルコフニコフ則への準拠は、触媒の酸性度によって異なります。
アルキル化反応の利用例としては、ベンゼンからのエチルベンゼン、クメン、およびアルキルベンゼンの製造、トルエンとプロペンのアルキル化によるシメンの製造、フェノールのアルキル化によるアルキルフェノールの製造、およびフラン、チオフェン、N-ヘテロ環を含むさまざまな複素芳香族化合物のアルキル化が挙げられます。
9. ニトロ化反応
ニトロ化反応は、芳香環に一つ以上のニトロ基(NO2)を不可逆的に導入し、水素原子を置換する反応です。
ニトロ化は親電子置換反応であり、次の式で表されます:
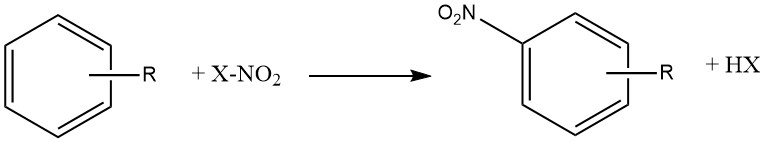
ニトロ基の導入は、環をさらなる親電子置換に対して不活性化(失活)させるため、モノニトロ化に使用される条件下でジニトロ化が起こることは稀です。
ジニトロ化には通常、より過酷な条件が必要であり、過剰でより強力な酸と、より高い温度を必要とします。これらの条件は、その場で段階的に反応を進めるのではなく、単離されたモノニトロ化合物に対して適用されることが多いです。
ニトロ化反応は非常に発熱的であり、ベンゼンのモノニトロ化(ΔH = -117 kJ/mol)やナフタレン(ΔH = -209 kJ/mol)がそれを証明しています。その結果、これは産業的に運営される単位操作の中で最も潜在的に危険なものの一つです。
ニトロ化の主な製品は、芳香環に一つのニトロ基が導入されたモノ置換ニトロ芳香族化合物です。ニトロ化による重要な産業製品には以下のものが含まれます:
- ニトロベンゼン (C6H5NO2)
- ニトロトルエン(例:オルト-ニトロトルエン、メタ-ニトロトルエン、パラ-ニトロトルエン)
- ニトロナフタレン(例:アルファ-ニトロナフタレン、ベータ-ニトロナフタレン)
- ニトロフェノール(例:オルト-ニトロフェノール、メタ-ニトロフェノール、パラ-ニトロフェノール)
- ニトロアニリン(例:オルト-ニトロアニリン、メタ-ニトロアニリン、パラ-ニトロアニリン)
10. 脱水素反応
水素化の逆である脱水素反応は、分子(通常は有機分子)から水素(H)が取り除かれる化学反応を指します。この一見単純なプロセスは、基礎的な実験室反応から大規模な産業プロセスまで、化学のさまざまな側面で重要な役割を果たしています。
この反応は C-H 結合を切断し、H2 ガスを放出することを伴い、多くの場合、吸熱的で、活性化エネルギーの障壁を克服するために熱または特定の触媒を必要とします。
脱水素は化学産業において以下の目的で使用される重要な反応です:
1. 価値の高い化学品の製造:脱水素は以下のような多くの製品を作るために不可欠です:
- スチレン:ポリスチレンプラスチックのモノマーで、エチルベンゼンの脱水素から製造されます。
- アルケン:ポリマー、燃料、潤滑剤の製造におけるさらなる反応に使用される不飽和炭化水素。
- ファインケミカル:医薬品、農薬、その他の特殊な分子には、しばしば脱水素ステップが含まれます。
2. エネルギー分野では、軽質炭化水素の接触脱水素が、従来の方法と比較してよりクリーンな燃料生産の可能性を提供します。
3. 脱水:アルコールから水(H2O)を取り除くことは脱水素の特殊なケースであり、水分子を排除することでアルケンを形成します。
11. エステル化反応
エステル化は、触媒の存在下でカルボン酸とアルコールが反応し、エステルと水を生成する可逆反応です。
エステル化反応は3つのステップのメカニズムで進行します:
- プロトン化:ブレンステッド酸触媒がカルボン酸のカルボニル酸素をプロトン化し、その親電子性を高めます。
- 親核攻撃:親核剤として働くアルコールの酸素原子が、親電子的なカルボニル炭素を攻撃し、四面体中間体を形成します。
- 脱プロトン化と水の脱離:中間体は(多くの場合触媒によって)脱プロトン化され、続いて水が排除されることで、エステルと副産物としての水が形成されます。
エステル化は平衡反応であり、ルシャトリエの原理により、エステルの収率を高める戦略が決定されます。過剰なアルコールの使用、水の除去(例:蒸留による)、および温度の最適化により、平衡をエステル形成の方へシフトさせることができます。
エステル化反応は幅広い用途があります:
- 香料と化粧品:エステルは、果物、花、香水の心地よい香りに大きく貢献しています。
- 医薬品:アスピリンやペニシリンを含む多数の薬物がエステル官能基を組み込んでいます。
- ポリマー:ポリマーの一種であるポリエステルはエステル化反応によって形成され、さまざまなプラスチックや合成繊維に使用されます。
- バイオ燃料:バイオディーゼルのようなバイオ燃料の製造にエステル化が採用されています。
- 食品添加物:エステルは特定の食品の食感や風味に寄与しています。
12. スルホン化反応
スルホン化は、芳香族化合物にスルホン酸基(-SO2OH)を導入する汎用性の高い有機反応です。この変換は、洗剤、染料、医薬品の合成など、さまざまな分野で重要な意味を持ちます。
スルホン化は通常、親電子芳香族置換(EAS)メカニズムによって進行します。主なステップは以下の通りです:
- 親電子剤の形成:三酸化硫黄(SO3)または発煙硫酸(H2SO4 + SO3)がスルホン化剤として働き、親電子的な SO3 分子を生成します。
- 芳香族親電子置換:SO3 親電子剤が芳香環の電子豊富な π 電子雲を攻撃し、σ 錯体中間体を形成します。
- 脱プロトン化:中間体がプロトンを失い、アリールスルホン酸生成物が形成されます。
ただし、スルホン化はしばしば可逆的です。酸性条件下で高温にすると、スルホン酸基は脱スルホン化を起こし、元の芳香族化合物と二酸化硫黄を放出することがあります。
スルホン化は、産業的および生物学的に関連するさまざまな分子の合成において、数多くの用途があります:
- 洗剤:広く使用されているアニオン界面活性剤であるドデシルベンゼンスルホン酸ナトリウム(SDS)は、ドデシルベンゼンをスルホン化することによって製造されます。
- 染料:スルホン化されたアゾ染料は鮮やかな色を示し、多様なテキスタイル用途に採用されています。
- 医薬品:抗生物質の一種であるスルホンアミド(サルファ剤)は、その抗菌活性のためにスルホン酸基の存在に依存しています。
これらの例以外にも、スルホン化はイオン交換樹脂、食品添加物、農薬など、他の数多くの化合物の合成において重要な役割を果たしています。
参考文献
- Callister, W. D., & Rethwisch, D. G. (2018). Materials Science and Engineering: An Introduction. Wiley.
- Chang, R. (2010). Chemistry (10th ed.). McGraw-Hill.
- Emsley, J. (2011). Nature’s Building Blocks: An A-Z Guide to the Elements. Oxford University Press.
- Green, J. (2018). An Introduction to the Chemical Process Industry. CRC Press.
- Kiehl, J. T. (2013). Industrial Chemical Processes: An Introduction. John Wiley & Sons.
- Meyers, R. A. (Ed.). (2001). Encyclopedia of Analytical Chemistry. Wiley.
- Seader, J. D., & Henley, E. J. (2011). Separation Process Principles. Wiley.
- Smith, J. M., Van Ness, H. C., & Abbott, M. M. (2005). Introduction to Chemical Engineering Thermodynamics (7th ed.). McGraw-Hill.
- Sperling, L. H. (Ed.). (2018). Introduction to Physical Polymer Science (4th ed.). Wiley.
- Turton, R., Bailie, R. C., Whiting, W. B., & Shaeiwitz, J. A. (2018). Analysis, Synthesis, and Design of Chemical Processes (5th ed.). Pearson.