수산화나트륨의 산업적 생산
1. 수산화나트륨 용액의 생산
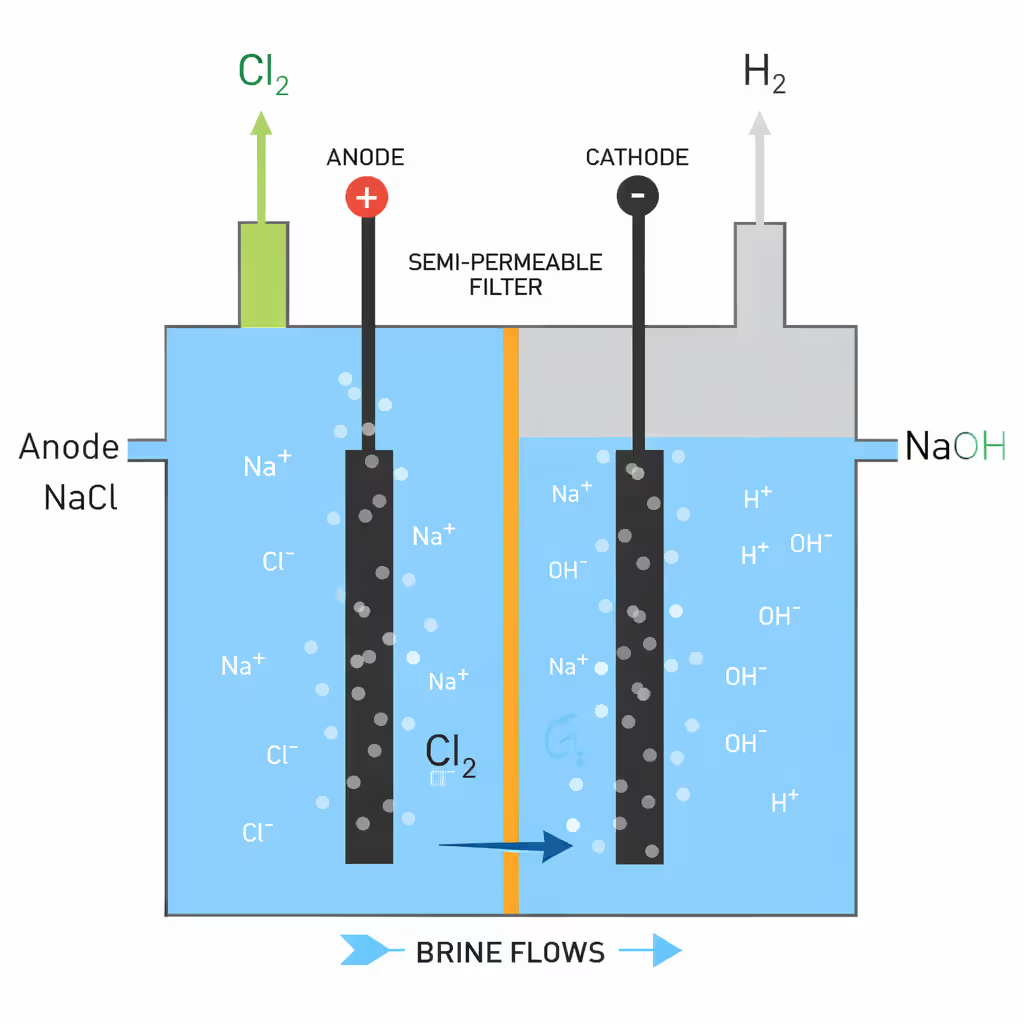
1.1. 염화나트륨의 전기분해
수산화나트륨 용액의 산업적 생산은 주로 염화나트륨의 전기분해를 통해 이루어집니다.
이 반응은 수산화나트륨 용액, 염소 가스, 수소 가스를 1: 0.88: 0.025의 질량비로 생성하며, 전체 반응식은 다음과 같습니다:
2 NaCl + 2 H2O → 2 NaOH + Cl2 + H2
이온교환막법(Membrane process)은 1980년대 초반, 클로르-알칼리(chlor-alkali) 생산을 위한 아말감법 및 격막법의 대안으로 도입되었습니다.
2004년 기준, 이온교환막법은 전체 클로르-알칼리 설비 용량의 44% 이상을 차지했습니다. 이 공정은 전기 에너지를 약 30% 절감하며 현재 가용한 최적의 기술로 간주되어, 신규 설비에서 이 기술의 사용이 점점 증가하고 있습니다.
일본에서는 1988년까지 비용 및 품질 문제를 고려하여 아말감법이 단계적으로 폐지되었고, 일부 격막법 공장들이 이온교환막법 공장으로 교체되었습니다.
아말감법(Amalgam process)에서는 80 – 120 °C에서 흑연 촉매 하에 나트륨 아말감과 물을 반응시켜 수산화나트륨 용액을 생산합니다. 이를 통해 얻은 50 wt % 용액은 냉각 후 원심 분리나 여과를 통해 수은을 제거한 뒤 별도의 추가 처리 없이 판매됩니다.
격막법(Diaphragm cell)은 약 18 wt %의 염화나트륨과 10-15 wt %의 수산화나트륨을 포함하는 용액을 생성합니다.
증발 과정에서 소모된 염화나트륨 용액과 함께 넘어온 불순물들은 분별 결정을 통해 용해도 한계까지 제거되지만, 염화나트륨 함량은 약 1 – 1.5 wt % 수준까지만 낮출 수 있습니다.
이온교환막법은 전해액의 혼합을 방지하기 위해 유압적으로 불투과성인 막을 사용합니다.
이 공정은 아말감법과 대등할 정도로 순도가 높고 염화물이 거의 없는 수산화나트륨 용액을 생산합니다. 다만, 전해조 가동이 중단될 경우 Cl‾ 이온이 막을 통해 확산되어 염화물 함량이 약 10배 정도 증가할 수 있습니다.
양극액(Anolyte)에 존재하는 황산염과 염소산염 역시 이온교환막 전해조에서 나오는 가성 용액의 불순물 농도에 영향을 미칩니다. 이는 양이온 선택성 막이 음이온에 대해 어느 정도 잔류 투과성을 가지고 있기 때문입니다. 대부분의 이온교환막 전해조는 NaOH 농도가 30 – 35 wt %일 때 최적의 경제적 성능을 보입니다.
전해조 내에서 50 wt % 수산화나트륨 용액을 직접 생산할 수 있는 이온교환 막이 개발되었으나, 전압이 상당히 상승하는 단점이 있습니다. 이러한 막은 증기 비용이 높고 전기 비용이 낮은 경우에만 실용적입니다.
30 – 33 wt % 수산화나트륨 용액은 증기 비용과 공장 규모에 따라 보통 2단 또는 3단 강하막식 증발기(Falling-film evaporator)에서 농축되어 상업용 50 wt % 용액이 됩니다.
3단 증발기의 증기 소비량은 NaOH(100%) 1톤당 0.55톤이며, 2단 증발기의 경우 0.71톤입니다. 이때 수산화나트륨 용액과 증기는 향류(Counter current)로 흐릅니다.
격막법 용액과 달리, 이온교환막 용액의 증발 과정에서는 열교환기를 오염시키거나 배관을 부식시킬 수 있는 고체 물질이 생성되지 않습니다.
니켈이나 스테인리스강과 같은 적절한 구조 재료를 사용할 경우, 증발 과정에서 혼입되는 금속 불순물은 약 1 wt ppm 수준입니다.
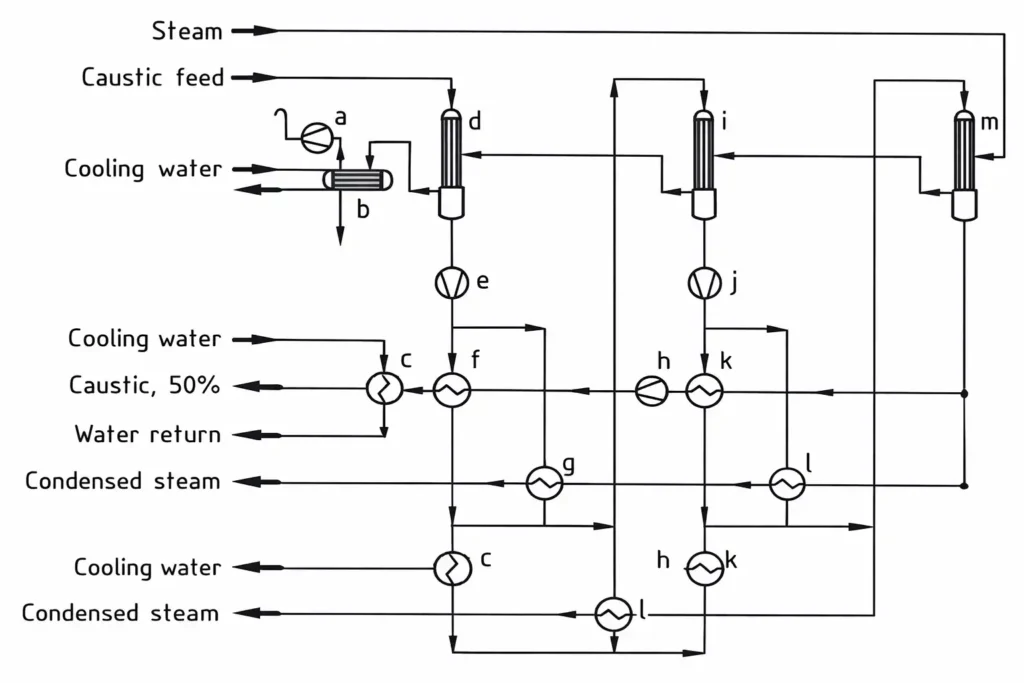
a) 진공 펌프; b) 응축기; c) 가성 용액 냉각기; d) 제1 증발기; e) 가성 용액 펌프; f) 제1 가성 용액 열교환기; g) 제2 열교환기; h) 가성 용액 펌프; i) 제2 증발기; j) 가성 용액 펌프; k) 제2 가성 용액 열교환기; l) 제1 열교환기; m) 제3 증발기
수산화나트륨을 생산하는 데 사용되는 세 가지 전기분해 공정은 각각 필요한 에너지 요구량이 다릅니다.
이온교환막법은 전기 에너지 소모가 NaOH 1톤당 2200 ~ 2500 kWh로 가장 적습니다. 하지만 50 wt % 용액을 만들기 위해서는 증기 형태로 NaOH 1톤당 200-300 kWh의 추가 에너지가 필요합니다.
반면, 격막법은 아말감법보다 전기 에너지는 적게 사용하지만 증발 단계에서 NaOH 1톤당 700-900 kWh가 필요합니다. 결과적으로 격막법이 총 에너지 소비량이 가장 높습니다.
전기 에너지 수요가 높기 때문에 연구자들은 전해조 전압을 낮추는 데 집중해 왔습니다. 이온교환막 공정은 연료 전지와 유사한 산소 확산 음극을 사용하여 전압을 약 1V 정도 낮출 수 있습니다. 다만, 이 경우에는 수소 부산물이 생성되지 않습니다.
이 기술은 큰 관심을 끌고 있습니다. 전해조 설계, 산소 확산 음극의 개발 및 전해조 설계로의 통합이 주요 연구 분야입니다. 또한 운전 파라미터와 전해조 주변 기기에 대한 연구도 진행 중입니다.
β-Al2O3 격막을 사용하여 350°C에서 용융 NaCl을 전기분해하는 기술도 유망합니다. 실험실 규모의 전해조에서는 NaOH 1톤당 2350 kWh의 전력 소비를 달성했습니다. 그럼에도 불구하고 이 기술은 아직 상업적 규모로 사용되지는 않고 있습니다.
1.2. 기타 공정
탄산나트륨 용액의 가성소다화(Causticization)를 이용한 수산화나트륨 생산은 가장 오래된 방법입니다. 전기분해가 등장하기 전까지는 유일한 방법이었습니다. 이 방법은 합성 또는 천연 탄산나트륨을 확보할 수 있는 기업들 사이에서 다시 관심을 받고 있습니다.
이 공정에서는 약 12%의 뜨거운 탄산나트륨 용액과 생석회를 혼합합니다. 침전된 탄산칼슘을 제거하고, 약 12%의 수산화나트륨 용액을 여러 단계에 걸쳐 증발시킵니다.
Na2CO3 + CaO·H2O → 2 NaOH + CaCO3
NaCl 및 Na2SO4를 포함하여 침전되는 불순물들은 여과되어 제거됩니다.
전기분해와 투석 전해조를 결합하는 것은 나트륨염을 해당하는 산과 알칼리로 분리하는 방법입니다:
Na2SO4 + 2 H2O → 2 NaOH + H2SO4
2실형 전해조에서는 양이온 또는 음이온 교환막을 사용할 수 있습니다. 3실형 전해조에서는 양이온 교환막과 음이온 교환막을 모두 사용할 수 있습니다. 또는 양이온, 음이온, 양극성 막(Bipolar membrane)을 조합하여 사용하는 다실형 전해조를 사용할 수도 있습니다.
그러나 산업적으로 운영되는 모든 전해조는 약간의 원료 염을 포함하는 희석된 수산화나트륨 용액(15-30 wt %)을 생성합니다.
따라서 이러한 유형의 공정은 얻어진 희석 수산화나트륨 용액을 중화 목적으로 재활용할 수 있는 공정에서 발생하는 나트륨염 함유 폐수를 처리하는 데 가장 적합합니다.
페라이트 회수 공정(Ferrite recovery process)은 소규모 종이 펄프 공장에 적합한 수산화나트륨 용액 생산의 대안을 제공합니다.
이 공정은 나트륨염과 유기 물질을 포함하는 폐액을 증발시키는 과정을 포함합니다. 생성된 잔류물을 Fe2O3와 혼합하여 소성하면 나트륨 페라이트가 형성되며, 이를 물로 분해하면 NaOH와 Fe2O3가 얻어집니다.
2. 무수 수산화나트륨의 생산

가성소다 고체라고도 불리는 고체 수산화나트륨은 수분 함량이 0.5 – 1.5 wt % 미만으로 떨어질 때까지 수산화나트륨 용액을 증발시켜 얻습니다.
가장 효율적인 에너지 활용은 스위스 바젤의 Bertrams 사가 건설한 공장의 흐름도(그림 1)와 같은 다단 설비를 통해 달성됩니다.
첫 번째 단계에서는 농축기에서 나오는 증기의 열을 이용해 예비 농축 장치에서 50 wt % 용액을 진공 증발시켜 농도를 약 60 wt %까지 높입니다.
두 번째 단계에서는 강하막식 증발기에서 용융염 열매체(NaNO2 – NaNO3 – KNO3)를 사용하여 400 °C 이상의 온도로 가열함으로써 약 99 wt %의 농도를 달성합니다.
농축된 생성물은 가스 리프트 펌프 역할을 하는 플래시 증발기로 공급되며, 여기서 용융 NaOH는 진공에 의해 가열된 상승관으로 끌어올려져 남은 수분이 증발하게 됩니다. 증기 기포는 용융 NaOH를 시스템의 가장 높은 지점까지 밀어 올리고, 그곳에서 증기는 펌프로 배출됩니다.
거의 무수에 가까운 용융물은 하강관을 통해 저장 용기로 이동하며, 그곳에서 컨디셔닝 설비로 펌핑됩니다.
조기 결정을 방지하기 위해 저장 용기, 펌프 및 배관은 반드시 가열되어야 합니다.
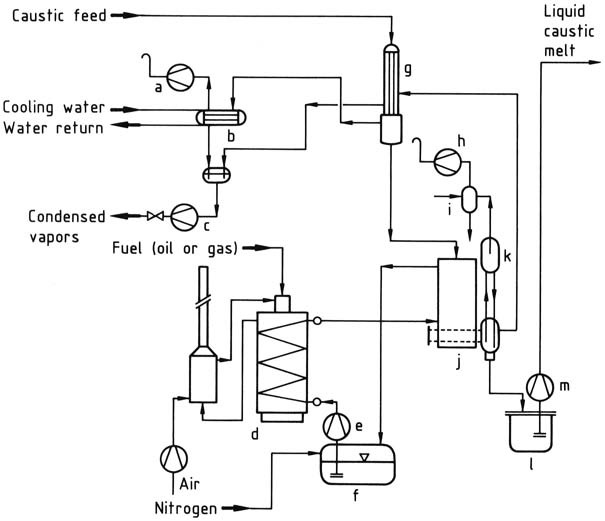
a) 진공 펌프; b) 응축기; c) 응축수 펌프; d) 용광로 장치; e) 염 용융 펌프; f) 가열 염 용융 탱크; g) 예비 농축 장치; h) 진공 펌프; i) 응축기; j) 낙하막 농축기; k) 플래시 증발기; l) 가열 가성소다 용융 탱크; m) 가성소다 용융 펌프
성형
고형화되지 않은 일수화물로 인한 덩어리짐(Caking)을 방지하기 위해, NaOH 용융물의 냉각 및 고형화는 NaOH의 응고점(322 °C)과 일수화물(NaOH· H2O, 62 °C)의 응고점을 모두 빠르게 통과하며 수행되어야 합니다.
시중에는 플레이크(Flakes), 프릴(Prills), 주조 블록(Cast blocks), 정제(Tablets), 브리켓(Briquettes) 및 과립(Granules) 등 다양한 형태의 고체 수산화나트륨이 판매되고 있습니다.
플레이크는 두께가 약 1.5 mm, 직경이 5 – 20 mm이며 겉보기 밀도는 약 0.9 kg/dm3입니다. 쉽게 부서지는 경향이 있어 취급 중에 먼지가 발생할 수 있습니다.
프릴의 겉보기 밀도는 1 kg/dm3보다 높으며 직경 0.1 – 0.8 mm(마이크로프릴) 또는 0.5 – 2.5 mm의 구형 형태를 띱니다.
1. 플레이크 (Flakes)
플레이크 생산은 용융 NaOH를 내부가 냉각된 회전 드럼이 부분적으로 잠겨 있는 조(Trough)에 공급하는 방식으로 이루어집니다. 용융 물질은 드럼 표면에서 고형화된 후 칼날에 의해 긁어내어집니다.
그 결과 생성된 NaOH 시트는 플레이크로 파쇄되어 중간 저장 사일로로 운반됩니다. 가교 현상(Bridging)을 방지하기 위해 재료는 작은 사일로에 보관되며 가능한 한 빨리 포대나 강철 드럼에 포장됩니다.
2. 프릴 (Prills)
프릴은 약 360 °C의 용융 NaOH를 분사하여 액적(Droplets)을 만듦으로써 생산됩니다. 회전 디스크나 바스켓을 사용하여 미세하게 분할된 액적을 만들며, 이들은 표면 장력에 의해 균일한 구체를 형성합니다.
프릴이 수직 통로를 따라 떨어질 때 공기를 위로 불어넣어 약 250 °C까지 냉각시킵니다. 완성된 제품은 깔대기에 수집되어 냉각 드럼으로 옮겨지며, 그곳에서 약 50 °C까지 냉각됩니다.
프릴은 플레이크보다 덩어리질 가능성이 적고 유동성이 좋으며 먼지가 거의 없어 사일로나 컨테이너 보관 및 운송에 이상적입니다.
3. 주조 블록 (Cast Blocks)
주조 블록의 경우, 용융 NaOH를 철제 드럼이나 유사한 용기에 직접 붓습니다. 철에 의한 추가 오염을 방지하기 위해 드럼 외부에 물을 뿌려 냉각시키며, 이는 용기 벽면에 수산화나트륨 고체 막을 즉시 형성하게 합니다.
4. 특수 형태
정제, 알약 또는 펠릿(Pellets)은 액적 공정을 통해 생산됩니다. 용융 NaOH를 은으로 만든 특수 장치에서 천천히 회전하며 냉각되는 테이블이나 컨베이어 벨트 위로 떨어뜨려 만듭니다.
이 공정은 금속 불순물 함량이 낮은 제품을 생산하므로 분석 목적으로 소량을 생산하는 데 매우 적합합니다.
참고 문헌
“Sodium Hydroxide”. Ullmann’s Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH.- https://onlinelibrary.wiley.com/doi/10.1002/14356007.a24_345.pub2