아세트산 무수물(Acetic Anhydride): 성질, 반응, 생산 및 용도
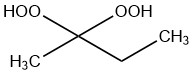
아세트산 무수물은 화학식 (CH3CO)2O를 가진 유기 화합물입니다. 자극적인 냄새가 나는 무색 액체로, 주로 아세틸화제(acetylating agent) 및 탈수제(dehydrating agent)로 사용됩니다. 1852년 염화 벤조일(benzoyl chloride)과 용융된 아세트산 칼륨의 반응을 통해 처음으로 제조되었습니다.
그 이후 아세트산 무수물은 다양한 연구 및 산업 응용 분야에서 매우 중요한 유기 중간체로 부상했습니다. 현재는 학계와 산업계의 합성 공정 전반에서 널리 사용되고 있습니다.
아세트산 무수물은 유럽종 포도(Vitis vinifera)에서 미량 발견되기도 하지만, 주로 산업적으로 생산됩니다.
목차
- 1. 아세트산 무수물의 물리적 성질
- 2. 아세트산 무수물의 화학 반응
-
2.1. 아세틸화 (Acetylation)
- 2.1.1. O-아세틸화
- 2.1.2. N-아세틸화
- 2.1.3. C-아세틸화
- 2.1.4. 무기산의 아세틸화
- 2.1.5. 산화물의 아세틸화
- 2.1.6. 염의 아세틸화
- 2.1.7. 아세톡시 실란의 생산
- 2.1.8. 고리 열림을 동반한 헤테로 고리 화합물에의 첨가
- 2.1.9. 탄소-탄소 이중 결합에의 산화적 첨가
- 2.1.10. 혼합 디아실 퍼옥사이드의 생산
- 2.1.11. N-옥사이드와의 반응
- 2.1.12. S-옥사이드와의 반응
- 2.1.13. 아실알(Acylals) 및 비닐 아세테이트의 생산
- 2.1.14. 삼불화 붕소 (Boron Trifluoride)
- 2.2. 탈수 (Dehydration)
- 2.3. α-양성자의 반응
- 2.4. 단일 카르보닐기의 반응
- 2.5. 은 케테나이드(Silver Ketenide)의 생산
-
2.1. 아세틸화 (Acetylation)
- 3. 아세트산 무수물의 생산
- 4. 아세트산 무수물의 용도
- 참고 문헌
1. 아세트산 무수물의 물리적 성질
아세트산 무수물은 자극적인 냄새가 특징인 무색 액체이며 강한 최루성(lachrymatory)을 가집니다. 아세트산 무수물과 관련된 주요 물리적 데이터는 아래 표와 같습니다.
| 성질 | 값 |
|---|---|
| 분자식 | (CH3CO)2O |
| 분자량 | 102.09 g/mol |
| 외관 | 무색 액체 |
| 밀도 | 1.08 g/cm3 |
| 끓는점 | 140.1 °C |
| 녹는점 | -73.1 °C |
| 물에 대한 용해도 | 격렬히 반응; 혼화성(miscible) |
| 냄새 | 자극적임 |
| 증기압 (25 °C) | 13 mmHg |
| 인화점 (밀폐식) | 49 °C |
| 자연 발화 온도 | 485 °C |
| 굴절률 | 1.392 |
| 점도 (25 °C) | 1.3 cP |
| 폭발 범위 (부피) | 2.3 – 10.6% |
-73.1 °C의 온도에서 아세트산 무수물은 고체에서 액체로의 상전이(녹는점)가 일어납니다. 반면, 101.3 kPa의 압력 하에서는 140 °C에서 끓습니다(끓는점).
아세트산 무수물은 극성 용매와 혼화성을 보이며 차가운 알코올에 용해되지만, 이때 분해 속도는 느립니다. 20 °C의 물에 용해될 때 용해도는 약 2.6 wt %이며, 점진적인 가수분해 과정을 동반합니다.
반대로, 15 °C에서 아세트산 무수물에 대한 물의 용해도는 약 10.7 wt %이며, 이 또한 점진적으로 분해되는 경향을 보입니다.
2. 아세트산 무수물의 화학 반응
아세트산 무수물은 광범위한 화학 반응을 나타내며 지방족 카르복실산 무수물로서 광범위하게 연구되어 왔습니다.
지난 25년 동안 아세트산 무수물은 수많은 논문과 특허에서 활용되어 왔으며, 특히 하이드록실기(-OH) 또는 아미노기(-NH)의 아세틸화(acetylation) 반응의 주요 단계로 사용됩니다.
2.1. 아세틸화 (Acetylation)
피리딘(pyridine) 내의 아세트산 무수물은 하이드록시, 아미노, 티올기를 포함한 다양한 분자에 아세틸기를 도입하는 데 사용됩니다.
2.1.1. O-아세틸화
아세트산 무수물은 아세트산으로는 달성하기 어렵거나 불가능한 알코올과의 에스테르화 반응에 매우 적합합니다. 이 과정에서 아세트산이 유리됩니다. 염기, 강산, 그리고 아세트산 나트륨과 같은 염이 촉매로 흔히 사용됩니다.
아세트산 무수물이 하이드록실기와 반응하는 대표적인 사례로는 아세틸 셀룰로오스, 아세틸살리실산(아스피린), 그리고 글리세롤 트리아세테이트의 형성이 있습니다.
아세트산 무수물이 과산화수소와 반응하면 반응물의 몰비에 따라 과아세트산(peracetic acid) 또는 디아세틸 퍼옥사이드(diacetyl peroxide)를 생성합니다.
(CH3CO)2O + 2 H2O2 → 2 CH3CO3H
(CH3CO)2O + H2O2 → CH3COOH + CH3CO3H
(CH3CO)2O + CH3CO3H → CH3COOOOCOCH3 + CH3COOH
2.1.2. N-아세틸화
NH기를 포함하는 화합물의 아세틸화는 다음 일반 식에 따라 아세트아미드를 생성합니다.
RR’NH + (CH3CO)2O → RR’NCOCH3 + CH3COOH
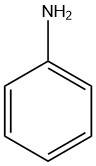
여기서 R과 R’은 수소(H) 또는 알킬기를 나타냅니다. 지방족 아민은 일반적으로 가열 없이 반응합니다. 예를 들어 아닐린(aniline)은 아세트아닐리드(acetanilide)를 생성하며, 이는 후속 질산화(nitration) 공정에서 산화를 방지하는 역할을 합니다.
N-아세틸화 반응은 일반적으로 OH기의 아세틸화보다 빠르게 진행되므로, 다중 작용기를 가진 화합물의 부분 아세틸화가 가능합니다. 그 예로 N-아세틸메티오닌-S-옥사이드 (1) 및 N-아세틸 안트라닐산 (2)과 같은 N-아세틸아미노산의 생산이 있습니다.
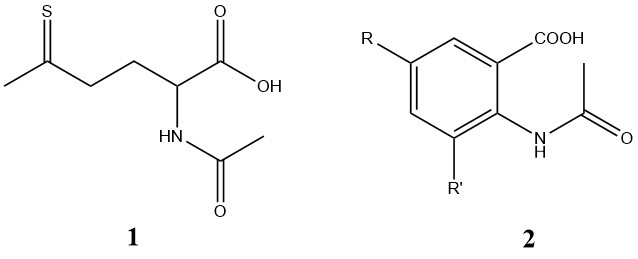
지방족 및 방향족을 불문하고 자유 NH기를 가진 아미드와 카바미드(carbamides)는 아세트산 무수물을 사용하여 아세틸화할 수 있습니다.
황산이 주로 촉매로 사용됩니다. 이 반응은 N,N,N’,N’-테트라아세틸에틸렌디아민((CH3CO)2NCH2CH2N(COCH3)2) 및 2,4,6,8-테트라아세틸아자바이사이클로[3.3.1]노난-3,7-디온과 같은 다양한 제품을 합성하는 데 응용됩니다.
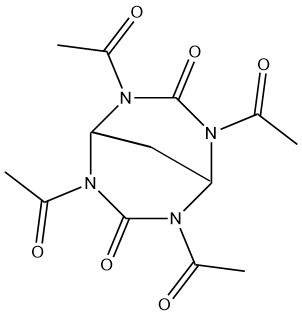
2.1.3. C-아세틸화
반응성 CH 결합을 가진 화합물은 때때로 촉매의 도움을 받아 아세트산 무수물로 아세틸화될 수 있습니다. 아세트산 칼륨을 촉매로 사용한 에틸 α-시아노아세토아세테이트(CH3COCH(CN)COOC2H5)의 생산과, 벤젠과 같은 방향족 탄화수소와의 프리델-크래프츠(Friedel-Crafts) 반응을 통한 아세토페논(acetophenone)의 형성이 주목할 만한 예입니다.
염화 알루미늄 존재 하에서 2,3-디메틸부타디엔 트리카르보닐 철의 아세틸화는 다음과 같은 착물을 생성합니다.
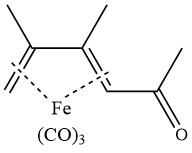
삼불화 붕소(boron trifluoride)에 의해 촉매되는 케톤과 아세트산 무수물의 반응은 β-디케톤의 형성으로 이어집니다.
트리아세틸메탄은 이소프로페닐 아세테이트, 아세트산 무수물, 그리고 염화 알루미늄 촉매로부터 직접 합성될 수 있습니다.
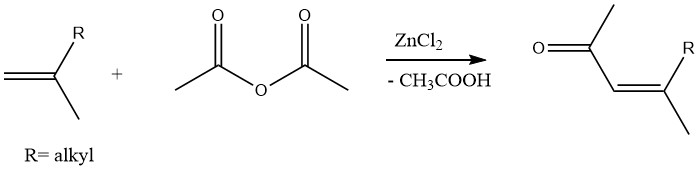
마찬가지로, 염화 아연을 촉매로 하여 올레핀을 아세트산 무수물로 아세틸화함으로써 불포화 메틸 케톤을 생산할 수 있습니다.
2.1.4. 무기산의 아세틸화
아세트산 무수물과 질산의 반응은 아세틸 나이트레이트(acetyl nitrate)를 형성하며, 이는 유기 화학에서 질산화제로 자주 사용됩니다. 아세틸 나이트레이트는 오산화이질소와 아세트산 무수물을 사용하여 합성할 수도 있습니다.
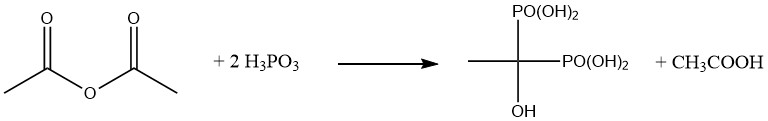
황산, 술폰산, 염산과 같은 다른 강산들도 아세트산 무수물과 혼합 무수물(mixed anhydrides)을 형성할 수 있습니다. 아세트산 무수물을 인산(phosphorous acid)과 반응시키면 1-하이드록시에탄-1,1-디포스폰산이 생성됩니다.
2.1.5. 산화물의 아세틸화
삼산화 안티모니는 아세트산 무수물과 반응하여 삼아세트산 안티모니(Sb(OCOCH3)3)를 생성합니다. 삼산화 크로뮴과의 유사한 반응은 크로밀 아세테이트 용액을 생성하며, 이는 올레핀 및 탄화수소의 산화에 자주 이용되지만 때때로 폭발 위험이 있으므로 주의해야 합니다.
2.1.6. 염의 아세틸화
다양한 염들은 대응하는 자유 산과 유사한 방식으로 카르복실산 무수물과 반응합니다.
Li−C−CR + (CH3CO)2O → CH3CO−C−CR + CH3COOLi
과산화 바륨을 아세트산 무수물로 처리하면 디아세틸 퍼옥사이드가 생성됩니다.
BaO2 + (CH3CO)2O → (CH3CO)2O2 + BaO
비닐 케톤을 생산하는 일반적인 방법에는 비닐 마그네슘 브로마이드와 아세트산 무수물의 반응이 포함됩니다.
2.1.7. 아세톡시 실란의 생산
아세트산 무수물은 다음 식에 따라 실란(silanes)과 반응합니다.
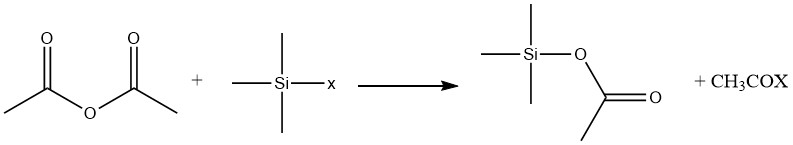
X = H, Cl, OR, NR2 인 경우.
2.1.8. 고리 열림을 동반한 헤테로 고리 화합물에의 첨가
이러한 반응들은 개념적으로 위에서 설명한 반응들과 유사합니다. 예를 들어, 강산성 또는 염기성 촉매 존재 하에 에틸렌 옥사이드로부터 에틸렌 글리콜 디아세테이트를 생산할 수 있으며, 트리옥산(trioxane)으로부터 옥시메틸렌 디아세테이트를 얻을 수 있습니다.
2.1.9. 탄소-탄소 이중 결합에의 산화적 첨가
산화적 첨가 반응은 상응하는 디아세테이트를 형성합니다. 예를 들어, 에틸렌을 아세트산 무수물에 첨가하면 에틸렌 글리콜 디아세테이트가 생성됩니다. 마찬가지로 부타디엔은 유사한 과정을 통해 1,4-디아세톡시-2-부텐으로 전환될 수 있습니다.
2.1.10. 혼합 디아실 퍼옥사이드의 생산
디아실 퍼옥사이드는 아세트산 나트륨 존재 하에서 지방족 알데히드와 아세트산 무수물의 혼합물에 산소를 반응시켜 합성할 수 있습니다.
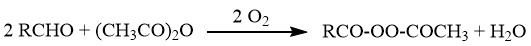
2.1.11. N-옥사이드와의 반응
N-옥사이드와의 반응은 특정 유형의 N-옥사이드에 따라 다양한 생성물을 생성합니다. 예를 들어, 피리딘-N-옥사이드는 2-아세틸옥시피리딘을 생성하는 반면, 4-피콜린-N-옥사이드는 4-아세틸옥시메틸렌피리딘과 3-아세틸옥시-4-메틸피리딘의 혼합물을 형성합니다. N-옥사이드의 폴로노브스키(Polonovski) 반응은 포름알데히드, 불포화 알데히드 및 산 아미드를 생성합니다.
2.1.12. S-옥사이드와의 반응
아세트산 무수물을 사용하여 술폭시드(sulfoxides)를 술피드(sulfides)로 환원시키는 것을 품머러(Pummerer) 반응이라고 합니다. 예를 들어, CH3SOR은 아세트산 무수물과 반응하여 CH3COOCH2SR과 CH3COOH를 생성합니다.
이 반응은 또한 아세트산 무수물과 함께 디메틸술폭시드 또는 테트라메틸렌 술폭시드 혼합물을 사용하여, 입체 장애가 있는 알코올을 포함한 1차 및 2차 알코올을 산화시켜 상응하는 카르보닐 화합물을 형성하는 데에도 활용됩니다.
2.1.13. 아실알(Acylals) 및 비닐 아세테이트의 생산
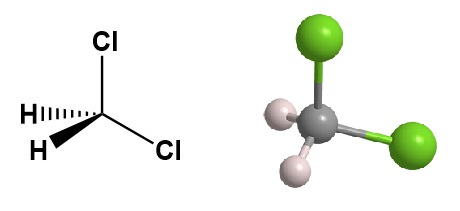
알데히드는 산 촉매 존재 하에서 아세트산 무수물과 반응하여 아실알을 형성합니다. 알데히드가 α-수소 원자를 가지고 있다면, 아세트산이 제거되면서 상응하는 비닐 아세테이트가 형성됩니다. 아연의 첨가는 아세트산 잔기의 절단을 촉진합니다. 이 공정은 특히 2,2-디클로로비닐 아세테이트의 합성에 적합합니다.
2.1.14. 삼불화 붕소 (Boron Trifluoride)
아세트산 무수물 및 치환된 아세트산 무수물은 따뜻한 물에서 분해되는 삼불화 붕소 착물을 사용하여 아세틸 케톤으로 변환될 수 있습니다.
2.2. 탈수 (Dehydration)
아세트산 무수물은 폭약 산업을 포함한 다양한 산업에서 탈수제로 응용됩니다. 탈수 성질의 대표적인 예로는 헤조겐(hexogen, 1,3,5-trinitrohexahydro-1,3,5-triazine) 생산이 있습니다.
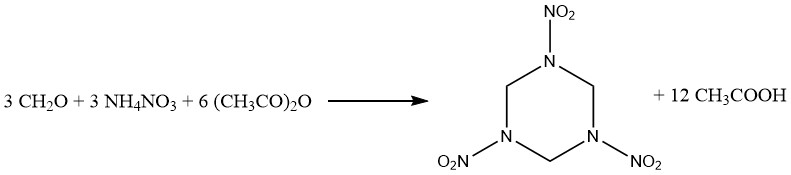
1,2,4,5-테트라하이드록시-3,6-디니트로사이클로헥산의 니트로에스테르 합성에서 아세트산 무수물은 수분 결합 능력을 위해 사용됩니다.
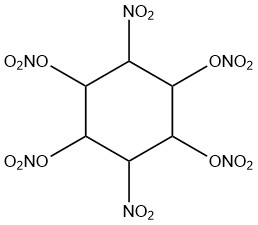
또한, 아세트산 무수물은 알독심(aldoximes)을 탈수시켜 알킬 시아니드를 생산하는 데 사용됩니다.
RCH=NOH + (CH3CO)2O → RCN + 2CH3COOH
추가적으로 아세트산 무수물은 수많은 고리화(cyclization) 반응에서 탈수제 역할을 합니다.
2.3. α-양성자의 반응
퍼킨(Perkin) 반응은 벤즈알데히드를 포함한 방향족 알데히드로부터 α, β-불포화산을 합성하는 데 널리 사용되는 방법입니다. 이 반응은 일반적으로 아세트산 칼륨 또는 아세트산 나트륨 존재 하에서 진행됩니다. 신남알아세트산 생산에도 사용됩니다.
유사한 반응으로는 아세트산 무수물과 산화제를 사용하는 산화적 카르복시메틸화, 그리고 긴 사슬 알켄을 대응하는 카르복실산 유도체로 전환하는 반응 등이 있습니다.
2.4. 단일 카르보닐기의 반응
어떤 경우에는 아세트산 무수물의 두 카르보닐기 중 하나만 반응에 참여하는 것이 가능합니다. 예를 들어, 염기 존재 하에서 아세트산 무수물이 시안화수소와 반응하면 화합물 (3)을 형성합니다. 마찬가지로, 그리냐르 시약(RMgBr) 존재 하에서 아세트산 무수물은 화합물 (4)를 생성합니다.
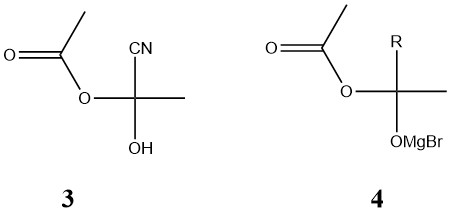
2.5. 은 케테나이드(Silver Ketenide)의 생산
아세트산 은과 아세트산 무수물을 실온에서 피리딘 존재 하에 반응시키면 은 케테나이드의 피리딘 착물을 형성합니다. 과량의 아세트산 무수물을 사용하면 생성된 혼합물을 피리딘과 아세트산의 분별 증류에 회부하여 은 케테나이드를 분리할 수 있습니다.
3. 아세트산 무수물의 생산
역사적으로 아세트산 무수물을 생산하는 가장 오래된 방법은 아세트산 나트륨을 염화 티오닐, 염화 술푸릴, 또는 염화 포스포릴과 같은 무기 염화물 과량과 함께 전환하는 것이었습니다.
이 공정에서 아세트산 나트륨의 절반은 염화 아세틸로 전환되고, 이것이 나머지 아세트산 나트륨과 반응하여 아세트산 무수물을 형성합니다.
또 다른 발전은 염화 알루미늄 존재 하에서 아세트산과 포스겐을 반응시켜 연속 가동이 가능하게 한 것입니다.
2 CH3COOH + COCl2 → (CH3CO)2O + 2 HCl + CO2
과거에 사용된 또 다른 두 가지 방법으로는 염화 아연과 같은 산 촉매 존재 하에서 에틸리덴 디아세테이트를 절단하여 아세트알데히드와 아세트산 무수물을 형성하는 방법과, 팔라듐(II) 촉매 상에서 비닐 아세테이트를 아세트산과 반응시키는 방법이 있었습니다. 그러나 이러한 공정들은 더 이상 산업적 중요성을 갖지 않습니다.
현재 아세트산 무수물의 생산은 주로 케텐 공정(ketene process) 또는 아세트알데히드 산화법을 통해 이루어집니다. 1983년에는 메틸 아세테이트의 카르보닐화(Halcon 공정)라고 알려진 또 다른 방법이 도입되었습니다.
서유럽에서는 아세트산 무수물의 약 77%가 케텐 공정을 통해 생산되며, 23%는 아세트알데히드 산화를 통해 생산됩니다.
미국에서는 테네시-이스트만(Tennessee-Eastman) 공장에 할콘 공정이 도입된 이후, 아세트산 무수물의 25%가 이 방법으로 생산되고 있으며 75%는 케텐 공정을 통해 생산됩니다.
3.1. 케텐 공정에 의한 아세트산 무수물의 생산
케텐 공정은 아세트산의 열분해를 통해 케텐을 형성하는 단계와, 이후 케텐을 아세트산과 반응시켜 아세트산 무수물을 생성하는 두 단계로 구성됩니다. 전체 반응은 다음과 같이 요약할 수 있습니다.
1. 아세트산의 열분해:
CH3COOH → CH2=C=O + H2O (ΔH = 147 kJ/mol)
2. 케텐과 아세트산의 반응:
CH2=C=O + CH3COOH → (CH3CO)2O (ΔH = -63 kJ/mol)
케텐과 물을 생성하기 위한 아세트산의 열분해는 미량의 인산 촉매 존재 하에 뜨거운 아세트산 증기를 700-750 °C 온도로 가열함으로써 수행됩니다.
케텐이 아세트산이나 물과 반응하기 전에 분리해낼 수 있도록 반응기 압력은 일반적으로 낮게 유지됩니다. 열분해 공정은 시크로말(Sicromal)과 같이 내열성이 매우 높은 강철 합금으로 만든 코일이 있는 다중 코일 반응기에서 진행됩니다.
케텐 공정은 원하는 생산 능력에 따라 여러 단계와 장비 구성을 포함합니다.
소규모 작업에서는 별도의 예열 및 분해 가마가 사용되며, 중간 규모 가마는 가스나 기름으로 가열되는 단일 챔버 가마로 구성되는 경우가 많습니다.
대규모 가마는 3개 또는 4개 챔버 시스템과 부분 가스 흐름을 사용하여 효과적으로 작동합니다. 중앙 증발기에서 공급되는 아세트산을 사용하여 여러 가마를 가동할 수도 있습니다.
아세트산의 열분해 후, 생성된 케텐은 아세트산과 반응하여 아세트산 무수물을 생성합니다. 이 반응에는 주로 스크러버(scrubber) 공정과 바커(Wacker) 공정의 두 가지 방식이 사용됩니다.
스크러버 공정에서는 라시히 링(Raschig rings)이 채워진 스크러버에서 순환하는 빙초산에 케텐이 흡수됩니다. 케텐은 주로 첫 번째 스크러버에서 흡수되며, 가공되지 않은 무수물을 포함하는 액체 혼합물이 수집 및 냉각됩니다.
바커 공정에서는 케텐이 액체 링 펌프(liquid-ring pump)를 통해 펌핑되며, 여기서 제어된 온도와 압력 하에 아세트산과 반응합니다. 가공되지 않은 무수물은 지속적으로 수집되며, 그중 일부는 반응 펌프로 되돌아갑니다.
반응에서 얻은 가공되지 않은 무수물은 증류를 통해 더욱 정제됩니다. 연속 증류와 불연속 증류 방식이 모두 사용됩니다.
불연속 증류에서는 초류(forerun), 중간류(middle run), 순수 무수물의 세 가지 분획을 얻습니다.
연속 증류는 여러 개의 칼럼을 사용하여 서로 다른 분획을 분리합니다. 무수물의 순도는 불연속 증류에서 보통 약 99% 수준이지만, 감압 하에서 조업함으로써 향상시킬 수 있습니다.
바커 공정은 후처리 공정(workup process)에도 활용되어, 추가 재료 없이 폐산을 처리할 수 있게 합니다. 이 공정은 높은 신뢰성과 에너지 절감 기능을 갖추고 있습니다.
100 kg의 아세트산 무수물을 생산하려면 농축된 묽은 아세트산을 고려할 때 약 122 kg의 아세트산이 필요합니다. 공정 수율은 약 75% 분해율에서 96% 이상입니다.
3.2. 아세탈데히드 산화에 의한 아세트산 무수물의 생산
아세트산 무수물은 아세탈데히드의 액상 산화에 의해 직접 생산될 수도 있습니다. 이 공정은 산소와 아세탈데히드로부터 형성된 과아세트산이 두 번째 아세탈데히드 분자와 반응하여 아세트산 무수물과 물을 생성하는 과정을 포함합니다.
이 공정에서는 효율적인 냉각과 적절한 촉매의 사용이 매우 중요합니다. 아세트산 망간과 아세트산 구리, 아세트산 코발트와 아세트산 니켈, 또는 고급 지방산의 코발트 및 구리 염과 같은 금속 염 조합이 촉매로 흔히 사용됩니다.
반응 온도를 유지하고 아세트산 무수물의 급격한 가수분해를 방지하기 위해 공정은 보통 40 °C에서 60 °C 사이에서 운영됩니다.
반응의 발열 특성으로 인해 효과적인 냉각이 필요하며, 물과 공비 혼합물(azeotropic mixtures)을 형성하는 메틸 아세테이트나 에틸 아세테이트와 같은 저비점 용매를 첨가하면 반응 혼합물에서 물을 분리하는 데 도움이 됩니다.
최종 제품에서 아세트산 무수물과 아세트산의 비율은 에틸 아세테이트와 아세탈데히드의 초기 비율에 따라 달라집니다.
실제로는 아세탈데히드와 에틸 아세테이트 혼합물을 아세트산 코발트 및 아세트산 구리 촉매를 첨가하여 산화시킵니다. 최적화된 반응 조건은 아세트산에 대한 아세트산 무수물의 비율을 더 높일 수 있습니다. 메틸렌 클로라이드, 디이소프로필 에테르, 사이클로헥사논, 에틸리덴 디아세테이트와 같은 다양한 용매가 공정에서 희석제로 사용될 수 있습니다.
산소와 아세탈데히드를 포함하는 가스 혼합물이 반응기로 도입되어 촉매 존재 하의 액상에서 산화가 일어납니다. 반응기 유출물은 수냉식 응축기를 통과하며, 이 응축기는 비응축성 가스의 분리기 역할도 합니다.
신선한 아세탈데히드가 충전 칼럼(packed column)으로 도입되어 응축기에서 나오는 오프가스(off-gas)와 결합합니다. 응축기와 칼럼에서 나온 응축액을 증류하여 원하는 제품을 얻습니다.
아세탈데히드는 비응축성 가스 흐름에서 회수됩니다. 오프가스에는 가연성 저비점 제품과 용매가 포함되어 있을 수 있으며, 이는 플레어(flare)를 통해 태워 없앨 수 있습니다.
위에 설명된 공정은 하나의 예시이며, 제조업체에 따라 반응기 구성 및 특정 반응 조건의 변형이 사용될 수 있습니다.
3.3. 메틸 아세테이트 카르보닐화에 의한 아세트산 무수물의 생산
아세트산 무수물 생산을 위한 전통적인 공정은 상당한 에너지를 소모하는 아세트산의 케텐 형성 열분해 과정을 포함합니다.
그러나 몬산토(Monsanto)의 아세트산 생산 공정과 메틸 아세테이트의 카르보닐화와 같은 대체 공정들이 개발되었습니다.
메틸 아세테이트를 카르보닐화하여 아세트산 무수물을 형성하는 방법은 1973년 할콘(Halcon)사에 의해 특허를 얻었으며, 이 공정을 사용한 첫 번째 공장은 1983년에 가동되었습니다. 이 공정에서는 메틸 아세테이트를 160 °C에서 190 °C 사이의 온도와 2-5 MPa의 일산화탄소 분압 하의 액상에서 카르보닐화합니다.
요오드화물 또는 기타 요오드 함유 물질로 활성화된 로듐 및 니켈 화합물을 포함한 다양한 촉매가 카르보닐화 반응에 사용될 수 있습니다. 로듐 촉매는 니켈 촉매보다 더 높은 활성을 보이며, 두 촉매 모두 95% 이상의 선택성을 나타냅니다.
합성에 사용되는 일산화탄소에 소량의 수소를 첨가하면 촉매의 활성과 수명이 향상됩니다. 크로뮴 화합물은 반응의 유도기(induction phase)를 단축하기 위해 사용될 수 있습니다.
카르보닐화 공정은 메틸 아세테이트 또는 디메틸 에테르로부터 시작할 수 있는데, 후자의 경우 아세트산 무수물로 전환되기 전에 메틸 아세테이트로 먼저 변환됩니다.
할콘 공정(그림 1)을 예로 들면, 건조된 메틸 아세테이트를 하스텔로이(Hastelloy) 라이닝이 된 반응기에 지속적으로 공급하며, 여기서 촉매 혼합물 존재 하에 175 °C에서 카르보닐화가 진행됩니다.
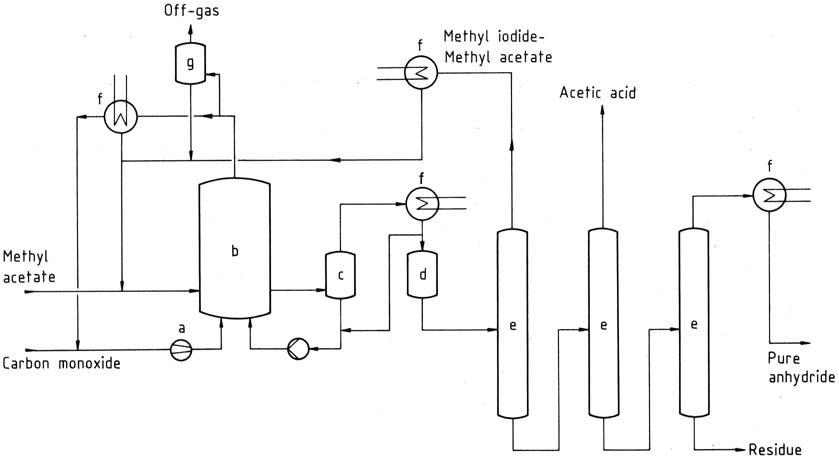
a) 압축기; b) 카르보닐화 반응기; c) 증발기; d) 흡착기; e) 증류 칼럼; f) 응축기; g) 스크러버
반응 중에 발생하는 열은 열 교환을 통해 제거되며, 메틸 아세테이트의 예열 및 저압 증기 생성에 활용됩니다. 반응하지 않은 일산화탄소는 응축성 가스 제거 후 재순환됩니다.
불활성 가스의 축적을 방지하기 위해 사이드 스트림(side stream)을 순수 아세트산 무수물로 세척합니다. 반응기를 떠나는 액체 반응 제품은 플래시 증류를 거쳐 재순환을 위해 촉매를 포함한 액체를 분리합니다.
가공되지 않은 무수물은 세 개의 연속된 칼럼에서 증류를 통해 더욱 정제되며, 마지막 칼럼에서 순도 99%의 아세트산 무수물을 생산합니다.
순수 무수물의 요오드화물 함량을 줄이기 위해 증류 공정 중에 아세트산 무수물 내 아세트산 칼륨 용액을 첨가할 수 있습니다.
이러한 대체 공정들은 에너지 소비 및 원료 활용 측면에서 전통적인 열분해 경로보다 이점을 제공하며, 석유 외에 석탄과 같은 다른 자원으로부터 아세트산 무수물을 생산할 수 있게 합니다.
4. 아세트산 무수물의 용도
아세트산 무수물은 아세틸화제와 탈수제로 모두 사용됩니다. 가장 두드러진 응용 분야 중 하나는 셀룰로오스의 대규모 아세틸화입니다. 그러나 아세트산 무수물이 사용되는 다른 여러 분야가 있습니다.
- 폴리(메틸아크릴이미드) 경질 폼 생산: 아미드기가 이미드기로 전환되는 동안 방출되는 암모니아의 결합제 역할을 합니다.
- 아세틸화된 플라스틱 보조제: 글리세롤 트리아세테이트, 아세틸 트리부틸 시트레이트, 아세틸 리시놀레이트 등이 포함됩니다.
- 폭약 생산: 특히 헤조겐 제조에 사용됩니다.
- 특정 유형의 브레이크액 생산.
- 시추용 유체(drilling fluids) 보조제 생산.
- 세제 산업: 특히 테트라아세틸에틸렌디아민(TAED)과 같은 저온 표백 활성제 생산에 사용됩니다.
- 염색 산업: 질산과 조합하여 질산화제로 사용되며, 용매 및 탈수 성질을 활용합니다.
- 다양한 유기 중간체 제조: 염화 클로로아세틸, 디아세틸 퍼옥사이드, 고급 카르복실산 무수물, 아세테이트, 그리고 삼불화 붕소 착물 등이 있습니다.
- 의약품 생산: 아세틸살리실산(아스피린), p-아세틸아미노페놀(아세트아미노펜), 아세트아닐리드, 아세토페나세틴, 테오필린, 염화 아세틸콜린, 술폰아미드, 호르몬, 비타민, 그리고 X선 조영제인 2,4,6-트리요오도-3,5-디아세틸아미도벤조산 등이 포함됩니다.
- 식품 산업 응용: 주로 동물성 및 식물성 지방의 아세틸화를 통해 원하는 용해도를 얻거나, 아세토스테아린(식용 포장재) 생산 및 식물성 기름의 청징(clarification)에 사용됩니다.
- 향료 및 향수: 에스테르 및 쿠마린(coumarin) 생산에 사용됩니다.
- 제초제: 메톨라클로르(Dual) 및 알라클로르(Lasso) 등.
참고 문헌
1. Acetic Anhydride and Mixed Fatty Acid Anhydrides; Ullmann’s Encyclopedia of Industrial Chemistry. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a01_065
2. https://lotus.naturalproducts.net/compound/lotus_id/LTS0216280